1 . 实验、类比、推理是化学学习的重要方法。已知:Mg可以在CO2中燃烧,生成MgO和C.某课外活动小组根据Mg与CO2的反应,探究Mg与SO2的反应,并探究其产物成分。
Ⅰ.探究Mg与SO2的反应

(1)写出A中制备SO2的化学方程式:___________ 。
(2)仪器a的作用是___________ ,装置B的作用之一是观察SO2的生成速率,为保证实验的严谨性其中的液体最好选择___________ (填序号)。
a.饱和NaHCO3溶液 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.浓硫酸
(3)补充完成D中的装置图并注明装置内选用的试剂。___________
Ⅱ.探究C中固体产物成分(已知C中Mg完全反应)
(4)将装置C中玻璃管内固体加入下图所示装置a中大试管内,若固体成分只有两种,某同学提出以下三种假设,依据充分反应后的现象,完成下列表格:

(5)为进一步验证假设③中MgS的存在,可将b中试剂换成CuSO4溶液。若MgS存在,则会产生黑色沉淀,请写出反应的化学方程式___________ 。
Ⅰ.探究Mg与SO2的反应

(1)写出A中制备SO2的化学方程式:
(2)仪器a的作用是
a.饱和NaHCO3溶液 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.浓硫酸
(3)补充完成D中的装置图并注明装置内选用的试剂。
Ⅱ.探究C中固体产物成分(已知C中Mg完全反应)
(4)将装置C中玻璃管内固体加入下图所示装置a中大试管内,若固体成分只有两种,某同学提出以下三种假设,依据充分反应后的现象,完成下列表格:

| 假设 | a中现象 | b中现象 |
| 假设① | 固体不完全溶解,无气泡产生 | 溶液不褪色 |
| 假设② | 固体不完全溶解,且有气泡产生 | 溶液褪色 |
| 假设③MgO和MgS | 固体完全溶解,且有气泡产生 |
(5)为进一步验证假设③中MgS的存在,可将b中试剂换成CuSO4溶液。若MgS存在,则会产生黑色沉淀,请写出反应的化学方程式
您最近一年使用:0次
2024-01-05更新
|
256次组卷
|
2卷引用:广东省深圳市高级中学2021-2022学年高一上学期期末考试化学试题
2 . 某化学兴趣小组为探究 的性质,按下图所示装置进行实验。请回答下列问题:
的性质,按下图所示装置进行实验。请回答下列问题:
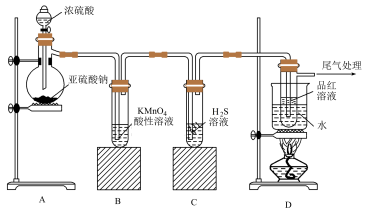
(1)装置A中盛放亚硫酸钠的仪器名称是___________ ,其中发生反应的化学方程式为:___________ 。
(2)实验过程中,装置B中的现象是___________ ,其中发生反应的离子方程式为___________ 。
(3)装置C中产生黄色沉淀,装置C中发生反应的化学方程式为___________ 。
(4)装置D的目的是探究 与品红溶液作用的可逆性,请写出相关实验操作及现象
与品红溶液作用的可逆性,请写出相关实验操作及现象___________ 。
(5)尾气可采用NaOH溶液吸收,写出相应的离子方程式___________ 。
 的性质,按下图所示装置进行实验。请回答下列问题:
的性质,按下图所示装置进行实验。请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是
(2)实验过程中,装置B中的现象是
(3)装置C中产生黄色沉淀,装置C中发生反应的化学方程式为
(4)装置D的目的是探究
 与品红溶液作用的可逆性,请写出相关实验操作及现象
与品红溶液作用的可逆性,请写出相关实验操作及现象(5)尾气可采用NaOH溶液吸收,写出相应的离子方程式
您最近一年使用:0次
3 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 检验乙醇是否含水 | 向乙醇中加入一小块钠,产生无色气体 | 乙醇中含有水 |
| B | 检验溴乙烷发生消去反应的产物 | 加热溴乙烷、乙醇和NaOH混合液,产生的气体通入溴水,溶液褪色 | 溴乙烷消去产物为乙烯 |
| C | 比较 与HClO的酸性强弱 与HClO的酸性强弱 | 往 溶液中通入 溶液中通入 气体,有沉淀产生 气体,有沉淀产生 | 酸性: |
| D | 将铜与浓硫酸反应产生的气体通入 溶液中 溶液中 | 产生白色沉淀 | 该气体中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列有关实验装置进行的相应实验,不能达到实验目的的是
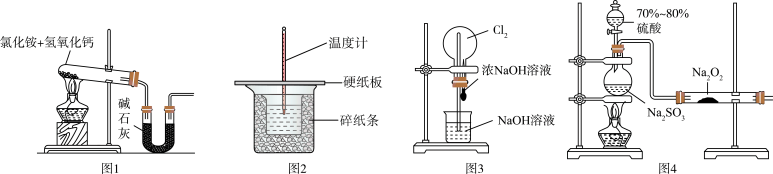

| A.用图1所示装置可制备得到干燥的氨气 |
| B.用图2所示装置可用于测定中和热 |
| C.用图3所示装置可以完成“喷泉”实验 |
| D.用图4所示装置能观察到右边装置中淡黄色固体变白色 |
您最近一年使用:0次
解题方法
5 . 下列实验报告记录的实验现象正确的是
| 实验 | 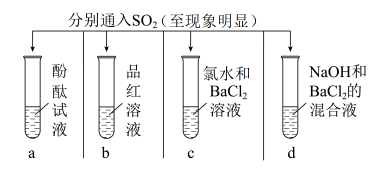 | ||||
| 现象 | A | 无色 | 不褪色 | 无色溶液 | 白色沉淀 |
| B | 红色 | 褪色 | 溶液变无色,白色沉淀 | 无色溶液 | |
| C | 无色 | 褪色 | 溶液变无色,白色沉淀 | 白色沉淀 | |
| D | 无色 | 褪色 | 无色溶液 | 无色溶液 | |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 1811年,法国化学家库尔图瓦将浓硫酸和海草灰(富含KI)混合后发现有紫色蒸气生成,该蒸气冷凝后变为紫黑色晶体。1813年经盖-吕萨克鉴定后正式将该物质命名为Iodine(碘)。
(1)将浓H2SO4滴入盛有KI固体的锥形瓶中,产生的气体能使湿润的醋酸铅试纸变黑(已知黑色物质为PbS),则该反应除生成I2以外,还会生成气体_______ (填化学式)。
(2)常温时HI为无色气体,易溶于水。其制备原理为3KI+H3PO4(浓) K3PO4+3HI↑。如图所示,制备并收集干燥的HI气体所需装置的接口顺序为(装置可重复使用,夹持和加热装置省略):a→e,f→
K3PO4+3HI↑。如图所示,制备并收集干燥的HI气体所需装置的接口顺序为(装置可重复使用,夹持和加热装置省略):a→e,f→_______ (已知浓H3PO4不易挥发和分解)。其中仪器Q的名称为_______ 。
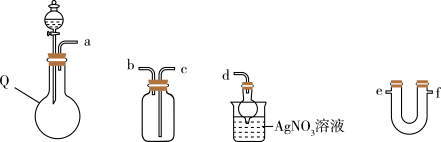
U形干燥管中的试剂为_______ 。若观察到_______ ,说明HI气体己收集满。
(3)久置KI溶液易被氧化导致变质,某实验小组取久置KI溶液进行实验,如图所示。
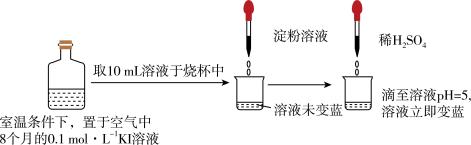
关于溶液立即变蓝的原因,该实验小组进行了如下探究。
①提出猜想
猜想Ⅰ:酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ:KI溶液久置过程中产生了IO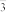 ,IO
,IO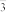 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。
②实验与结论。
③分析:久置KI溶液中IO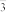 的产生可认为经历了两个过程
的产生可认为经历了两个过程_______ (写离子方程式);3I2+6OH-=5I-+IO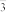 +3H2O。
+3H2O。
(1)将浓H2SO4滴入盛有KI固体的锥形瓶中,产生的气体能使湿润的醋酸铅试纸变黑(已知黑色物质为PbS),则该反应除生成I2以外,还会生成气体
(2)常温时HI为无色气体,易溶于水。其制备原理为3KI+H3PO4(浓)
 K3PO4+3HI↑。如图所示,制备并收集干燥的HI气体所需装置的接口顺序为(装置可重复使用,夹持和加热装置省略):a→e,f→
K3PO4+3HI↑。如图所示,制备并收集干燥的HI气体所需装置的接口顺序为(装置可重复使用,夹持和加热装置省略):a→e,f→
U形干燥管中的试剂为
(3)久置KI溶液易被氧化导致变质,某实验小组取久置KI溶液进行实验,如图所示。

关于溶液立即变蓝的原因,该实验小组进行了如下探究。
①提出猜想
猜想Ⅰ:酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ:KI溶液久置过程中产生了IO
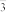 ,IO
,IO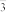 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。②实验与结论。
| 实验编号 | 实验方案 | 实验现象 | 结论与解释 |
| i | 往试管中加入10mL0.1mol•L-1新制KI溶液并加入几滴淀粉溶液, | 50min后溶液变蓝 | 猜想Ⅰ不成立。判断的依据是 |
| ii | 取少量KIO3溶液与少量KI溶液混合,加入淀粉溶液,再滴加稀H2SO4。 | 溶液立即 变蓝 | 猜想Ⅱ成立。写出相关反应离子方程式: |
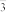 的产生可认为经历了两个过程
的产生可认为经历了两个过程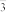 +3H2O。
+3H2O。
您最近一年使用:0次
7 . 氯元素是非常重要的非金属元素,某化学活动社团为了探究氯气的制法、性质和用途,设计了如下实验装置。
(1)实验室制备氯气的反应的化学方程式_____ 。
(2)B中饱和食盐水的作用是_____ 。
(3)广口瓶C、E中,有色布条褪色的是_____ (填“C”或“E”)。
(4)装置F可用于制漂白粉,漂白粉的有效成分是_____。
(5)烧杯G的作用是_____ ,请写出 中反应的离子方程式
中反应的离子方程式_____
(6)写出装置Ⅰ中反应的化学方程式_____ 。

(1)实验室制备氯气的反应的化学方程式
(2)B中饱和食盐水的作用是
(3)广口瓶C、E中,有色布条褪色的是
(4)装置F可用于制漂白粉,漂白粉的有效成分是_____。
A. | B. | C. | D. 和 和 |
 中反应的离子方程式
中反应的离子方程式(6)写出装置Ⅰ中反应的化学方程式
您最近一年使用:0次
名校
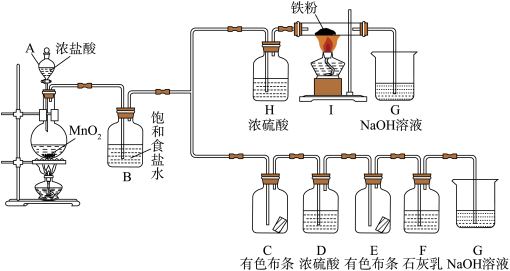
8 . 某食品膨松剂作用物质为NaHCO3,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
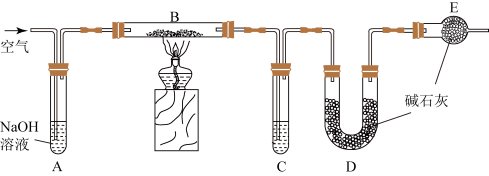
已知:碱石灰是固体氢氧化钠和氧化钙的混合物;2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
回答下列问题:
(1)A装置中NaOH溶液的作用是除去空气中的_______ ,C装置内所盛试剂是_______ ,E装置的作用是_______ ,若没有E装置,测定的结果_______ (填“偏高”、“偏低”或“无影响”);若没有A装置,B装置左侧用橡皮塞封闭,实验结果将_______ (填“偏高”、“偏低”或“无影响”)。
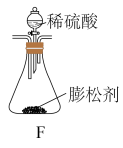
(2)充分加热后,测得D的质量增加6.6g,若装置B换为装置F进行实验(膨松剂质量相同)。不考虑导致误差因素,则测得D的质量增加_______ 。
(3)分解产物Na2CO3是重要化工原料,研究其性质:分别取少量NaCO3溶液,
①与碱反应:滴加澄清石灰水,现象为_______ ,
②与盐反应:滴加X溶液,产生白色沉淀,则X可能为_______ (写其中一种的名称)。
③与酸反应:滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式_______ ;
(4)取a克Na2CO3与NaHCO3混合物进行下列三组实验,其中能测定Na2CO3质量分数的是_______ (填序号)。
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙吸收,增重b克
任选上述合理方案中的一种,计算Na2CO3的质量分数为_______ 。


已知:碱石灰是固体氢氧化钠和氧化钙的混合物;2NaHCO3
 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑回答下列问题:
(1)A装置中NaOH溶液的作用是除去空气中的
(2)充分加热后,测得D的质量增加6.6g,若装置B换为装置F进行实验(膨松剂质量相同)。不考虑导致误差因素,则测得D的质量增加
(3)分解产物Na2CO3是重要化工原料,研究其性质:分别取少量NaCO3溶液,
①与碱反应:滴加澄清石灰水,现象为
②与盐反应:滴加X溶液,产生白色沉淀,则X可能为
③与酸反应:滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式
(4)取a克Na2CO3与NaHCO3混合物进行下列三组实验,其中能测定Na2CO3质量分数的是
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙吸收,增重b克
任选上述合理方案中的一种,计算Na2CO3的质量分数为
您最近一年使用:0次
2023-06-08更新
|
549次组卷
|
6卷引用:广东省佛山市南海区2022-2023学年高一上学期初高衔接学习素养测试化学试题
广东省佛山市南海区2022-2023学年高一上学期初高衔接学习素养测试化学试题广东省惠州市实验中学2022-2023学年高一上学期期中考试化学试题浙江省东阳市横店高级中学2022-2023学年高一上学期10月份检测化学试题四川省眉山市仁寿第一中学校南校区2023-2024学年高一上学期开学化学试题(已下线)期中测试卷一【测试范围:第一、二章】-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)江西省南昌市第一中学2023-2024学年高一上学期11月期中考试化学试题
解题方法
9 . 某小组用如图所示装置(夹持装置省略)制备 ,并探究
,并探究 与
与 溶液的反应。
溶液的反应。
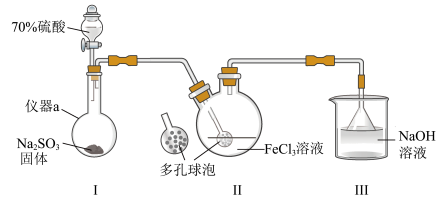
回答下列问题:
(1)实验开始后,装置Ⅱ中溶液很快由黄色变为红棕色;停止通入 ,放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色,有同学认为此时该溶液中含有
,放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色,有同学认为此时该溶液中含有 ,并进行以下实验验证:
,并进行以下实验验证:
(2)为探究装置Ⅱ中溶液颜色变化的原因,查阅资料后提出假设:该装置中可能存在以下两种化学反应。将反应②补充完整。_______ 。
①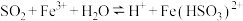 (红棕色);
(红棕色);
② Fe(HSO3)2+ + Fe3+ + ______ = _______ + 2Fe2+ + 3H+
(3)实验结束后向Ⅲ中加入适量Na2S溶液,并调节溶液至酸性,发现产生黄色浑浊,请写出此时发生反应的离子方程式__________________________________________ 。
 ,并探究
,并探究 与
与 溶液的反应。
溶液的反应。
回答下列问题:
(1)实验开始后,装置Ⅱ中溶液很快由黄色变为红棕色;停止通入
 ,放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色,有同学认为此时该溶液中含有
,放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色,有同学认为此时该溶液中含有 ,并进行以下实验验证:
,并进行以下实验验证:| 操作 | 现象 | 结论 |
取少量装置Ⅱ中溶液于试管中,先滴加 溶液,振荡 溶液,振荡 | 先无明显现象,加入 溶液后,现象是 溶液后,现象是 | 溶液中含有 |
①
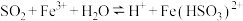 (红棕色);
(红棕色);② Fe(HSO3)2+ + Fe3+ + ______ = _______ + 2Fe2+ + 3H+
(3)实验结束后向Ⅲ中加入适量Na2S溶液,并调节溶液至酸性,发现产生黄色浑浊,请写出此时发生反应的离子方程式
您最近一年使用:0次
10 . 某校化学社团活动小组同学在学习完钠、氯及其化合物后设计了如下两组探究实验。请回答下列问题:
实验一:探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO3固体,D为固定蚊香的硬纸片)。
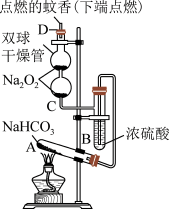
(1)Na2O2固体呈___________ 色。
(2)试管A中发生反应的化学方程式为___________ 。
(3)D处观察到的实验现象是___________ ,故推测Na2O2可用于___________ 。
实验二:某化学兴趣小组用图甲装置制备了氯气,并进行了一系列实验。
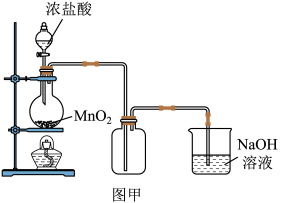
(4)盛有浓盐酸的仪器名称为___________ ;盛有NaOH溶液的仪器名称为___________ 。
(5)实验室制备氯气的反应的化学方程式是___________ 。
(6)乙同学认为图甲装置制备的氯气不纯净,其中混有_________ 气体和___________ ,需要对氯气进行洗气,其洗气过程是先让含杂质的氯气通过___________ 再通过___________ (填字母选项)。
A.浓硫酸 B.饱和食盐水 C.水
(7)乙同学对装置进行了如图乙改进。你认为合理吗?(合理则填入“合理”二字,如不合理则填入“不合理”并用文字说明理由)___________ 。
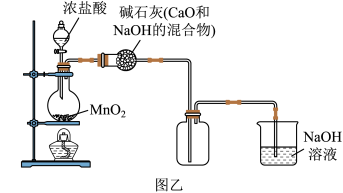
(8)在实验室制取氯气时,我们可以通过___________ (填字母选项)检验氯气已经收集满。
A.干燥的有色纸片 B.湿润的有色纸片 C.湿润的KI淀粉试纸
(9)最后将气体通入NaOH溶液中,作用是___________ (用文字描述)
实验一:探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO3固体,D为固定蚊香的硬纸片)。

(1)Na2O2固体呈
(2)试管A中发生反应的化学方程式为
(3)D处观察到的实验现象是
实验二:某化学兴趣小组用图甲装置制备了氯气,并进行了一系列实验。

(4)盛有浓盐酸的仪器名称为
(5)实验室制备氯气的反应的化学方程式是
(6)乙同学认为图甲装置制备的氯气不纯净,其中混有
A.浓硫酸 B.饱和食盐水 C.水
(7)乙同学对装置进行了如图乙改进。你认为合理吗?(合理则填入“合理”二字,如不合理则填入“不合理”并用文字说明理由)

(8)在实验室制取氯气时,我们可以通过
A.干燥的有色纸片 B.湿润的有色纸片 C.湿润的KI淀粉试纸
(9)最后将气体通入NaOH溶液中,作用是
您最近一年使用:0次



