1 . 取一定量的酸性硫酸锰( )溶液,向其中依次加入下列物质,对应现象如表所示:
)溶液,向其中依次加入下列物质,对应现象如表所示:
已知:
①金属铋(Bi)价态为+3时较稳定, 在水溶液中以离子形态存在;
在水溶液中以离子形态存在;
②铋酸钠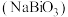 无色,难溶于水,高锰酸根离子呈紫红色;
无色,难溶于水,高锰酸根离子呈紫红色;
③淀粉溶液遇 变为蓝色。
变为蓝色。
(1)写出步骤1中的离子反应方程式______________ ,氧化产物为_____________ (填离子符号)。
(2)写出步骤2中的离子反应方程式________________________________ 。
(3)步骤2中过量的 可以氧化
可以氧化 ,则步骤3中现象A为
,则步骤3中现象A为________________________ 。
(4)由上述现象可知, 、
、 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为______________ 。
(5)根据上述结论,推断下列离子反应可能发生且书写正确的是__________ (填字母)。
a.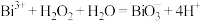
b.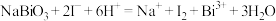
c.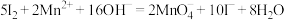
d.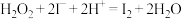
 )溶液,向其中依次加入下列物质,对应现象如表所示:
)溶液,向其中依次加入下列物质,对应现象如表所示:| 步骤1 | 步骤2 | 步骤3 | |
| 依次加入 | 适量 | 过量的 溶液 溶液 | 适量 -淀粉混合液 -淀粉混合液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 现象A |
①金属铋(Bi)价态为+3时较稳定,
 在水溶液中以离子形态存在;
在水溶液中以离子形态存在;②铋酸钠
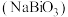 无色,难溶于水,高锰酸根离子呈紫红色;
无色,难溶于水,高锰酸根离子呈紫红色;③淀粉溶液遇
 变为蓝色。
变为蓝色。(1)写出步骤1中的离子反应方程式
(2)写出步骤2中的离子反应方程式
(3)步骤2中过量的
 可以氧化
可以氧化 ,则步骤3中现象A为
,则步骤3中现象A为(4)由上述现象可知,
 、
、 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(5)根据上述结论,推断下列离子反应可能发生且书写正确的是
a.
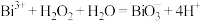
b.
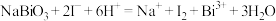
c.
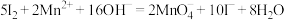
d.
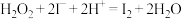
您最近一年使用:0次
名校
解题方法
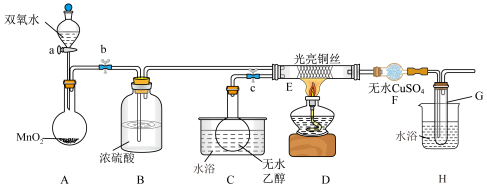
2 . 某同学设计了如图所示装置(夹持装置已省略)进行乙醇的催化氧化实验。先按图示安装好实验装置,关闭活塞 、
、 、
、 ,在铜丝的中间部分加热片刻,然后打开活塞
,在铜丝的中间部分加热片刻,然后打开活塞 、
、 、
、 ,通过控制活塞
,通过控制活塞 和
和 ,有节奏(间歇性)地通入气体。已知:乙醛可被氧化为乙酸,乙醛的沸点:
,有节奏(间歇性)地通入气体。已知:乙醛可被氧化为乙酸,乙醛的沸点: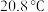 ,乙酸的沸点:
,乙酸的沸点: 。
。
回答下列问题:
(1) 的作用是
的作用是_____ 。
(2)硬质玻璃管 中可观察到
中可观察到_____ 现象,实验过程中乙醇催化氧化的化学方程式为_____ 。
(3) 和
和 两个水浴的作用不相同。
两个水浴的作用不相同。 的作用是
的作用是_____ , 的作用是
的作用是_____ 。
(4)仪器 的作用是
的作用是_____ 。
(5)若试管 中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_____ 。要除去该物质,可在混合液中加入_____ (填字母),然后再通过(填实验操作)即可得到乙醛_____ 。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
(6)该小组通过以上实验探究做出了如下猜想,你认为正确的是_____ (填字母)。
a.表面被氧化为黑色的铜丝在酒精灯上灼烧,可闻到刺激性气味
b.乙醇催化氧化生成乙醛时,乙醇分子中只有 键发生断裂
键发生断裂
c.利用金属钠能检验试管 中有没有未反应的乙醇
中有没有未反应的乙醇
 、
、 、
、 ,在铜丝的中间部分加热片刻,然后打开活塞
,在铜丝的中间部分加热片刻,然后打开活塞 、
、 、
、 ,通过控制活塞
,通过控制活塞 和
和 ,有节奏(间歇性)地通入气体。已知:乙醛可被氧化为乙酸,乙醛的沸点:
,有节奏(间歇性)地通入气体。已知:乙醛可被氧化为乙酸,乙醛的沸点: ,乙酸的沸点:
,乙酸的沸点: 。
。
回答下列问题:
(1)
 的作用是
的作用是(2)硬质玻璃管
 中可观察到
中可观察到(3)
 和
和 两个水浴的作用不相同。
两个水浴的作用不相同。 的作用是
的作用是 的作用是
的作用是(4)仪器
 的作用是
的作用是(5)若试管
 中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
(6)该小组通过以上实验探究做出了如下猜想,你认为正确的是
a.表面被氧化为黑色的铜丝在酒精灯上灼烧,可闻到刺激性气味
b.乙醇催化氧化生成乙醛时,乙醇分子中只有
 键发生断裂
键发生断裂c.利用金属钠能检验试管
 中有没有未反应的乙醇
中有没有未反应的乙醇
您最近一年使用:0次
3 . 某小组探究镁与醋酸溶液反应的实质。
【实验】在常温水浴条件下进行实验Ⅰ~Ⅲ,记录生成气体的体积和溶液 变化,如图1、2。
变化,如图1、2。
Ⅰ.取 光亮的镁屑(过量)放入
光亮的镁屑(过量)放入 溶液中;
溶液中;
Ⅱ.取 光亮的镁屑放入
光亮的镁屑放入 溶液(
溶液( )中;
)中;
Ⅲ.取 光亮的镁屑放入
光亮的镁屑放入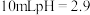 的
的 溶液中。
溶液中。
【数据】
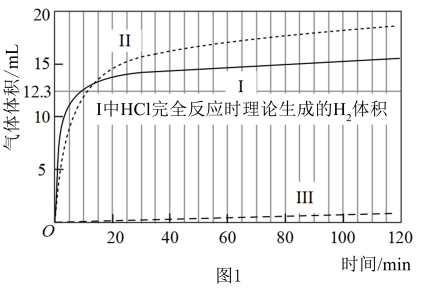
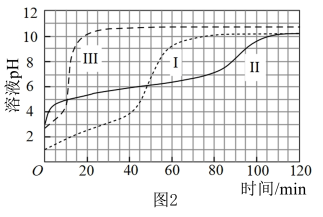
(1)起始阶段Ⅰ中主要反应的离子方程式为___________ 。
(2)Ⅱ起始溶液中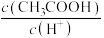 约为
约为___________ (用“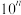 ”表示)。
”表示)。
(3)起始阶段,导致Ⅱ和Ⅲ中气体生成速率差异的主要因素不是 ,实验证据是
,实验证据是___________ 。
基于溶液组成预测Ⅱ的气体生成速率快于Ⅲ的原因是 能直接与
能直接与 反应。
反应。
验证:【实验Ⅳ】室温下,将一小段打磨光亮的镁条投入 冰醋酸中,立即产生大量气体。
冰醋酸中,立即产生大量气体。
(4)选择冰醋酸的理由是___________ 。
探究醋酸溶液中与 反应的主要微粒。
反应的主要微粒。
【实验Ⅴ】与实验Ⅱ相同的条件和试剂用量,将溶液换成含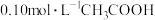 和
和 的
的 混合溶液(
混合溶液( )。各时刻气体生成的瞬时速率(
)。各时刻气体生成的瞬时速率( )对比如下。
)对比如下。
(5)①将a~c时刻对应溶液中的粒子浓度进行排序: :
:___________ (用“>”或“=”连接表示,下同);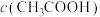 :
:___________ 。
②结合a~c中微粒浓度的比值分析, 和
和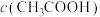 中哪一因素对气体生成速率影响更大:
中哪一因素对气体生成速率影响更大:___________ 。
(6)综合以上实验得出结论:
①镁与醋酸溶液反应时, 、
、 、
、 均能与镁反应产生氢气。
均能与镁反应产生氢气。
② 反应产生气体的主要微粒是
反应产生气体的主要微粒是___________ 。
【实验】在常温水浴条件下进行实验Ⅰ~Ⅲ,记录生成气体的体积和溶液
 变化,如图1、2。
变化,如图1、2。Ⅰ.取
 光亮的镁屑(过量)放入
光亮的镁屑(过量)放入 溶液中;
溶液中;Ⅱ.取
 光亮的镁屑放入
光亮的镁屑放入 溶液(
溶液( )中;
)中;Ⅲ.取
 光亮的镁屑放入
光亮的镁屑放入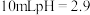 的
的 溶液中。
溶液中。【数据】


(1)起始阶段Ⅰ中主要反应的离子方程式为
(2)Ⅱ起始溶液中
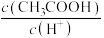 约为
约为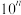 ”表示)。
”表示)。(3)起始阶段,导致Ⅱ和Ⅲ中气体生成速率差异的主要因素不是
 ,实验证据是
,实验证据是基于溶液组成预测Ⅱ的气体生成速率快于Ⅲ的原因是
 能直接与
能直接与 反应。
反应。验证:【实验Ⅳ】室温下,将一小段打磨光亮的镁条投入
 冰醋酸中,立即产生大量气体。
冰醋酸中,立即产生大量气体。(4)选择冰醋酸的理由是
探究醋酸溶液中与
 反应的主要微粒。
反应的主要微粒。【实验Ⅴ】与实验Ⅱ相同的条件和试剂用量,将溶液换成含
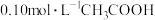 和
和 的
的 混合溶液(
混合溶液( )。各时刻气体生成的瞬时速率(
)。各时刻气体生成的瞬时速率( )对比如下。
)对比如下。| a.Ⅴ起始速率 | b.Ⅱ起始速率 | c.Ⅱ进行到 时速率 时速率 |
| 2.1 | 2.3 | 0.8 |
(5)①将a~c时刻对应溶液中的粒子浓度进行排序:
 :
: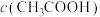 :
:②结合a~c中微粒浓度的比值分析,
 和
和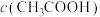 中哪一因素对气体生成速率影响更大:
中哪一因素对气体生成速率影响更大:(6)综合以上实验得出结论:
①镁与醋酸溶液反应时,
 、
、 、
、 均能与镁反应产生氢气。
均能与镁反应产生氢气。②
 反应产生气体的主要微粒是
反应产生气体的主要微粒是
您最近一年使用:0次
4 . 2020年初,突如其来的新型冠状肺炎在全世界肆虐,社会生产、人民生活都受到了一定程度的影响,同学们也不能正常上学。“停课不停学”的网络课程学习让同学们充分发挥了自主学习能力。某中学的几位同学就查阅了大量资料,并进行相关实验探究,来认识可以有效灭活新型冠状病毒的含氯消毒剂一次氯酸钠 。
。
I.次氯酸钠的制备和性质
(1)84消毒液制取的主要原料是氯气,实验室制氯气的化学方程式是:___________ 。制得氯气 (标准状况)。需要消耗
(标准状况)。需要消耗
___________ 克,被氧化的 的物质的量是多少
的物质的量是多少___________ 。
(2)家中常用的84消毒液的有效成分即是次氯酸钠, 中氯元素的化合价为
中氯元素的化合价为___________ 。若将 通入冷的稀
通入冷的稀 溶液中则可制得消毒液,该反应的离子方程式为
溶液中则可制得消毒液,该反应的离子方程式为___________ 。
(3)在查阅资料中,同学们发现“百度百科”中有这样一句话:家用洁测灵不能和84消毒液混用,否则会产生氯气,引起中毒,发生的反应为: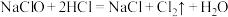 。该反应中
。该反应中
___________ (“得到”或“失去”)电子,每转移 个电子,反应生成标准状况下氯气
个电子,反应生成标准状况下氯气___________ L。
II.同学们探究84消毒液在不同下使红纸褪色的情况,做了如下实验,
步骤1:将 市售84消毒液稀释100倍,测得稀释后溶液的
市售84消毒液稀释100倍,测得稀释后溶液的 ;
;
步骤2:将稀释后的溶液各 分别加入a、b、c三个洁净的烧杯中;
分别加入a、b、c三个洁净的烧杯中;
步骤3:用 溶液将a、b、c三个烧杯内溶液的分别调至10、7和4
溶液将a、b、c三个烧杯内溶液的分别调至10、7和4
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如表。
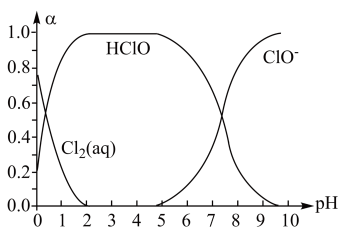
已知溶液中 和
和 的物质的量分数(
的物质的量分数( )随溶液变化的关系如图所示:
)随溶液变化的关系如图所示:
(4)由实验现象可获得结论:溶液的 在4-10范围内,
在4-10范围内, 越大,红纸褪色
越大,红纸褪色___________ (填“越快”或“越慢”)。
(5)结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是___________ 。
 。
。I.次氯酸钠的制备和性质
(1)84消毒液制取的主要原料是氯气,实验室制氯气的化学方程式是:
 (标准状况)。需要消耗
(标准状况)。需要消耗
 的物质的量是多少
的物质的量是多少(2)家中常用的84消毒液的有效成分即是次氯酸钠,
 中氯元素的化合价为
中氯元素的化合价为 通入冷的稀
通入冷的稀 溶液中则可制得消毒液,该反应的离子方程式为
溶液中则可制得消毒液,该反应的离子方程式为(3)在查阅资料中,同学们发现“百度百科”中有这样一句话:家用洁测灵不能和84消毒液混用,否则会产生氯气,引起中毒,发生的反应为:
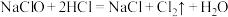 。该反应中
。该反应中
 个电子,反应生成标准状况下氯气
个电子,反应生成标准状况下氯气II.同学们探究84消毒液在不同下使红纸褪色的情况,做了如下实验,
步骤1:将
 市售84消毒液稀释100倍,测得稀释后溶液的
市售84消毒液稀释100倍,测得稀释后溶液的 ;
;步骤2:将稀释后的溶液各
 分别加入a、b、c三个洁净的烧杯中;
分别加入a、b、c三个洁净的烧杯中;步骤3:用
 溶液将a、b、c三个烧杯内溶液的分别调至10、7和4
溶液将a、b、c三个烧杯内溶液的分别调至10、7和4步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如表。
| 烧杯 | 溶液的 | 现象 |
| a | 10 |  后,红纸基本不褪色; 后,红纸基本不褪色; 后红纸褪色 后红纸褪色 |
| b | 7 |  后,红纸颜色变浅; 后,红纸颜色变浅; 后红纸褪色 后红纸褪色 |
| c | 4 |  后,红纸颜色比b烧杯中 后,红纸颜色比b烧杯中 后的浅; 后的浅; 后红纸褪色 后红纸褪色 |
 和
和 的物质的量分数(
的物质的量分数( )随溶液变化的关系如图所示:
)随溶液变化的关系如图所示:
(4)由实验现象可获得结论:溶液的
 在4-10范围内,
在4-10范围内, 越大,红纸褪色
越大,红纸褪色(5)结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次
5 . 氯气是一种重要的化工原料,如图是一些含氯产品。
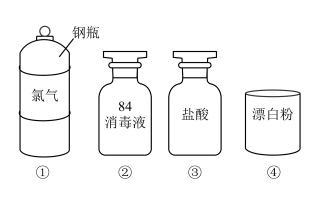
(1)①中钢瓶上应贴的标签为_________(填字母)。
(2)“84消毒液”在抗击新冠肺炎疫情中发挥了重要作用。下列说法不正确的是_________(填字母)。
(3)如图是探究氯气性质和用途的实验装置。
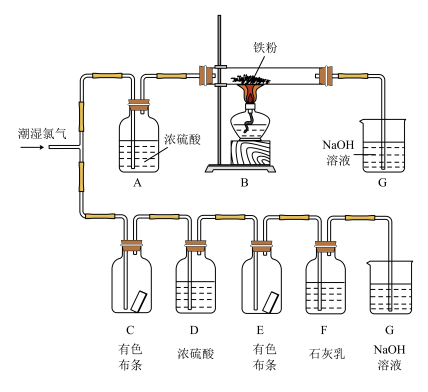
①写出B中的化学反应方程式_________ 。
②该实验中设置装置C、D、E的主要目的是_________ ,与该实验目的直接相关的实验现象是_________ 。
③装置F可用于制漂白粉,漂白粉的有效成分是_________ (填化学式)。
④烧杯G的作用是_________ (用离子方程式表示)。

(1)①中钢瓶上应贴的标签为_________(填字母)。
| A.腐蚀品 | B.爆炸品 | C.有毒品 | D.易燃品 |
| A.“84消毒液”为混合物 |
| B.“84消毒液”可用于杀灭新型冠状病毒 |
| C.“84消毒液”杀菌消毒的过程中并未发生氧化还原反应 |
| D.“84消毒液”除能杀菌消毒外,还可作漂白剂 |

①写出B中的化学反应方程式
②该实验中设置装置C、D、E的主要目的是
③装置F可用于制漂白粉,漂白粉的有效成分是
④烧杯G的作用是
您最近一年使用:0次
解题方法
6 . 某化学兴趣小组制取SO2并探究SO2与FeCl3溶液的反应,所用装置如图所示。下列说法错误的是
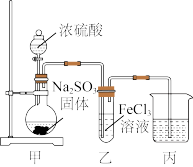

| A.甲中浓硫酸浓度不宜过大,以防止氧化亚硫酸钠 |
| B.乙中反应的氧化剂与还原剂物质的量之比为2:1 |
| C.为尽快观察到乙中的实验现象,可增大FeCl3溶液浓度或加热 |
| D.丙装置的作用是吸收剩余的SO2,防止污染空气,但是应该连接倒扣漏斗 |
您最近一年使用:0次
名校
解题方法
7 . 氮的氧化物( )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成
还原生成 。某同学在实验室中对
。某同学在实验室中对 与
与 反应进行了探究。回答下列问题:
反应进行了探究。回答下列问题:
I.氨气的制备
某化学实验小组同学利用如图装置制备氨气,并探究氨气的性质(部分仪器已略去)。
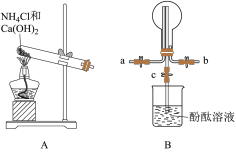
(1)实验室制备氨气的化学方程式为_________ 。
(2)若观察到装置B中的烧瓶内产生了红色喷泉,你认为引发喷泉的操作应是_________ 。
(3)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是_________ (填序号)。
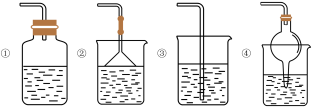
II.氨气与二氧化氮的反应
(4)将I中收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入
充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。
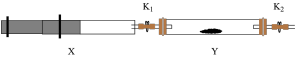
在一定温度下按图示装置进行实验。打开 ,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式
,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式_________ 。
(5)若有 和
和 的混合物1mol,充分反应。反应后所得到产物中,经氧化得到的
的混合物1mol,充分反应。反应后所得到产物中,经氧化得到的 比经还原得到的
比经还原得到的 多1.4g,则反应混合物中
多1.4g,则反应混合物中 与
与 的体积比是
的体积比是_________ 。
 )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成
还原生成 。某同学在实验室中对
。某同学在实验室中对 与
与 反应进行了探究。回答下列问题:
反应进行了探究。回答下列问题:I.氨气的制备
某化学实验小组同学利用如图装置制备氨气,并探究氨气的性质(部分仪器已略去)。

(1)实验室制备氨气的化学方程式为
(2)若观察到装置B中的烧瓶内产生了红色喷泉,你认为引发喷泉的操作应是
(3)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

II.氨气与二氧化氮的反应
(4)将I中收集到的
 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入
充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。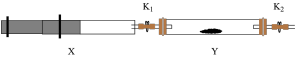
在一定温度下按图示装置进行实验。打开
 ,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式
,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式(5)若有
 和
和 的混合物1mol,充分反应。反应后所得到产物中,经氧化得到的
的混合物1mol,充分反应。反应后所得到产物中,经氧化得到的 比经还原得到的
比经还原得到的 多1.4g,则反应混合物中
多1.4g,则反应混合物中 与
与 的体积比是
的体积比是
您最近一年使用:0次
名校
解题方法
8 . 下表是元素周期表的一部分,请针对表中标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是_______ (填元素符号,下同)。
(2)这些元素的最高价氧化物对应水化物中碱性最强的是_______ (填化学式,下同),具有两性的是_______ ,这两种物质发生反应的离子方程式为_______ 。
(3)写出⑤⑨形成化合物的电子式:_______ 。
(4)某化学研究性学习小组利用以下装置制取并探究②的最简单氢化物的性质。在A装置中发生反应的化学方程式为_______ 。
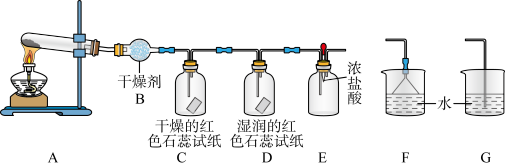
ⅰ.B装置中的干燥剂是_______ 。
ⅱ.C、D 装置中试纸颜色会发生变化的是_______ (填”C”或“D”)。
ⅲ.当实验进行段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到 E装置中的现象是_______ 。
ⅳ.为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_______ (填“F”或“G”)。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)这些元素的最高价氧化物对应水化物中碱性最强的是
(3)写出⑤⑨形成化合物的电子式:
(4)某化学研究性学习小组利用以下装置制取并探究②的最简单氢化物的性质。在A装置中发生反应的化学方程式为

ⅰ.B装置中的干燥剂是
ⅱ.C、D 装置中试纸颜色会发生变化的是
ⅲ.当实验进行段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到 E装置中的现象是
ⅳ.为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是
您最近一年使用:0次
解题方法
9 . 钠的化合物在生产、生活中有着重要的用途。
Ⅰ.某同学查阅资料得知 常作为汽车安全气囊中的冷却剂,为了探究其原理并比较
常作为汽车安全气囊中的冷却剂,为了探究其原理并比较 和
和 的热稳定性,设计了如下实验,回答下列问题:
的热稳定性,设计了如下实验,回答下列问题:

(1)整个实验过程中,烧杯B中的现象是_____________________ 。
(2)写出实验过程中套管内发生反应的化学方程式:__________________________ 。
(3)该实验可说明 的热稳定性
的热稳定性_________ (填“强于”、“弱于”或“等于”) ;上述实验装置中,能否将
;上述实验装置中,能否将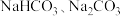 的位置互换?
的位置互换?________ (填“能”或“不能”)。
Ⅱ.在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。在实验室按如图所示装置,可进行实验模拟 的供氧作用,并收集产生的氧气。
的供氧作用,并收集产生的氧气。

(4)为了除去未反应完全的 ,B中应盛放
,B中应盛放_______ 溶液。
(5)U形管中 与
与 反应的化学方程式为
反应的化学方程式为__________________ 。
Ⅰ.某同学查阅资料得知
 常作为汽车安全气囊中的冷却剂,为了探究其原理并比较
常作为汽车安全气囊中的冷却剂,为了探究其原理并比较 和
和 的热稳定性,设计了如下实验,回答下列问题:
的热稳定性,设计了如下实验,回答下列问题:
(1)整个实验过程中,烧杯B中的现象是
(2)写出实验过程中套管内发生反应的化学方程式:
(3)该实验可说明
 的热稳定性
的热稳定性 ;上述实验装置中,能否将
;上述实验装置中,能否将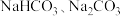 的位置互换?
的位置互换?Ⅱ.在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。在实验室按如图所示装置,可进行实验模拟
 的供氧作用,并收集产生的氧气。
的供氧作用,并收集产生的氧气。
(4)为了除去未反应完全的
 ,B中应盛放
,B中应盛放(5)U形管中
 与
与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
10 . 氯及其化合物既是重要化工原料,又是高效、广谱消毒剂。
(1)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:_______ 。
(2)实验室利用如图装置制备 和
和 。
。
已知: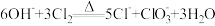

①盛放浓盐酸的仪器名称是_______ ,A中发生反应的离子方程式为_______ 。
②B中盛放的试剂是_______ ,作用是_______ ;C中试管内盛放的试剂为_______ 。
③E中盛放的试剂可选用_______ 。
A.稀盐酸 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
(1)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:
(2)实验室利用如图装置制备
 和
和 。
。已知:
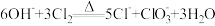

①盛放浓盐酸的仪器名称是
②B中盛放的试剂是
③E中盛放的试剂可选用
A.稀盐酸 B.
 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
您最近一年使用:0次



