1 . 某小组同学探究MnO 、MnO
、MnO 的性质。
的性质。
资料:i.MnO 的氧化能力与溶液的酸碱度有关,在酸性环境、中性环境、碱性环境能
的氧化能力与溶液的酸碱度有关,在酸性环境、中性环境、碱性环境能
被SO 分别还原为Mn2+(无色)、MnO2、MnO
分别还原为Mn2+(无色)、MnO2、MnO (绿色)。
(绿色)。
ii. MnO 在强碱溶液中能稳定存在,在酸性或纯水环境中易转化为MnO
在强碱溶液中能稳定存在,在酸性或纯水环境中易转化为MnO 和MnO2。
和MnO2。
I.验证MnO 与SO
与SO 的反应,实验如下:
的反应,实验如下:
(1)实验①参与反应的高锰酸钾和亚硫酸钠物质的量之比为_______ 。
(2)实验④中绿色很快消失,有大量棕色沉淀生成,结合离子方程式分析可能的原因_______ 。甲同学补做了实验_______ (填操作和现象),证明猜测合理。
II.验证 MnO 的性质。
的性质。
某同学用b试管得到的绿色溶液设计实验如下:
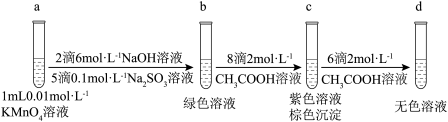
(3)c试管中得到紫色溶液和棕色浑浊的离子反应方程式为_______ 。继续滴加醋酸,沉淀溶解,得到无色透明溶液,有如下两种猜想:
① MnO 、MnO2可能被CH3COOH还原。
、MnO2可能被CH3COOH还原。
设计实验:将1mL 0.01mol·L−1 KMnO4溶液与少量MnO2固体混合,再向其中加入少许2mol·L−1 CH3COOH溶液,_______ (填现象),证明猜想不合理。
② MnO 、MnO2 可能被
、MnO2 可能被_______ 还原,发生的反应:_______ ,_______ 。
经实验验证,猜想合理。
由以上实验可知:MnO 、MnO2的性质不仅与溶液的酸碱度有关;还与试剂的用量等有关。
、MnO2的性质不仅与溶液的酸碱度有关;还与试剂的用量等有关。
 、MnO
、MnO 的性质。
的性质。资料:i.MnO
 的氧化能力与溶液的酸碱度有关,在酸性环境、中性环境、碱性环境能
的氧化能力与溶液的酸碱度有关,在酸性环境、中性环境、碱性环境能被SO
 分别还原为Mn2+(无色)、MnO2、MnO
分别还原为Mn2+(无色)、MnO2、MnO (绿色)。
(绿色)。ii. MnO
 在强碱溶液中能稳定存在,在酸性或纯水环境中易转化为MnO
在强碱溶液中能稳定存在,在酸性或纯水环境中易转化为MnO 和MnO2。
和MnO2。I.验证MnO
 与SO
与SO 的反应,实验如下:
的反应,实验如下:| 实验 | 序号 | 试剂X | 现象 |
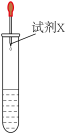 1mL0.01mol·L−1 KMnO4溶液 | ① | 2滴3mol·L−1 H2SO4 3滴0.1mol·L−1 Na2SO3 | 溶液褪为无色 |
| ② | 2滴纯水 3滴0.1mol·L−1 Na2SO3 | 产生棕色沉淀 | |
| ③ | 2滴6mol·L−1 NaOH 3滴0.1 mol·L−1 Na2SO3 | 溶液变为绿色 | |
| ④ | 2滴6mol·L−1 NaOH 10滴0.1mol·L−1 Na2SO3 | 溶液变为绿色溶液, 有浑浊,绿色很快消失,有大量棕色沉淀生成 |
(2)实验④中绿色很快消失,有大量棕色沉淀生成,结合离子方程式分析可能的原因
II.验证 MnO
 的性质。
的性质。某同学用b试管得到的绿色溶液设计实验如下:

(3)c试管中得到紫色溶液和棕色浑浊的离子反应方程式为
① MnO
 、MnO2可能被CH3COOH还原。
、MnO2可能被CH3COOH还原。设计实验:将1mL 0.01mol·L−1 KMnO4溶液与少量MnO2固体混合,再向其中加入少许2mol·L−1 CH3COOH溶液,
② MnO
 、MnO2 可能被
、MnO2 可能被经实验验证,猜想合理。
由以上实验可知:MnO
 、MnO2的性质不仅与溶液的酸碱度有关;还与试剂的用量等有关。
、MnO2的性质不仅与溶液的酸碱度有关;还与试剂的用量等有关。
您最近一年使用:0次
2 . 为探究FeCl3的性质,进行了如下实验(FeCl3和Na2SO3溶液浓度均为0.1mol·L−1)。
分析上述实验现象,所得结论不合理 的是
| 实验 | 操作与现象 |
| ① | 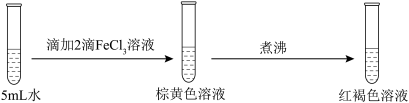 |
| ② | 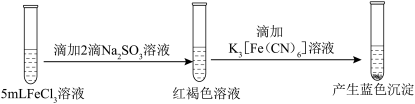 |
| ③ | 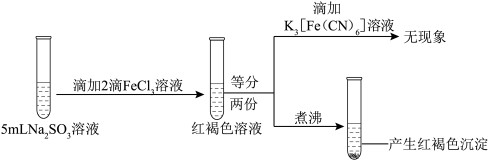 |
| A.实验①说明加热促进Fe3+水解反应 |
| B.实验②说明Fe3+ 既发生了水解反应,又发生了还原反应 |
| C.实验③说明Fe3+ 发生了水解反应,但没有发生还原反应 |
D.实验①-③说明SO 对Fe3+ 的水解反应无影响,但对还原反应有影响 对Fe3+ 的水解反应无影响,但对还原反应有影响 |
您最近一年使用:0次
2023-04-14更新
|
1097次组卷
|
7卷引用:北京市门头沟区2023届高三下学期一模考试化学试题
北京市门头沟区2023届高三下学期一模考试化学试题(已下线)专题14 化学实验方案的设计与评价(已下线)题型45 物质性质探究型综合实验北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题 山东省泰安肥城市2023-2024学年高三9月阶段测试化学试题北京市海淀区教师进修学校附属实验学校2023届高三三模化学试题(已下线)第3讲 物质制备实验的设计与评价



