1 . 钠的燃烧产物中混有黑色物质,研究小组进行如下图所示的实验探究。下列推测不正确的是
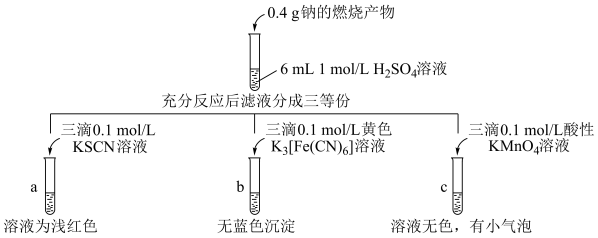
已知:K3[Fe(CN)6]能与Fe2+产生蓝色沉淀,是检验Fe2+的一种方法。

已知:K3[Fe(CN)6]能与Fe2+产生蓝色沉淀,是检验Fe2+的一种方法。
| A.过氧化钠与硫酸的反应可能有:Na2O2+2H+=2Na++H2O2 |
| B.a试管中的现象说明燃烧前钠块中含有铁元素 |
C.c试管的溶液为无色,推测发生的反应为:5H2O2+6H++2MnO =2Mn2++5O2↑+8H2O =2Mn2++5O2↑+8H2O |
| D.根据以上实验可判定:该实验中钠的燃烧产物里含Fe2O3,不含Fe3O4 |
您最近一年使用:0次
名校
解题方法
2 . 某小组同学探究FeSO4溶液与NaClO溶液的反应。
实验Ⅰ:向敞口容器中加入一定体积0.1mol·L-1FeSO4溶液,不断搅拌,逐滴加入pH≈13的84消毒液,溶液pH变化曲线如下图所示(从B点开始滴入84消毒液)。

B~C段,开始时产生红褐色沉淀,随后沉淀消失,溶液变为暗红色;
C点之后,逐渐产生大量黄色沉淀,有刺激性气味气体产生,溶液颜色明显变浅。
已知:25℃,饱和NaClO溶液的pH约为11,Fe3+完全沉淀时的pH≈13。
(1)Cl2通入NaOH溶液可得上述84消毒液,该84消毒液中阴离子主要有___________ 。
(2)A~B段,FeSO4溶液在搅拌下pH略有下降,用离子方程式解释原因___________ 。
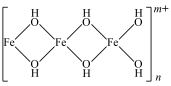
(3)B~C段,产生红褐色沉淀的离子方程式为___________ 。查阅资料可知,暗红色物质为聚合硫酸铁,是一种无机高分子化合物,其主要阳离子的结构为如下所示,该阳离子中Fe的配位数为___________ 。
(4)取少量C点溶液,加入___________ (补充试剂和现象),证明溶液中无Fe2+。C点之后产生的黄色沉淀经检验为铁黄(FeOOH),写出暗红色物质转化为黄色沉淀的离子方程式___________ 。
实验Ⅱ:向敞口容器中加入一定体积的pH≈13的84消毒液,不断搅拌,逐滴加入0.1mol·L-1FeSO4溶液,溶液pH变化曲线如下图所示。

E→H段,迅速产生大量红褐色沉淀且逐渐增多,H后开始产生有刺激性气味的气体,最终得到暗红色溶液和大量黄色沉淀。
已知:Cl2、HClO、ClO-在不同pH条件下的百分含量如下图:

(5)G→H段pH骤降的原因是___________ (用离子方程式表示)。
(6)综合以上实验,FeSO4溶液与NaClO溶液的反应产物与___________ 有关。
实验Ⅰ:向敞口容器中加入一定体积0.1mol·L-1FeSO4溶液,不断搅拌,逐滴加入pH≈13的84消毒液,溶液pH变化曲线如下图所示(从B点开始滴入84消毒液)。

B~C段,开始时产生红褐色沉淀,随后沉淀消失,溶液变为暗红色;
C点之后,逐渐产生大量黄色沉淀,有刺激性气味气体产生,溶液颜色明显变浅。
已知:25℃,饱和NaClO溶液的pH约为11,Fe3+完全沉淀时的pH≈13。
(1)Cl2通入NaOH溶液可得上述84消毒液,该84消毒液中阴离子主要有
(2)A~B段,FeSO4溶液在搅拌下pH略有下降,用离子方程式解释原因
(3)B~C段,产生红褐色沉淀的离子方程式为

(4)取少量C点溶液,加入
实验Ⅱ:向敞口容器中加入一定体积的pH≈13的84消毒液,不断搅拌,逐滴加入0.1mol·L-1FeSO4溶液,溶液pH变化曲线如下图所示。

E→H段,迅速产生大量红褐色沉淀且逐渐增多,H后开始产生有刺激性气味的气体,最终得到暗红色溶液和大量黄色沉淀。

已知:Cl2、HClO、ClO-在不同pH条件下的百分含量如下图:

(5)G→H段pH骤降的原因是
(6)综合以上实验,FeSO4溶液与NaClO溶液的反应产物与
您最近一年使用:0次
2023-11-06更新
|
219次组卷
|
3卷引用:北京市丰台区2023-2024学年高三上学期期中练习化学试题
3 . 某兴趣小组同学用图1所示装置,向一定体积的0.01mol/LBa(OH)2溶液中逐滴滴加0.2mol/LH2SO4溶液,不断搅拌并测定溶液导电能力的变化,实验测得混合溶液的导电能力随时间变化的曲线如图2所示。
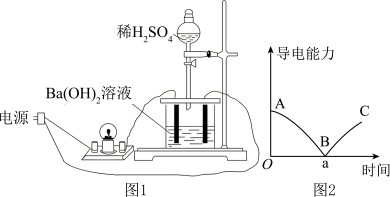
(1)用化学用语解释未滴加硫酸时,接通电源后灯泡变亮的原因:_______ ;
(2)实验过程中观察到的现象是:烧杯中_______ ,小灯泡_______ 。
(3)写出Ba(OH)2溶液与稀H2SO4反应的离子方程式_______ 。
(4)B点代表反应恰好完全,用Na2SO4溶液替代H2SO4溶液,重复上述实验进行对照,分析二者现象上的不同之处为_______ 。

(1)用化学用语解释未滴加硫酸时,接通电源后灯泡变亮的原因:
(2)实验过程中观察到的现象是:烧杯中
(3)写出Ba(OH)2溶液与稀H2SO4反应的离子方程式
(4)B点代表反应恰好完全,用Na2SO4溶液替代H2SO4溶液,重复上述实验进行对照,分析二者现象上的不同之处为
您最近一年使用:0次
4 . 小组利用如下装置探究氯气与水反应的产物。
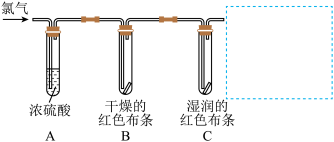
(1)浓硫酸的作用是_______ 。
(2)实验时,根据_______ 现象,甲同学得出初步结论:氯气与水反应生成的产物具有漂白性。
(3)Cl2与H2O反应的离子方程式为_______ 。
(4)乙同学们分析后,认为用该实验装置不能得出“HClO是漂白性物质”的结论,理由是_______ 。为了进一步证明该结论,应补充设计实验:_______ 。
(5)图中所示的实验设计还存在不足,请根据相关物质的性质,在图中的虚框内补充有关实验装置_______ ,并用离子方程式表示该原理_______ 。

(1)浓硫酸的作用是
(2)实验时,根据
(3)Cl2与H2O反应的离子方程式为
(4)乙同学们分析后,认为用该实验装置不能得出“HClO是漂白性物质”的结论,理由是
(5)图中所示的实验设计还存在不足,请根据相关物质的性质,在图中的虚框内补充有关实验装置
您最近一年使用:0次
5 . 某实验小组探究 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。
(1)取实验2后的溶液,进行如下实验:
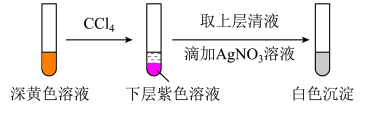
①根据______ 现象,判断实验2中有I2生成,因此反应后溶液显黄色。
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:_____ 。
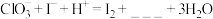
(2)查阅资料:一定条件下, 和I2都可以被氧化成
和I2都可以被氧化成 。
。
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是______ 。
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。
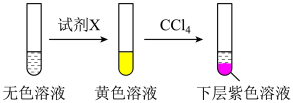
其中试剂X可以是______ (填字母)。
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 |
| 1 | 0.05mL | 浅黄色 |
2 | 0.02mL | 深黄色 | |
3 | 0.25mL | 浅黄色 | |
4 | 0.30mL | 无色 |

①根据
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:
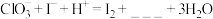
(2)查阅资料:一定条件下,
 和I2都可以被氧化成
和I2都可以被氧化成 。
。作出假设:NaClO3溶液用量增加导致溶液褪色的原因是
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。

其中试剂X可以是
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
您最近一年使用:0次
名校
6 . 碳酸亚铁(白色固体,难溶于水)可用于制备补血剂乳酸亚铁,也可用作可充电电池的电极。某研究小组设计实验制备 ,依次进行了实验I、II、III,方案如下:
,依次进行了实验I、II、III,方案如下:
资料:ⅰ.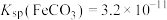 ,
,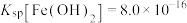
ⅱ. 吸附
吸附 后会呈现茶色
后会呈现茶色
ⅲ.
(1)实验I中的白色沉淀是______ 。
甲同学从理论上解释了该沉淀不是 的原因
的原因____________________________________ 。
(2)请结合化学用语解释 溶液呈碱性的原因
溶液呈碱性的原因________________________________ 。
(3)写出实验II中“产生白色沉淀及气泡”的离子方程式_____________________________ 。
(4)与实验I和II对比,实验Ⅲ使用 溶液的优点有
溶液的优点有________________________ 。
【实验反思】乙同学进一步确认实验I中红褐色沉淀的成分,进行了如下实验:
取沉淀溶于足量的硫酸,向其中通入 气体至饱和,溶液变为红棕色,放置12小时后溶液呈浅绿色。
气体至饱和,溶液变为红棕色,放置12小时后溶液呈浅绿色。
(5)请结合化学用语解释“先出现红棕色,12小时后变为浅绿色”的原因________________________ 。
 ,依次进行了实验I、II、III,方案如下:
,依次进行了实验I、II、III,方案如下:0.8 mol/L 溶液 溶液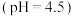
| 实验 | 试管内试剂 | 现象 |
Ⅰ | 1 mol/L  溶液 溶液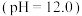 | 产生白色沉淀后很快变为灰绿色沉淀,5 min后出现明显的红褐色 | |
Ⅱ | 1 mol/L  溶液 溶液 | 产生白色沉淀后逐渐变茶色,有小气泡生成 | |
Ⅲ | 1 mol/L  溶液 溶液 | 产生白色沉淀及无色气泡,较长时间保持白色 |
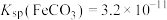 ,
,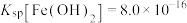
ⅱ.
 吸附
吸附 后会呈现茶色
后会呈现茶色ⅲ.

(1)实验I中的白色沉淀是
甲同学从理论上解释了该沉淀不是
 的原因
的原因(2)请结合化学用语解释
 溶液呈碱性的原因
溶液呈碱性的原因(3)写出实验II中“产生白色沉淀及气泡”的离子方程式
(4)与实验I和II对比,实验Ⅲ使用
 溶液的优点有
溶液的优点有【实验反思】乙同学进一步确认实验I中红褐色沉淀的成分,进行了如下实验:
取沉淀溶于足量的硫酸,向其中通入
 气体至饱和,溶液变为红棕色,放置12小时后溶液呈浅绿色。
气体至饱和,溶液变为红棕色,放置12小时后溶液呈浅绿色。(5)请结合化学用语解释“先出现红棕色,12小时后变为浅绿色”的原因
您最近一年使用:0次





