名校
解题方法
1 . 以海水为原料可获得钠、镁等金属及其化合物。
(1)将金属钠分别放入下列溶液中,既有气体产生,又有沉淀产生的是_____ (填序号,下同)
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④CuSO4溶液 ⑤饱和石灰水
溶液 ④CuSO4溶液 ⑤饱和石灰水
(2)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是_____。
与水的反应,下列说法正确的是_____。

(3)某膨松剂中发挥作用的物质为碳酸氢钠,学校兴趣小组为研究该膨松剂在加热情况下放出气体的量,设计了如图所示实验(装置A、C、D、E中的试剂足量)。
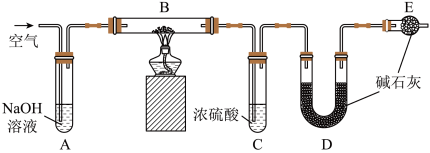
①加热前,需向装置内通入空气,用离子反应方程式解释装置A的作用_______ ,停止加热后,还需继续通入一段时间的空气,目的是_______ 。
②将一定质量的膨松剂样品装入装置B中,装置B中可能发生反应的化学反应方程式为___________ ;样品产生的二氧化碳的质量可通过测定实验前后装置_____ (填装置对应的标号)的质量测得。
③若没有装置E,可能会造成测定结果_______ (填“偏大”、“偏小”或“不变”)。
④实验测得二氧化碳的质量为13.2 g,则二氧化碳的体积(标准状况)为______ L,膨松剂样品中所含碳酸氢钠的物质的量为_____ mol。
(1)将金属钠分别放入下列溶液中,既有气体产生,又有沉淀产生的是
①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④CuSO4溶液 ⑤饱和石灰水
溶液 ④CuSO4溶液 ⑤饱和石灰水(2)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是_____。
与水的反应,下列说法正确的是_____。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
(3)某膨松剂中发挥作用的物质为碳酸氢钠,学校兴趣小组为研究该膨松剂在加热情况下放出气体的量,设计了如图所示实验(装置A、C、D、E中的试剂足量)。

①加热前,需向装置内通入空气,用离子反应方程式解释装置A的作用
②将一定质量的膨松剂样品装入装置B中,装置B中可能发生反应的化学反应方程式为
③若没有装置E,可能会造成测定结果
④实验测得二氧化碳的质量为13.2 g,则二氧化碳的体积(标准状况)为
您最近一年使用:0次
2 . 2021年在四川广汉三星堆新发现大量青铜器,如青铜面具、青铜神树等等。如图中的文物是三星堆出土的青铜面具之一,由于时间久远,表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、O2、CO2作用产生的,其化学式为Cu2(OH)2CO3,请用学过的方法对其展开探究。

(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有___________ 、___________ (选取其中两点)。
(2)从不同的物质分类标准的角度分析,“铜绿”不属于___________ 。
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐 F.碱
(3)从“铜绿”的组成、类别和性质的关联角度,预测它可能具有的化学性质,并用化学方程式加以表达(注:选写两个你认为可以实现的反应方程式,并且尽可能使得到的产物形态不同)
①___________ ,②___________ 。
(4)以“铜绿”为反应物可以实现以下物质转化:

反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式___________ 。

(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有
(2)从不同的物质分类标准的角度分析,“铜绿”不属于
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐 F.碱
(3)从“铜绿”的组成、类别和性质的关联角度,预测它可能具有的化学性质,并用化学方程式加以表达(注:选写两个你认为可以实现的反应方程式,并且尽可能使得到的产物形态不同)
①
(4)以“铜绿”为反应物可以实现以下物质转化:

反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式
您最近一年使用:0次
2023-11-02更新
|
343次组卷
|
3卷引用:江苏省江都区大桥中学2023-2024学年高一上学期期末复习模拟测试化学试题
名校
解题方法
3 . 下表列出了3种燃煤烟气脱硫方法的原理。
(1)如果不对燃煤烟气脱硫,易形成硫酸型酸雨,酸雨一般指的是pH小于___________ 的降雨。
(2)方法Ⅰ中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为: 、
、___________ 。
(3)能提高燃煤烟气中 去除率的措施有___________(只有一个选项符合题意,填字母)。
去除率的措施有___________(只有一个选项符合题意,填字母)。
(4)采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的 ,原因是
,原因是___________ (用离子方程式表示)。
(5)方法Ⅱ中CO将 还原为S时,自身转化为
还原为S时,自身转化为___________ (填化学式)。
(6)对方法Ⅲ 吸收 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的___________ 反应。
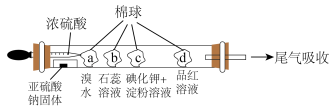
(7)下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将浓硫酸滴入装有亚硫酸钠固体的培养皿中。关于此实验的“现象”“解释或结论”以及对应关系均正确的是___________。
| 方法Ⅰ | 用氨水将 转化为 转化为 ,再氧化成 ,再氧化成 |
| 方法Ⅱ | 用生物质热解气(主要成分CO、 、 、 )将 )将 在高温下还原成单质硫 在高温下还原成单质硫 |
| 方法Ⅲ | 用 溶液吸收 溶液吸收 ,再经电解转化为 ,再经电解转化为 |
(2)方法Ⅰ中氨水吸收燃煤烟气中
 的化学反应为:
的化学反应为: 、
、(3)能提高燃煤烟气中
 去除率的措施有___________(只有一个选项符合题意,填字母)。
去除率的措施有___________(只有一个选项符合题意,填字母)。| A.增大氨水浓度 | B.升高反应温度 |
| C.使燃煤烟气快速通过氨水 | D.通入空气使 转化为 转化为 |
 ,原因是
,原因是(5)方法Ⅱ中CO将
 还原为S时,自身转化为
还原为S时,自身转化为(6)对方法Ⅲ 吸收
 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的(7)下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将浓硫酸滴入装有亚硫酸钠固体的培养皿中。关于此实验的“现象”“解释或结论”以及对应关系均正确的是___________。

| 选项 | 现象 | 解释或结论 |
| A | a处黄色褪去 | 非金属性:Br>S |
| B | b处变为红色 |  与水反应生成酸性物质 与水反应生成酸性物质 |
| C | c处变为蓝色 |  具有一定的氧化性 具有一定的氧化性 |
| D | d处红色先褪去后恢复 |  具有漂白性且漂白性不稳定 具有漂白性且漂白性不稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列有关物质的性质与用途具有对应关系的是
A. 能溶于水,可用于制备 能溶于水,可用于制备 | B. 受热易分解,可用来制造抗酸药物 受热易分解,可用来制造抗酸药物 |
C.浓硫酸具有脱水性,可用于干燥 | D.铁粉能与 反应,可用作食品保存的脱氧剂 反应,可用作食品保存的脱氧剂 |
您最近一年使用:0次
解题方法
5 . 浓盐酸和高锰酸钾在室温下即可制备氯气,用如图装置制备少量的氯气并探究其性质。下列实验装置和操作能达到实验目的的是
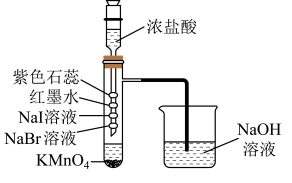

| A.根据溴化钠和碘化钠中的现象可证明氧化性:Br2<I2 |
| B.红墨水褪色,说明氯水具有漂白性 |
| C.紫色石蕊试液先变红后褪色,说明氯气具有酸性和强氧化性 |
| D.可用饱和食盐水代替NaOH溶液吸收多余的氯气 |
您最近一年使用:0次
名校
解题方法
6 . 金属镓有“电子工业脊梁”的美誉,镓与铝的化学性质类似。从刚玉渣(含钛、镓的低硅铁合金,还含有少量氧化铝)回收镓的流程如图所示:
请回答下列问题。
(1)“酸浸”过程中禁止明火加热,原因是___________ 。
(2)“结晶”过程中得到 的具体操作为
的具体操作为___________ 。
(3)“中和沉淀”过程中pH应调节的范围为___________ 。
(4)“碳酸化”过程中不能通入过量 的原因为
的原因为___________ (用离子方程式表示)。
(5)下列说法中不正确的是___________(填字母)。
(6)GaN具有优异的光电性能。工业上常采用在1100℃条件下,利用Ga与 反应可制备GaN,该过程的化学方程式为
反应可制备GaN,该过程的化学方程式为___________ 。

| 金属离子 |  |  |  |  |
开始沉淀时 的pH 的pH | 4.5 | 3.7 | 2.2 | 7.5 |
沉淀完全时 的pH 的pH | 5.5 | 4.7 | 3.2 | 9.0 |
(1)“酸浸”过程中禁止明火加热,原因是
(2)“结晶”过程中得到
 的具体操作为
的具体操作为(3)“中和沉淀”过程中pH应调节的范围为
(4)“碳酸化”过程中不能通入过量
 的原因为
的原因为(5)下列说法中不正确的是___________(填字母)。
| A.为提高浸出率,可将刚玉渣研磨 |
B.“结晶”过程中得到的 可作为净水剂 可作为净水剂 |
C.由流程图可知酸性: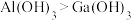 |
| D.“碱浸”过程中可用氨水代替NaOH溶液 |
 反应可制备GaN,该过程的化学方程式为
反应可制备GaN,该过程的化学方程式为
您最近一年使用:0次
2023-07-10更新
|
313次组卷
|
3卷引用:江苏省淮阴中学2022-2023学年高一下学期6月阶段测试化学试题
江苏省淮阴中学2022-2023学年高一下学期6月阶段测试化学试题江苏省昆山中学2022-2023学年高一下学期6月阶段测试化学试题(已下线)综合期末压轴85+18题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
7 . 下列依据实验现象推理得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 某盐和 混合研磨,产生 混合研磨,产生 | 该盐是 |
| B | 某待测液中加入 溶液,产生白色沉淀 溶液,产生白色沉淀 | 待测液含有 |
| C | 铜片与浓硫酸加热,产生的气体通入品红溶液,品红褪色 | 生成 气体 气体 |
| D | 常温时向盛有浓硝酸的两支试管中分别投入铜片与铁片后,铜片逐渐溶解而铁片不溶解 | 金属性:Cu>Fe |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 常温下 与
与 反应能生成
反应能生成 和
和 。实验室探究
。实验室探究 与
与 反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
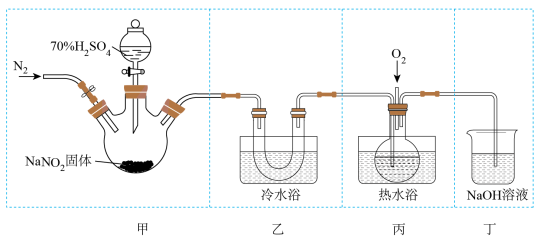
 与
与 反应能生成
反应能生成 和
和 。实验室探究
。实验室探究 与
与 反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
| A.用装置甲制取气体 | B.用装置乙收集生成的 |
C.用装置丙检验 生成 生成 | D.蒸发丁中所得溶液得到纯净 晶体 晶体 |
您最近一年使用:0次
名校
解题方法
9 . 利用Zn和 溶液反应模拟地下水的脱硝过程,并探究脱硝原理及相关因素对脱硝速率的影响。模拟过程的实验装置如图所示。
溶液反应模拟地下水的脱硝过程,并探究脱硝原理及相关因素对脱硝速率的影响。模拟过程的实验装置如图所示。 洗涤Zn粒,再用蒸馏水洗涤至接近中性;将
洗涤Zn粒,再用蒸馏水洗涤至接近中性;将 溶液的pH调至2.5。
溶液的pH调至2.5。
①用稀 洗涤Zn粒的目的是
洗涤Zn粒的目的是__________ 。
②向上述 溶液中加入足量洗涤后的Zn粒,写出Zn与
溶液中加入足量洗涤后的Zn粒,写出Zn与 溶液反应生成
溶液反应生成 的离子方程式
的离子方程式__________ 。
③锥形瓶中NaOH溶液的作用是__________ 。
(2)某兴趣小组进行了如下实验:取两套如图所示装置,分别加入等体积、等浓度的 溶液;将溶液的pH值调节为2.5,并通入氮气;将其中一套实验装置浸入热水浴中(或浸入冰水浴中);向三颈瓶中分别加入足量且等质量的同种Zn粒,用离子色谱仪测定相同反应时间时三颈瓶中
溶液;将溶液的pH值调节为2.5,并通入氮气;将其中一套实验装置浸入热水浴中(或浸入冰水浴中);向三颈瓶中分别加入足量且等质量的同种Zn粒,用离子色谱仪测定相同反应时间时三颈瓶中 的浓度。(已知:溶液中的
的浓度。(已知:溶液中的 的物质的量浓度可用离子色谱仪测定)
的物质的量浓度可用离子色谱仪测定)
①该实验的目的是探究__________ 对脱氮速率的影响。
②该实验过程中采用了科学探究中一种重要的思想方法是__________ 。
(3)反应过程中有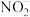 生成。为测定反应液中
生成。为测定反应液中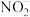 的含量,取过滤后的滤液100mL,用
的含量,取过滤后的滤液100mL,用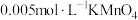 酸性溶液滴定,消耗
酸性溶液滴定,消耗 溶液的体积为16.00mL。(在此条件下
溶液的体积为16.00mL。(在此条件下 不与
不与 酸性溶液反应)。计算过滤后的滤液中
酸性溶液反应)。计算过滤后的滤液中 的物质量浓度
的物质量浓度__________ 。
 溶液反应模拟地下水的脱硝过程,并探究脱硝原理及相关因素对脱硝速率的影响。模拟过程的实验装置如图所示。
溶液反应模拟地下水的脱硝过程,并探究脱硝原理及相关因素对脱硝速率的影响。模拟过程的实验装置如图所示。
 洗涤Zn粒,再用蒸馏水洗涤至接近中性;将
洗涤Zn粒,再用蒸馏水洗涤至接近中性;将 溶液的pH调至2.5。
溶液的pH调至2.5。①用稀
 洗涤Zn粒的目的是
洗涤Zn粒的目的是②向上述
 溶液中加入足量洗涤后的Zn粒,写出Zn与
溶液中加入足量洗涤后的Zn粒,写出Zn与 溶液反应生成
溶液反应生成 的离子方程式
的离子方程式③锥形瓶中NaOH溶液的作用是
(2)某兴趣小组进行了如下实验:取两套如图所示装置,分别加入等体积、等浓度的
 溶液;将溶液的pH值调节为2.5,并通入氮气;将其中一套实验装置浸入热水浴中(或浸入冰水浴中);向三颈瓶中分别加入足量且等质量的同种Zn粒,用离子色谱仪测定相同反应时间时三颈瓶中
溶液;将溶液的pH值调节为2.5,并通入氮气;将其中一套实验装置浸入热水浴中(或浸入冰水浴中);向三颈瓶中分别加入足量且等质量的同种Zn粒,用离子色谱仪测定相同反应时间时三颈瓶中 的浓度。(已知:溶液中的
的浓度。(已知:溶液中的 的物质的量浓度可用离子色谱仪测定)
的物质的量浓度可用离子色谱仪测定)①该实验的目的是探究
②该实验过程中采用了科学探究中一种重要的思想方法是
(3)反应过程中有
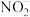 生成。为测定反应液中
生成。为测定反应液中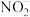 的含量,取过滤后的滤液100mL,用
的含量,取过滤后的滤液100mL,用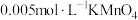 酸性溶液滴定,消耗
酸性溶液滴定,消耗 溶液的体积为16.00mL。(在此条件下
溶液的体积为16.00mL。(在此条件下 不与
不与 酸性溶液反应)。计算过滤后的滤液中
酸性溶液反应)。计算过滤后的滤液中 的物质量浓度
的物质量浓度
您最近一年使用:0次
2023-06-20更新
|
114次组卷
|
2卷引用:江苏省常州市第一中学2022-2023学年高一下学期期末测试化学试题
解题方法
10 . 为探究 的性质,采用下列实验装置制少量
的性质,采用下列实验装置制少量 并进行相应的实验探究:
并进行相应的实验探究:
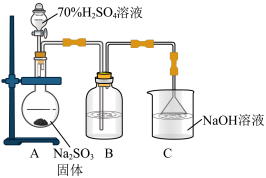
(1)装置A中盛放浓硫酸的仪器名称是___________ 。
(2)若B中的试剂是品红溶液,B中溶液红色褪去, 表现的性质
表现的性质___________ 。
(3)若B中的试剂是酸性 溶液,则B中的现象是
溶液,则B中的现象是___________ ,写出反应的离子方程式( 被还原为
被还原为 )
)___________ 。
(4)装置C中倒置漏斗的作用是___________ ,反应的离子方程式为___________ 。
(5)已知: 可还原某含碲物质(主要成分为
可还原某含碲物质(主要成分为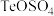 )溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量
)溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量 ,加热到一定温度,持续通入
,加热到一定温度,持续通入 ,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
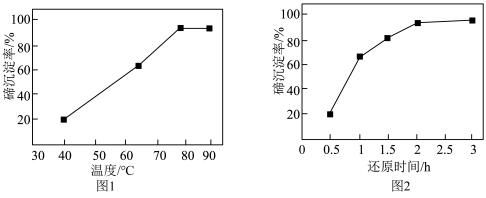
①由图可知,最适宜的温度和还原时间分别为___________ 。
②图1中80℃后,升高温度,碲沉淀率几乎不再升高,甚至有下降趋势。可能的原因是________ 。
 的性质,采用下列实验装置制少量
的性质,采用下列实验装置制少量 并进行相应的实验探究:
并进行相应的实验探究:
(1)装置A中盛放浓硫酸的仪器名称是
(2)若B中的试剂是品红溶液,B中溶液红色褪去,
 表现的性质
表现的性质(3)若B中的试剂是酸性
 溶液,则B中的现象是
溶液,则B中的现象是 被还原为
被还原为 )
)(4)装置C中倒置漏斗的作用是
(5)已知:
 可还原某含碲物质(主要成分为
可还原某含碲物质(主要成分为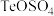 )溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量
)溶液可得到粗碲。具体实验操作为:取该溶液于烧瓶中,加入适量 ,加热到一定温度,持续通入
,加热到一定温度,持续通入 ,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
,待反应一定时间,过滤得到粗碲。在一定条件下,碲沉淀率与温度、还原时间的变化曲线分别如图1、图2所示:
①由图可知,最适宜的温度和还原时间分别为
②图1中80℃后,升高温度,碲沉淀率几乎不再升高,甚至有下降趋势。可能的原因是
您最近一年使用:0次



