1 . 一氧化二氯(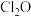 )是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。制备出的
)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。制备出的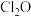 要冷却成固体才便于操作和保存,制取少量的
要冷却成固体才便于操作和保存,制取少量的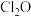 是用干燥的氧化汞和氯气反应:
是用干燥的氧化汞和氯气反应: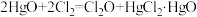 (反应放热)。某化学兴趣小组设计如图装置以制备
(反应放热)。某化学兴趣小组设计如图装置以制备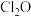 (支撑、加热及夹持装置已省略)。
(支撑、加热及夹持装置已省略)。

已知:①a中固体试剂是 ,b中试剂是浓盐酸。
,b中试剂是浓盐酸。
②有关物质的熔沸点如下表。
请回答:
(1)仪器b的名称_______ ,B中盛有的液体c应是_______ 。
(2)写出装置A中制备氯气的离子方程式_______ 。
(3)待装置A不再产生氯气后,M处通入干燥空气的作用是_______ 。
(4)装置中D的水浴温度应控制在18℃~20℃原因之一是:温度过底反应太慢不利于制备,另一个原因是:_______ 。
(5)E中的保温瓶中盛有液态制冷剂e是_______ (在“干冰”“冰水”“液态空气”“液氨”“液氯”中选择一种)
(6)据文献报道,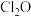 的另一种制备方法是利用
的另一种制备方法是利用 与潮湿的
与潮湿的 反应来制得,同时生成
反应来制得,同时生成 和NaCl两种盐,写出该反应的化学方程式
和NaCl两种盐,写出该反应的化学方程式_______ 。
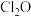 )是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。制备出的
)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。制备出的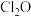 要冷却成固体才便于操作和保存,制取少量的
要冷却成固体才便于操作和保存,制取少量的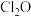 是用干燥的氧化汞和氯气反应:
是用干燥的氧化汞和氯气反应: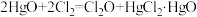 (反应放热)。某化学兴趣小组设计如图装置以制备
(反应放热)。某化学兴趣小组设计如图装置以制备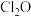 (支撑、加热及夹持装置已省略)。
(支撑、加热及夹持装置已省略)。
已知:①a中固体试剂是
 ,b中试剂是浓盐酸。
,b中试剂是浓盐酸。②有关物质的熔沸点如下表。
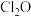 |  |  |  |  |  | |
| 熔点 | -120.6℃ | -209.86C | -218.4℃ | -78.5℃(升华) | -77.3C | -101℃ |
| 沸点 | 3.8℃ | -195.8℃ | -183℃ | -33.35℃ | -34.6℃ |
(1)仪器b的名称
(2)写出装置A中制备氯气的离子方程式
(3)待装置A不再产生氯气后,M处通入干燥空气的作用是
(4)装置中D的水浴温度应控制在18℃~20℃原因之一是:温度过底反应太慢不利于制备,另一个原因是:
(5)E中的保温瓶中盛有液态制冷剂e是
(6)据文献报道,
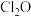 的另一种制备方法是利用
的另一种制备方法是利用 与潮湿的
与潮湿的 反应来制得,同时生成
反应来制得,同时生成 和NaCl两种盐,写出该反应的化学方程式
和NaCl两种盐,写出该反应的化学方程式
您最近一年使用:0次
2 . 次氯酸(HClO)消毒液高效安全,适用于一般物体表面消毒、手部消毒,以及地面、空间和环境消毒。下图装置在D中制得颜色类似于氯气的Cl2O气体,E中得到次氯酸(HClO)。已知Cl2O气体45℃可分解,与水反应生成HClO。
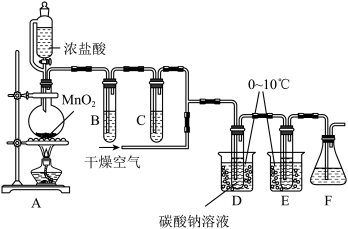
(1)装置A中使用该漏斗的目的是_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)C装置、F装置中分别盛装_______ 、_______ 。
(4)D中盛装碳酸钠溶液用来吸收氯气制备Cl2O。D中生成的气体中含有CO2,则生成Cl2O的化学方程式为_______ 。
(5)实验时,一直要通入干燥的空气,主要作用是_______ ,同时还可以抑制Cl2O的分解,保证实验安全。
(6)为了探究反应条件对产物的影响,另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O
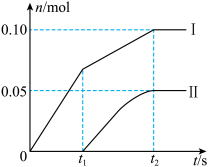
①图中曲线I表示_______ 离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为_______ mol,参加反应的氯气的体积为_______ (标况下)
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37 mol,则产物中 =
=_______ 。

(1)装置A中使用该漏斗的目的是
(2)装置A中发生反应的离子方程式为
(3)C装置、F装置中分别盛装
(4)D中盛装碳酸钠溶液用来吸收氯气制备Cl2O。D中生成的气体中含有CO2,则生成Cl2O的化学方程式为
(5)实验时,一直要通入干燥的空气,主要作用是
(6)为了探究反应条件对产物的影响,另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO
 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O
①图中曲线I表示
②所取石灰乳中含有Ca(OH)2的物质的量为
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37 mol,则产物中
 =
=
您最近一年使用:0次
20-21高一·浙江·阶段练习
解题方法
3 . 工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。
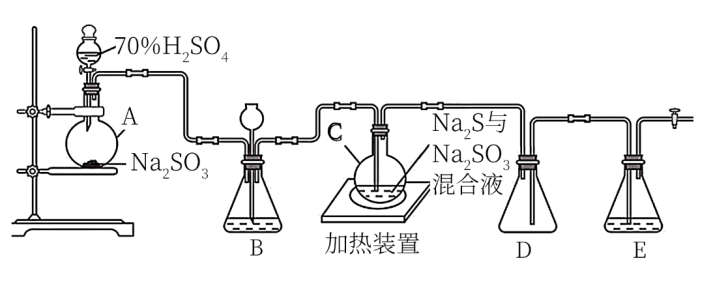
烧瓶C中发生反应如下:
Na2S (aq)+H2O (1) +SO2 (g)=Na2SO3 (aq)+H2S (aq) (I)
2H2S (aq) +SO2 (g) =3S (s) +2H2O (l) (II)
S(s)+Na2SO3 (aq) Na2S2O3 (aq) (III)
Na2S2O3 (aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若_______ ,则整个装置气密性良好。
(2)装置D的作用是_______ ,装置E的作用是_______ 。
(3)装置A中反应的化学方程式为_______ 。
(4)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为_______ 。
(5)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择_______ 。
a.蒸馏水 b.饱和Na2SO3溶液
c. 饱和NaHSO3溶液 d. 饱和NaHCO3溶液
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4 等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:_______ 。供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液

烧瓶C中发生反应如下:
Na2S (aq)+H2O (1) +SO2 (g)=Na2SO3 (aq)+H2S (aq) (I)
2H2S (aq) +SO2 (g) =3S (s) +2H2O (l) (II)
S(s)+Na2SO3 (aq)
 Na2S2O3 (aq) (III)
Na2S2O3 (aq) (III)(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若
(2)装置D的作用是
(3)装置A中反应的化学方程式为
(4)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为
(5)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择
a.蒸馏水 b.饱和Na2SO3溶液
c. 饱和NaHSO3溶液 d. 饱和NaHCO3溶液
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4 等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:
您最近一年使用:0次
名校
解题方法
4 . 一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。某化学兴趣小组设计如图装置以制备Cl2O(支撑及夹持装置已省略)。
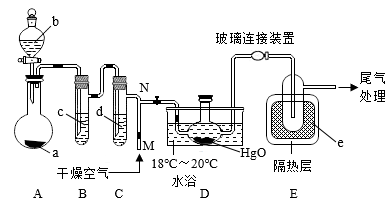
已知:①a中固体试剂是MnO2,b中试剂是浓盐酸。
②Cl2O的部分性质如表:
请回答:
(1)指出该制备装置中存在的一个明显错误_____ (经改进后进行有关实验)。
(2)装置C中盛有的试剂是_____ 。
(3)写出装置A中制备Cl2的化学方程式_____ 。
(4)装置D中采用18℃~20℃水浴的原因之一是:如温度过低,反应速率慢,另一个可能的原因是_____ 。
(5)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,装置D、E间采用这种连接方式的理由是_____ 。
(6)Cl2O是市场上一种比较理想的饮用水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2的消毒效率(以单位质量得到的电子数表示)是等质量的Cl2O的_____ 倍(结果保留一位小数)
(7)据文献报道,Cl2O的另一种制备方法是利用Cl2与适量潮湿的Na2CO3反应来制得,同时产生一种无色气体(该气体含两种元素),写出该反应的化学方程式______ 。

已知:①a中固体试剂是MnO2,b中试剂是浓盐酸。
②Cl2O的部分性质如表:
| 熔点 | 沸点 | 制备方法 |
| 120.6℃ | 3.8℃ | 2HgO+2Cl2=Cl2O+HgCl2·HgO(反应放热) |
(1)指出该制备装置中存在的一个明显错误
(2)装置C中盛有的试剂是
(3)写出装置A中制备Cl2的化学方程式
(4)装置D中采用18℃~20℃水浴的原因之一是:如温度过低,反应速率慢,另一个可能的原因是
(5)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,装置D、E间采用这种连接方式的理由是
(6)Cl2O是市场上一种比较理想的饮用水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2的消毒效率(以单位质量得到的电子数表示)是等质量的Cl2O的
(7)据文献报道,Cl2O的另一种制备方法是利用Cl2与适量潮湿的Na2CO3反应来制得,同时产生一种无色气体(该气体含两种元素),写出该反应的化学方程式
您最近一年使用:0次
5 . 已知CuCl易被氧化。工业上,以硫化铜精矿为原料,制备氯化亚铜的流程如下:下列说法不正确的是( )


| A.步骤①,焙烧时可能会产生有毒气体,要注意尾气吸收 |
| B.步骤②,浸出液显蓝色 |
| C.步骤③,主要反应为2CuSO4+2NaCl+Na2SO3+H2O=2CuCl↓+Na2SO4+H2SO4 |
| D.步骤④,操作步骤为:过滤、洗涤(用盐酸、乙醇)、干燥(空气中) |
您最近一年使用:0次
6 . 某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。
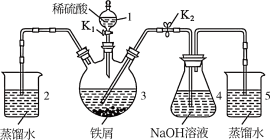
请回答:
(1) 仪器1的名称________ 。装置5的作用________ 。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________ 。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________ 。

请回答:
(1) 仪器1的名称
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因
您最近一年使用:0次
2019-04-12更新
|
5824次组卷
|
19卷引用:浙江省瑞安市上海新纪元高级中学2019-2020学年高一(7-10)班下学期期初考试化学试题
浙江省瑞安市上海新纪元高级中学2019-2020学年高一(7-10)班下学期期初考试化学试题2019年4月浙江省普通高校招生选考科目考试化学试题浙江省宁波市北仑中学2019-2020学年高二6月月考化学试题人教版(2019)高一必修第一册第三章 铁 金属材料 高考挑战区人教版(2019)高一必修第一册 第三章素养检测高一必修第一册(鲁科2019)第3章 第1节 铁的多样性专题9 第一~三单元综合拔高练-高中化学必修第二册苏教版2019(已下线)新人教必修1第3章第一节第2课时铁的氧化物和氢氧化物(课后)(已下线)专题17.基础实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)第5章 金属及其化合物(章末复习)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)2019年高考浙江卷化学试题变式题(实验题)2020届高考化学二轮复习大题精准训练——以“气体”为纽带的化学综合实验专题3.1 金属及其化合物(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(苏教版2019)必修第二册专题9 金属与人类文明 C 高考挑战区(已下线)微专题14 氢氧化亚铁、高铁酸盐的制备实验探究-备战2023年高考化学一轮复习考点微专题(已下线)题型28 氢氧化亚铁的制备实验探究(已下线)第2讲 铁、铁的氧化物、铁的氢氧化物(已下线)考点10 铁及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
7 . 下图为某化工企业生产流程示意图,下列说法正确的是
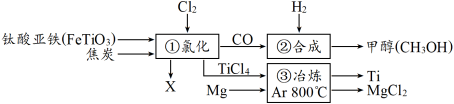

| A.钛酸亚铁(FeTiO3)中钛元素为+3价 |
| B.①中反应为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为FeCl3 |
| C.③中氩气(Ar)作反应物,反应类型为置换反应 |
| D.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 |
您最近一年使用:0次
2018-09-02更新
|
767次组卷
|
4卷引用:2022年高一新东方开学考化学试卷
名校
8 . 下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、6 mol/L硫酸溶液、NaOH溶液。下列说法错误的是( )
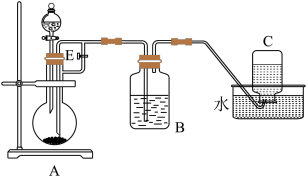
| A.B中盛有一定量的NaOH溶液,A中应预先加入的试剂是铁屑 |
| B.实验开始时应先将活塞E关闭 |
| C.生成Fe(OH)2的操作为:关闭E,使A中溶液压入B瓶中 |
| D.取下装置B中的橡皮塞,使空气进入,有关反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
您最近一年使用:0次
2016-12-09更新
|
1854次组卷
|
16卷引用:浙江省绍兴市2021-2022学年高一上学期期末调测化学试题
浙江省绍兴市2021-2022学年高一上学期期末调测化学试题2015-2016学年重庆市第一中学高一上学期期末化学试卷2016-2017学年河北省石家庄市第一中学高一上学期期末考试化学试卷河北省阜城中学2017-2018学年高一上学期第四次月考化学试题新疆乌鲁木齐市第四中学2021-2022学年高一上学期期末考试化学试题(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)湖南省长沙市实验中学2022-2023学年高一上学期期末考试化学试题四川省绵阳市南山中学2022-2023学年高一上学期12月线上测试化学试题天津市新华中学2023-2024学年高一上学期第二次月考化学试卷广东省广州天省实验学校2022-2023学年高一上学期期末考试化学试卷四川省雅安市天立学校2023-2024学年高一上学期第三次教学质量检测化学试题(已下线)第5单元 常见的金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)黑龙江省哈尔滨市第六中学2021-2022学年高三上学期期中考试化学试题(已下线)【教材实验热点】04 Fe(OH)2与Fe(OH)3胶体的制备(已下线)考点10 铁及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
解题方法
9 . 下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验时必须使用铁屑、6 mol/L硫酸溶液,其他试剂任选。填写下列空白:
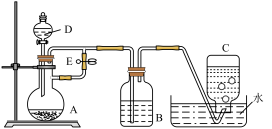
(1)B中盛有一定量的NaOH溶液,D仪器的名称________ ,A中反应的离子方程式为________ 。
(2)实验开始时应先将活塞E_____ (填“打开”或“关闭”), 在C中收到的气体主要为_______ ;当C瓶或A瓶中的气泡_________ 时,将活塞E_____ (填“打开”或“关闭”),此刻B瓶中可能发生的化学反应(用离子方程式表示,有几个写几个)是:_________________________ ;
(3)拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式:____________ 。

(1)B中盛有一定量的NaOH溶液,D仪器的名称
(2)实验开始时应先将活塞E
(3)拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式:
您最近一年使用:0次
11-12高一上·浙江台州·期中
10 . 氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用到氯气。工业上通常采用电解法制氯气:观察下图,回答:

Ⅰ(1)若饱和食盐水中含有酚酞,通电后_____ (填a或b)侧先变红。
(2)电解反应的化学方程式为__________________
Ⅱ某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为________________________________________ ,若在标准状态下收集到22.4升的氯气,则被氧化的HCl的物质的量是_____________ 。
(2)漂白粉将在U形管中产生,其化学方程式是_________________________________ 。
(3) C装置的作用是____________________ 。
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是______________________________________ 。
②试判断另一个副反应(用化学方程式表示)_____________________________________ 。为避免此副反应的发生,可将装置作何改进____________________________________ 。
(5)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是_____________ 。

Ⅰ(1)若饱和食盐水中含有酚酞,通电后
(2)电解反应的化学方程式为
Ⅱ某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为
(2)漂白粉将在U形管中产生,其化学方程式是
(3) C装置的作用是
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应(用化学方程式表示)
(5)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是
| A.食盐 | B.食醋 | C.烧碱 | D.纯碱 |
您最近一年使用:0次



