名校
解题方法
1 . 海洋资源的利用具有广阔前景。
(1)从海水制得的粗盐含有Ca2+、Mg2+、 等杂质离子,正确的除杂操作顺序为___________
等杂质离子,正确的除杂操作顺序为___________
①加入稍过量的BaCl2溶液;②加入稍过量的Na2CO3溶液;③加入适量的稀盐酸;④加入稍过量的NaOH溶液;⑤过滤。
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入Cl2,将Br-氧化,该反应的离子方程式是______ 。
(3)下图是从海水中提取镁的简单流程。
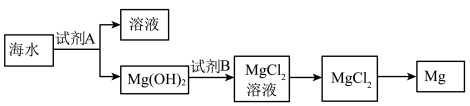
①工业上常用于沉淀Mg2+ 的试剂A是___________ 。
②由无水MgCl2制取Mg的化学方程式是___________ 。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
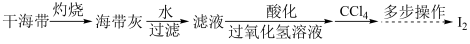
①灼烧海带时所用的主要仪器名称是___________ 。
②向酸化的滤液中加H2O2溶液,写出该反应的离子方程式:___________ 。
(1)从海水制得的粗盐含有Ca2+、Mg2+、
 等杂质离子,正确的除杂操作顺序为___________
等杂质离子,正确的除杂操作顺序为___________①加入稍过量的BaCl2溶液;②加入稍过量的Na2CO3溶液;③加入适量的稀盐酸;④加入稍过量的NaOH溶液;⑤过滤。
| A.④①②③⑤ | B.②①④⑤③ | C.①②⑤③④ | D.①④②⑤③ |
(3)下图是从海水中提取镁的简单流程。

①工业上常用于沉淀Mg2+ 的试剂A是
②由无水MgCl2制取Mg的化学方程式是
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
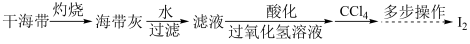
①灼烧海带时所用的主要仪器名称是
②向酸化的滤液中加H2O2溶液,写出该反应的离子方程式:
您最近一年使用:0次
名校
2 . 海带提碘过程中以 为溶剂将
为溶剂将 从碘水溶液中提取出来,通过下列实验可从
从碘水溶液中提取出来,通过下列实验可从 的
的 溶液中回收
溶液中回收 。
。

下列说法错误的是
 为溶剂将
为溶剂将 从碘水溶液中提取出来,通过下列实验可从
从碘水溶液中提取出来,通过下列实验可从 的
的 溶液中回收
溶液中回收 。
。
下列说法错误的是
| A.反应1的目的为将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中 |
| B.操作1需要用到的玻璃仪器有普通漏斗、烧杯和玻璃棒 |
C.反应2的离子方程式为 |
| D.操作2的名称为过滤 |
您最近一年使用:0次
2023-08-21更新
|
215次组卷
|
2卷引用:江西省宜春市丰城拖船中学2023-2024学年高二上学期开学化学试题
名校
3 . 实验室模拟工业海带提砷的流程如图。下列说法错误的是
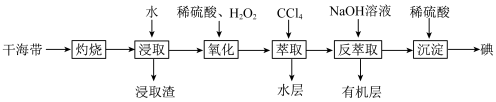
| A.“灼烧”用到的硅酸盐仪器有坩埚、泥三角、玻璃棒、酒精灯 |
B.“氧化”时发生反应的离子方程式为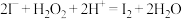 |
| C.“反萃取”所得有机层经处理后可循环再利用 |
D.“沉淀”时每生成 碘,理论上转移 碘,理论上转移 电子 电子 |
您最近一年使用:0次
2023-08-03更新
|
309次组卷
|
3卷引用:江西省抚州市黎川县第二中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
4 . 海藻中食含碘元素。某小组同学在实验室里用灼烧海藻的灰分提取碘,流程如下图所示:
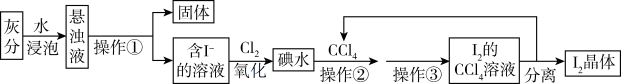
(1)操作①的名称_____ ,操作③的名称_____ 。实验室进行操作①使用的仪器有铁架台(带铁圈)、漏斗和_____ 。
(2)操作②选用CCl4的理由是_____(填写序号)。
(3)用NaOH溶液反萃取后再加稀硫酸,可以分离I2和CCl4。有关化学方程式为:
碱性条件: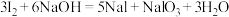 ;
;
酸性条件: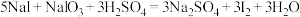 。
。
以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的_____ (填仪器名称)中加入少量1mol/LNaOH溶液;
②振荡至溶液的_____ 色消失,静置,分层,则_____ (填“上”。“下”)层为CCl4;
③将含碘的碱溶液从仪器的_____ (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴1mol⋅L-1H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体。
(4)本实验中可以循环利用的物质是_____ 。

(1)操作①的名称
(2)操作②选用CCl4的理由是_____(填写序号)。
| A.CCl4不溶于水 | B.CCl4的密度比水大 |
| C.碘在CCl4中比在水中溶解度更大 | D.CCl4与碘水不反应 |
碱性条件:
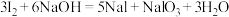 ;
;酸性条件:
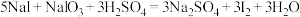 。
。以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的
②振荡至溶液的
③将含碘的碱溶液从仪器的
④边搅拌边加入几滴1mol⋅L-1H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体。
(4)本实验中可以循环利用的物质是
您最近一年使用:0次
2023-07-19更新
|
124次组卷
|
2卷引用:江西省抚州市黎川县第二中学2023-2024学年高二上学期开学考试化学试题
名校
5 . 海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
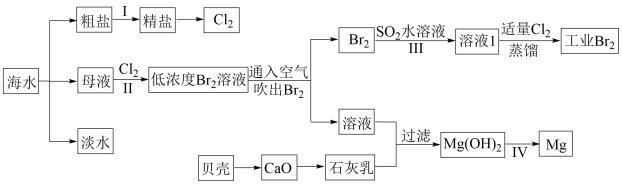
回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:___________________ 。
(2)步骤I中,粗盐中含有Ca2+、Mg2+、SO 等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
(3)步骤II已经获得Br2,步骤III又将Br2还原为Br-,其目的是___________________ 。
(4)写出步骤III反应的离子方程式:______________________ 。工业上也可用Na2CO3溶液代替二氧化硫水溶液吸收Br2,完成下列化学方程式:__________ 。________Br2+ _______Na2CO3 ________NaBrO3+ ________CO2+ ____________
________NaBrO3+ ________CO2+ ____________
(5)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:
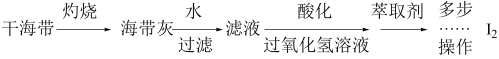
向酸化的滤液中加入过氧化氢溶液,可将I-氧化为I2,请写出该反应的离子方程式:_______________ 。

回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:
(2)步骤I中,粗盐中含有Ca2+、Mg2+、SO
 等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。| A.①②③④ | B.②③④① | C.②④③① | D.③④②① |
(4)写出步骤III反应的离子方程式:
 ________NaBrO3+ ________CO2+ ____________
________NaBrO3+ ________CO2+ ____________(5)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:
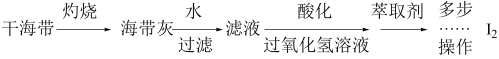
向酸化的滤液中加入过氧化氢溶液,可将I-氧化为I2,请写出该反应的离子方程式:
您最近一年使用:0次
2023-04-24更新
|
319次组卷
|
2卷引用:江西省新余市第一中学2023-2024学年高二上学期开学考试化学试题
解题方法
6 . 海带中含有的碘元素可经过灼烧→浸取→过滤→氧化→萃取→蒸馏步骤完成,各步骤中选用的实验用品正确的是
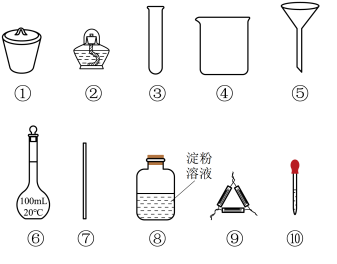

| A.将海带灼烧成灰,选用②和③ |
| B.过滤得到滤液,选用④、⑤、⑦和⑩ |
| C.向滤液中加入过氧化氢将碘离子氧化为I2,选用④和⑦ |
| D.检验I2,选用③、⑧和⑩ |
您最近一年使用:0次
名校
解题方法
7 . 下列实验操作或实验仪器的使用正确的是
| A.做“海带中碘元素的分离及检验”实验时,须用过量的氯气或双氧水氧化I- |
| B.用剩的药品能否放回原瓶,应视具体情况而定 |
| C.其他条件相同时,双氧水在碱性溶液中分解速率比在酸性溶液中慢 |
| D.滴定接近终点时,滴定管的尖嘴不能接触锥形瓶内壁 |
您最近一年使用:0次
2023-04-02更新
|
905次组卷
|
3卷引用:山东省烟台第一中学2023-2024学年高三下学期2月份开学考试化学试题
名校
8 . 下列生产过程中只发生物理变化的是
| A.煤的气化 | B.海带提碘 | C.氯碱工业 | D.海水晒盐 |
您最近一年使用:0次
名校
解题方法
9 . 海洋资源的利用具有广阔前景。
(1)下图是从海水中提取粗溴的主要流程

①从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是_______ 。
②可用热空气吹出溴是因为溴的_______ (选填编号)
A.熔点较低 B.熔点较高 C.沸点较低 D.沸点较高
(2)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是_______ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_______ 。反应结束后,再加入 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为_______ ,可以观察到 层呈
层呈_______ 色。
(1)下图是从海水中提取粗溴的主要流程

①从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是
②可用热空气吹出溴是因为溴的
A.熔点较低 B.熔点较高 C.沸点较低 D.沸点较高
(2)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:
①灼烧海带至灰烬时所用的主要仪器名称是
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为 层呈
层呈
您最近一年使用:0次
2023-03-09更新
|
512次组卷
|
3卷引用:吉林省长春外国语学校2023-2024学年高二上学期开学考试化学试题
名校
10 . 海水晒盐后精制得到 ;氯碱工业电解饱和
;氯碱工业电解饱和 溶液得到
溶液得到 和
和 ;向海水晒盐得到的卤水中通
;向海水晒盐得到的卤水中通 可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是

 ;氯碱工业电解饱和
;氯碱工业电解饱和 溶液得到
溶液得到 和
和 ;向海水晒盐得到的卤水中通
;向海水晒盐得到的卤水中通 可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
| A.用装置甲灼烧碎海带 | B.用装置乙过滤海带灰的浸泡液 |
C.用装置丙制备用于氧化浸泡液中 的 的 | D.用装置丁吸收氧化浸泡液中 后的 后的 尾气 尾气 |
您最近一年使用:0次
2023-02-16更新
|
228次组卷
|
2卷引用:江苏省苏州市木渎高级中学2022-2023学年高一下学期期初调研化学试题



