解题方法
1 . 下列反应的离子方程式书写错误的是
| A.Na2O2与足量盐酸反应:2Na2O2+4H+=4Na++O2↑+2H2O |
| B.向海带灰浸出液中滴加几滴硫酸酸化的过氧化氢溶液: 2I- + H2O2+2H+= I2 + 2H2O |
C.向草酸溶液 中滴加几滴高锰酸钾酸性溶液:2 + 5H2C2O4+ 6H+ = 2Mn2++ 10CO2↑+ 8H2O + 5H2C2O4+ 6H+ = 2Mn2++ 10CO2↑+ 8H2O |
D.向硫酸铝溶液中加入过量氨水: Al3+ + 4OH-= +2H2O +2H2O |
您最近一年使用:0次
解题方法
2 . 海带中含有丰富的碘元素,从海带中提取碘的实验流程如图所示:
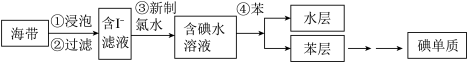
(1)进行步骤②过滤操作时,需要使用的玻璃仪器有_______ 。
(2)写出步骤③所发生反应的离子方程式:_______ 。
(3)步骤④的操作名称是_______ 。该步骤中不能用酒精代替苯的理由是_______ 。
(4)检验提取碘后水层是否仍含碘单质的方法是_______ 。

(1)进行步骤②过滤操作时,需要使用的玻璃仪器有
(2)写出步骤③所发生反应的离子方程式:
(3)步骤④的操作名称是
(4)检验提取碘后水层是否仍含碘单质的方法是
您最近一年使用:0次
解题方法
3 . 海水是一个巨大的化学资源宝库。下列有关海水综合利用的说法正确的是
A.从海水中可以获得 ,电解 ,电解 溶液可制备金属钠 溶液可制备金属钠 |
| B.从海水中提取溴的过程中利用了氧化还原反应原理 |
| C.海水中含有镁元素,只需经过物理变化就可以得到镁单质 |
D.目前工业上可直接从海水中提取 |
您最近一年使用:0次
2022-11-24更新
|
136次组卷
|
2卷引用:苏教2020版化学必修第一册专题3 从海水中获得的化学物质 第三单元 海洋化学资源的综合利用课后习题
名校
解题方法
4 . 海水资源的利用具有非常广阔的前景。
I.情景1——实验室模拟海带提碘
某化学兴趣小组在实验室模拟从海带中提取碘的实验,实验流程如图所示。
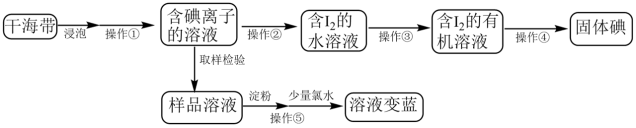
(1)提碘的原料一般选择海带或海藻,是因为_______ ,操作①的名称是_______ 。
(2)操作②为氧化,实验室一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,请写出该步骤中发生反应的离子方程式是_________ 。
(3)操作③用到的主要仪器是________ ;该步骤中加入石油醚能提取碘水中的碘,说明石油醚不溶于水,不与水反应,且______ 。操作④通过敞口挥发就能得到固体碘。
(4)操作⑤取样检验时,最好是先加入数滴淀粉溶液再逐滴加入少量氯水,请解释这样做的原因____________ 。
II.情景2——离子交换法从海带中提取碘
用离子交换法从海带中提取碘是一种较为先进的制碘工艺应用技术。下图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。
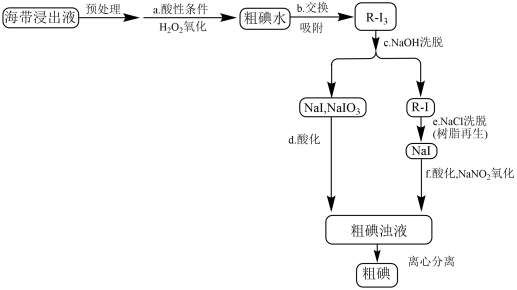
已知:①I2+I-⇌
②强碱性阴离子树脂(用R-Cl表示)对多碘离子( )有很强的交换吸附能力。
)有很强的交换吸附能力。
③步骤b交换吸附时发生的反应:R-Cl+ =R-I+Cl-。
=R-I+Cl-。
试回答下列问题:
(5)图中a、b、c、d、e、f各步反应中,属于氧化还原反应的有:___________ (填序号)
(6)酸性条件下,原料被H2O2氧化时发生的反应有:①2I-+H2O2+2H+=I2+2H2O;②I2+I-⇌ 。依据整个生产流程分析是否可以加足量H2O2?说明理由。
。依据整个生产流程分析是否可以加足量H2O2?说明理由。___________
(7)图中在NaCl洗脱时离子交换树脂(表示为R-Cl)可以得到再生,并重复使用,请用化学方程式表示离子交换树脂再生的原理___________ 。
III.情景3——海水提镁
目前世界上60%的镁是从海水中提取的。已知海水提镁的主要步骤如下:
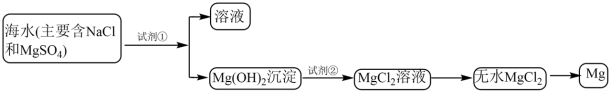
(8)为了使镁离子沉淀下来,加入的足量试剂①________ 。加入的足量试剂②是________ (填化学式)。
(9)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:MgCl2(熔融) Mg+Cl2↑,标出电子转移的方向和数目
Mg+Cl2↑,标出电子转移的方向和数目_______ 。
(10)氯气是MgCl2转化为Mg时获得的副产品,用化学方程式表示该物质的某种用途______ 。
I.情景1——实验室模拟海带提碘
某化学兴趣小组在实验室模拟从海带中提取碘的实验,实验流程如图所示。

(1)提碘的原料一般选择海带或海藻,是因为
(2)操作②为氧化,实验室一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,请写出该步骤中发生反应的离子方程式是
(3)操作③用到的主要仪器是
(4)操作⑤取样检验时,最好是先加入数滴淀粉溶液再逐滴加入少量氯水,请解释这样做的原因
II.情景2——离子交换法从海带中提取碘
用离子交换法从海带中提取碘是一种较为先进的制碘工艺应用技术。下图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。

已知:①I2+I-⇌

②强碱性阴离子树脂(用R-Cl表示)对多碘离子(
 )有很强的交换吸附能力。
)有很强的交换吸附能力。③步骤b交换吸附时发生的反应:R-Cl+
 =R-I+Cl-。
=R-I+Cl-。试回答下列问题:
(5)图中a、b、c、d、e、f各步反应中,属于氧化还原反应的有:
(6)酸性条件下,原料被H2O2氧化时发生的反应有:①2I-+H2O2+2H+=I2+2H2O;②I2+I-⇌
 。依据整个生产流程分析是否可以加足量H2O2?说明理由。
。依据整个生产流程分析是否可以加足量H2O2?说明理由。(7)图中在NaCl洗脱时离子交换树脂(表示为R-Cl)可以得到再生,并重复使用,请用化学方程式表示离子交换树脂再生的原理
III.情景3——海水提镁
目前世界上60%的镁是从海水中提取的。已知海水提镁的主要步骤如下:

(8)为了使镁离子沉淀下来,加入的足量试剂①
(9)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:MgCl2(熔融)
 Mg+Cl2↑,标出电子转移的方向和数目
Mg+Cl2↑,标出电子转移的方向和数目(10)氯气是MgCl2转化为Mg时获得的副产品,用化学方程式表示该物质的某种用途
您最近一年使用:0次
5 . 化学与生活、生产、能源及环境等密切相关。下列说法正确的是
| A.向浸泡过海带灰的水中滴入淀粉溶液有蓝色出现 |
| B.“天宫二号”空间实验室的硅电池板将光能直接转换为电能 |
| C.由植物及其废弃物制成的燃料乙醇属于不可再生能源 |
| D.用Na2S作还原剂可除去污水中的Cu2+和Hg2+ |
您最近一年使用:0次
解题方法
6 . 从海带中提取碘的工艺流程如图所示,下列说法错误的是


| A.步骤1可在坩埚中灼烧干海带 |
| B.步骤3反应的离子方程式为2I-+H2O2+2H+=I2+2H2O |
| C.设计步骤4、5的目的是富集碘,降低成本,提高生产效率 |
| D.步骤6的实验操作名称是蒸馏 |
您最近一年使用:0次
名校
7 . 从海带中提取碘单质的工艺流程如下。下列关于海水制碘的说法不正确 的是
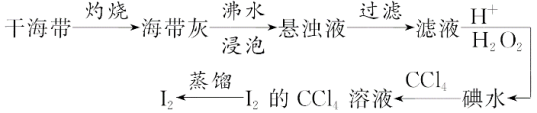

| A.在碘水中加入几滴淀粉溶液,溶液变蓝色 |
| B.实验室在坩埚中灼烧干海带,并且用玻璃棒搅拌 |
| C.含I-的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 |
| D.碘水加入CCl4得到I2的CCl4溶液,该操作为“萃取” |
您最近一年使用:0次
2022-01-01更新
|
344次组卷
|
2卷引用:黑龙江省大庆铁人中学2021-2022学年高二上学期期末考试化学试题
名校
8 . 海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确 的是
A.向苦卤中通入 是为了提取溴 是为了提取溴 |
B.从海水中可以得到 ,电解 ,电解 饱和溶液可制备 饱和溶液可制备 |
| C.工业上通常选用氢氧化钠作为沉淀剂提镁 |
D.目前工业上直接由海水提取 |
您最近一年使用:0次
名校
解题方法
9 . 已知苯的密度为0.81g/cm3; 。从海带中提取碘的实验过程如下:
。从海带中提取碘的实验过程如下:
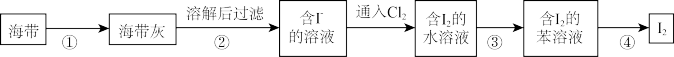
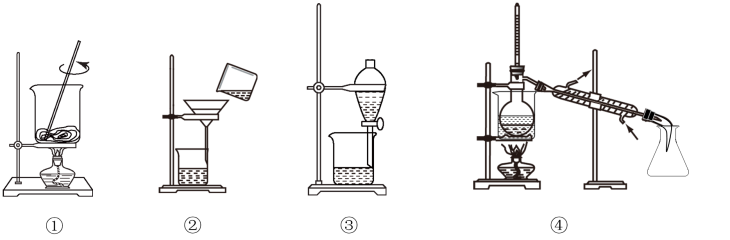
以上过程中,涉及到下列操作的示意图,其中正确的是
 。从海带中提取碘的实验过程如下:
。从海带中提取碘的实验过程如下: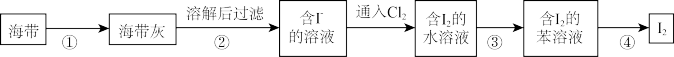
以上过程中,涉及到下列操作的示意图,其中正确的是

| A.①将海带灼烧成灰 | B.②过滤得含 的溶液 的溶液 |
| C.③碘的苯溶液从下层放出 | D.④分离碘并回收苯 |
您最近一年使用:0次
10 . 实验室模拟工业制法从卤水中的碘(主要以I-形式存在)提取碘产品的工艺流程如下:
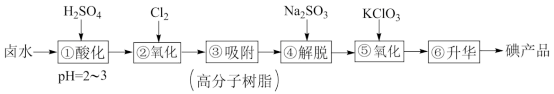
回答下列问题:
(1)实验室中常用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,所用装置如图所示:
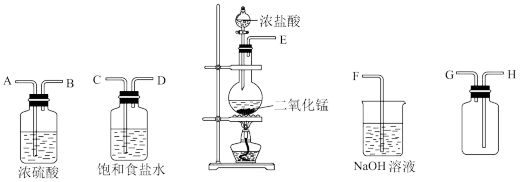
①写出气体发生装置制取氯气的化学方程式___________ 。
②连接上述仪器的正确顺序(填各接口处的字母)是:___________ 。
___________接___________;___________接___________;___________接___________;___________接___________。
③装置中,饱和食盐水的作用是___________ 。
(2)设计步骤③和④的目的是___________ 。
(3)步骤④解脱反应的离子方程式为___________ 。
(4)若②和⑤中分别得到等量I2,则消耗的m(Cl2):m(KClO3)=___________ 。

回答下列问题:
(1)实验室中常用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,所用装置如图所示:

①写出气体发生装置制取氯气的化学方程式
②连接上述仪器的正确顺序(填各接口处的字母)是:
___________接___________;___________接___________;___________接___________;___________接___________。
③装置中,饱和食盐水的作用是
(2)设计步骤③和④的目的是
(3)步骤④解脱反应的离子方程式为
(4)若②和⑤中分别得到等量I2,则消耗的m(Cl2):m(KClO3)=
您最近一年使用:0次



