名校
解题方法
1 . 海带灰富含以I-形式存在的碘元素。在实验室中,从海带灰浸取液中提取碘单质的流程如图:
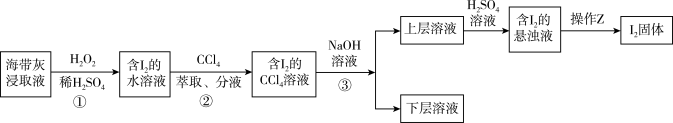
下列说法正确的是

下列说法正确的是
| A.为提高①中反应的速率,可增大硫酸浓度或在高温条件下进行 |
| B.操作②中CCl4,可用酒精、苯等代替 |
| C.操作③使用的是反萃取法,得到的上层溶液为紫红色 |
| D.操作Z所需的玻璃仪器有烧杯、玻璃棒、漏斗 |
您最近一年使用:0次
2022-07-07更新
|
585次组卷
|
4卷引用:山东省济南市2021-2022学年高一下学期期末考试化学试题
名校
解题方法
2 . 我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:
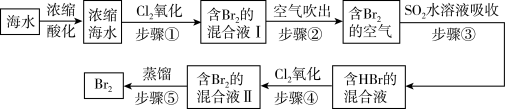
(1)步骤①中获得Br2的离子方程式为____ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是____ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有___ 个电子转移(用a和NA的代数式表示)。
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:____ 、____ 。
(5)“试剂a”通常应具有一定的____ 性。
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:____ 。
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___ 。(选填编号)
(7)“操作II”宜选用的装置是____ 。(选填编号)
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:____ 。
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是____ mg•g-1(保留四位小数)。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:
(5)“试剂a”通常应具有一定的
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水不互溶不与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
(7)“操作II”宜选用的装置是
A. | B.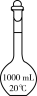 | C.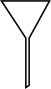 | D. |
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O
 =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
3 . 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O。(_______)
您最近一年使用:0次
2022-02-26更新
|
558次组卷
|
7卷引用:专题08 化学方程式正误判断—2022年高考化学二轮复习讲练测(全国版)-讲义
(已下线)专题08 化学方程式正误判断—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)考点04 离子反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)第一章 化学物质及其变化 第2讲 离子反应离子方程式(已下线)考点04 离子反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)
名校
4 . 从海产品中提取碘是我国工业上获取碘的重要途径,实验室证明海带中存在碘元素的方法如下:
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的_______ (填标号)。
a. b.
b. c.
c. d.
d.
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。
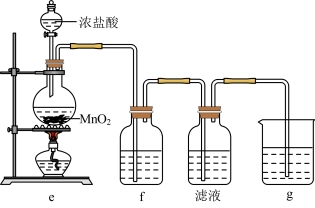
①装置e中发生反应的化学方程式是_______ 。
②装置f、g中所装的试剂分别是_______ 、_______ 。
③检验“滤液”中有碘单质生成的方法是_______ 。若通入 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是_______ 。
(3)“步骤Ⅲ”氧化剂氧化时,用 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是_______ 。
(4)若“步骤Ⅲ”所得溶液经过分离提纯获得 ,其物质的量是
,其物质的量是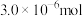 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是_______ mg/kg。
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的
a.
 b.
b. c.
c. d.
d.
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。

①装置e中发生反应的化学方程式是
②装置f、g中所装的试剂分别是
③检验“滤液”中有碘单质生成的方法是
 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是(3)“步骤Ⅲ”氧化剂氧化时,用
 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是(4)若“步骤Ⅲ”所得溶液经过分离提纯获得
 ,其物质的量是
,其物质的量是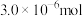 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是
您最近一年使用:0次
2022-07-20更新
|
525次组卷
|
3卷引用:辽宁省县级重点高中协作体2021-2022学年高一下学期期末考试化学试题
5 . 下列说法正确的是
| A.二氧化硅有很好的导电性,可用于制造光导纤维 |
| B.侯氏制碱法的原理是将氨通入二氧化碳的氯化钠饱和溶液中,使碳酸钠从溶液中析出 |
| C.生铁含碳2%-4.5%,将生铁进一步炼制,就可以得到用途更广泛的钢(含碳0.03%-2%) |
D.工业上以海带为原料制碘时,利用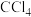 萃取碘水中的碘,分液、蒸馏获得粗碘 萃取碘水中的碘,分液、蒸馏获得粗碘 |
您最近一年使用:0次
2022-02-22更新
|
482次组卷
|
2卷引用:浙江省浙南名校联考2021-2022学年下学期高三返校联考化学试题
6 . 下列方案设计、现象和结论有不正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 氨水中NH3检验 | 在一支洁净的试管中滴加几滴氨水,将湿润的红色石蕊试纸粘在玻璃棒上靠近试管口,观察试纸颜色变化。 | 若试纸由红色变为蓝色, 则有NH3 |
| B | 海带中碘元素的检验 | 取3g干燥的海带灼烧,在灰分中加入蒸馏水,过滤,在滤液中加入适量稀硫酸,再加入适量新制氯水,取出少许混合液于试管中,滴入几滴淀粉溶液。 | 若溶液显蓝色,则含碘元素。 |
| C | 火柴头中氯元素的检验 | 摘下几根火柴的火柴头, 将火柴头浸于蒸馏水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液。 | 若出现白色沉淀,则含氯元素 |
| D | 乙酸乙酯水解条件的比较 | 取两支试管编号为1、2,1中加入4mL蒸馏水+2滴甲基橙+2mL乙酸乙酯,2中加入4 mL4mol/LNaOH溶液+2滴石蕊溶液+2mL乙酸乙酯,振荡后同时插入75°C热水浴,加热约5分钟。观察现象。 | 1中颜色无变化,2中颜色蓝色变浅,说明水解程度 2大于1. |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 浩瀚的海洋里蕴藏着丰富的化学资源,从海带中提取碘单质和从海水中提取溴单质的工艺流程如图。回答下列问题:
I.海带提碘
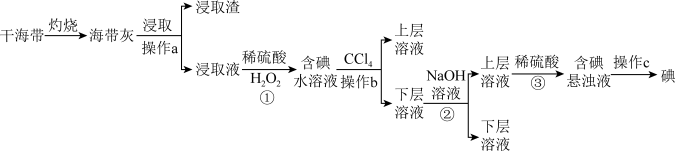
(1)在实验室进行干海带的灼烧操作时,需要用到的下列仪器有____ (填标号)。
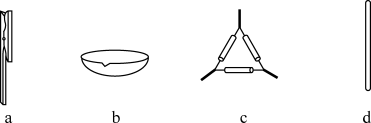
(2)浸取液中碘主要以I-存在,写出①发生反应的离子方程式____ 。
(3)操作b的名称为____ 。
(4)写出②加入NaOH溶液的目的____ ;写出③反应中氧化剂与还原剂物质的量之比为____ 。
II.海水提溴
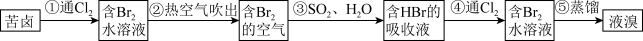
(5)流程中能说明同主族元素性质递变规律的反应为____ (写出离子方程式)。
(6)步骤③化学方程式为____ 。
I.海带提碘

(1)在实验室进行干海带的灼烧操作时,需要用到的下列仪器有

(2)浸取液中碘主要以I-存在,写出①发生反应的离子方程式
(3)操作b的名称为
(4)写出②加入NaOH溶液的目的
II.海水提溴
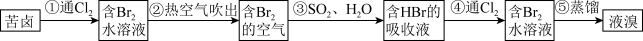
(5)流程中能说明同主族元素性质递变规律的反应为
(6)步骤③化学方程式为
您最近一年使用:0次
2022-05-23更新
|
452次组卷
|
2卷引用:山东省青岛地区2021-2022学年高一下学期期中考试化学试题
名校
8 . 海带是一种含碘量很高的海藻,从中提取的磷广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图,下列有关说法正确的是
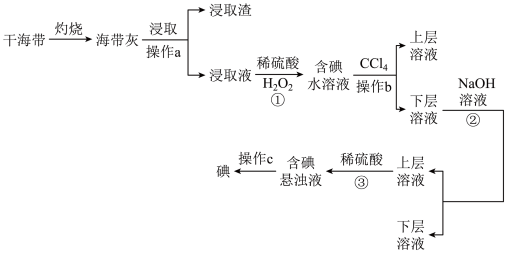

| A.实验室将干海带置于蒸发皿中灼烧 |
| B.操作a与操作c方法相同 |
| C.操作b中用于提取碘的试剂还可以是乙醇 |
D.③的离子方程式: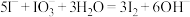 |
您最近一年使用:0次
2022-07-14更新
|
418次组卷
|
3卷引用:山东省菏泽市2021-2022学年高一下学期期末教学质量检测化学试题
名校
9 . 利用提供的实验仪器(夹持装置任选)和药品不能完成的实验是
| 实验仪器 | 分液漏斗、酒精灯、烧杯、蒸发皿、试管、漏斗、玻璃棒、三脚架、泥三角、双孔橡胶塞、胶头滴管、导管、石棉网 |
| 药品 | 溴乙烷、粗硝酸钾、硝酸、盐酸、 、 、 、 、 、 、 、蒸馏水 、蒸馏水 |
| A.检验溴乙烷中的溴原子 |
B.验证元素非金属性: |
| C.重结晶法提纯硝酸钾 |
| D.海带提碘实验中灼烧干海带 |
您最近一年使用:0次
2022-01-17更新
|
760次组卷
|
6卷引用:山东省烟台市2021-2022学年高三上学期期末考试化学试题
山东省烟台市2021-2022学年高三上学期期末考试化学试题湖南省衡阳市第八中学2021-2022学年高三下学期开学考试(第六次月考)化学试题(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)趋势1 创新命题形式湖南省岳阳市岳阳县第一中学2023-2024学年高三下学期3月月考化学试题
名校
解题方法
10 . 实验室进行海带提碘实验,萃取后继续分离得到单质碘的主要操作:用浓氢氧化钠溶液进行反萃取、分液、酸化、过滤及干燥等。下列对应各实验步骤的装置错误的是
A.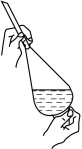 | B.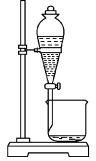 | C. | D.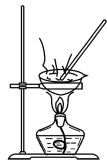 |
您最近一年使用:0次



