9. 高锰酸钾是一种典型的强氧化剂,热分解产生锰酸钾、二氧化锰、氧气。
Ⅰ.已知:①MnO
2(s)=Mn(s)+O
2(g)
∆
H=+520 kJ·mol
-1②S(s)+O
2(g)=SO
2(g)
∆
H=-297 kJ·mol
-1③Mn(s)+2O
2(g)+S(s)=MnSO
4(s)
∆
H=-1065 kJ·mol
-1固体MnO
2和二氧化硫气体反应生成MnSO
4固体的热化学方程式为
___________。
Ⅱ.将KMnO
4酸性溶液充分加热,溶液紫色褪去,产生无色气体,反应的离子方程式为
___________。
Ⅲ.KMnO
4是一种常用消毒剂,其消毒机理与下列物质相似的是
___________(填字母编号)。
A.双氧水 B.75%消毒酒精 C.肥皂水 D.“84”消毒液
Ⅳ.测定KMnO
4产品的纯度可用标准Na
2S
2O
3溶液进行滴定。
(1)配制250 mL 0.1000 mol•L
-1标准Na
2S
2O
3溶液,需要使用的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管和
___________。所需蒸馏水应加热煮沸后冷却备用,目的是
___________。
(2)取KMnO
4粗品2.1000 g溶于水,并在溶液中加入
___________进行酸化(填字母编号)。
A.稀盐酸
B.稀硫酸
C.硝酸
D.次氯酸
(3)将(2)所得溶液平均分成三份,分别用标准Na
2S
2O
3溶液进行滴定,记录实验消耗Na
2S
2O
3溶液的体积。
①放标准溶液的仪器应选
___________(填“甲”或“乙”);
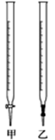
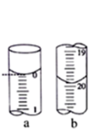
②第一次滴定过程中滴定管滴定初始和结束时读数如图,所用标准液体积为
V1=
___________mL;
③重复滴定两次,三次平行实验数据如表:(有关离子方程式为:8MnO

+5S
2O

+14H
+=10SO

+8Mn
2++7H
2O)
| 实验次数 | 1 | 2 | 3 |
| 消耗Na2S2O3溶液体积/mL | V1 | 20.10 | 20.00 |
计算该KMnO
4产品的纯度为
___________%(保留一位小数)。
④若测定结果偏高,其原因可能是
___________(填字母编号)。
A.滴定管用蒸馏水洗净后未用标准溶液润洗
B.滴定终点读数时,俯视滴定管,其他操作正确
C.配制标准溶液时,俯视定容
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液