10. 研究CO
2的综合利用、实现CO
2资源化,生产高能燃料和高附加值化学品,有利于实现碳资源的有效循环,是力争2030年前实现碳达峰、2060年前实现碳中和的方向之一。
回答下列问题:
(1)已知下列反应的热化学方程式:
I.CO
2(g)+H
2(g)

CO(g)+H
2O(g) ΔH
1=+41.2kJ•mol
-1Ⅱ.2CO(g)+4H
2(g)

C
2H
4(g)+2H
2O(g) ΔH
2Ⅲ.2CO
2(g)+6H
2(g)

C
2H
4(g)+4H
2O(g) ΔH
3=-249.6kJ•mol
-1反应Ⅱ中,ΔH
2=
________。
(2)将等物质的量CO(g)和H
2O(g)充入恒容密闭容器中发生如下反应:CO(g)+H
2O(g)=CO
2(g)+H
2(g),已知反应速率v=v
正-v
逆=k
正•(CO)•c(H
2O)-k
逆•c(CO
2)•c(H
2),其中k
正、k
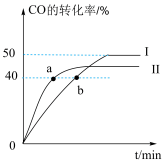
逆分别为正、逆反应速率常数。在不同温度下,CO的转化率随时间变化曲线如图所示。计算b处的

=
________。
(3)在体积为2L的恒压密闭容器中,起始充入1molCO
2(g)和3molH
2(g),发生反应Ⅲ,该反应在不同温度下达到平衡时,各组分的体积分数随温度的变化如图所示。
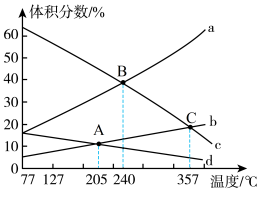
①表示H
2的体积分数随温度变化的曲线是
________(填字母序号)。
②205℃时,反应达到平衡后,容器中气体的总物质的量为
________mol,CO
2(g)的平衡转化率为
________。若平衡时总压为P,该反应的平衡常数K
p=
________(列出计算式)。
(4)CO
2加氢制甲醇也具有重要的经济价值,其热化学方程式为CO
2(g)+3H
2(g)=CH
3OH(g)+H
2O(g) ΔH<0,但也存在竞争反应CO
2(g)+H
2(g)=CO(g)+H
2O(g) ΔH>0,在恒温密闭容器中,维持压强和投料比不变,将CO
2和H
2按一定流速通过反变应器,CO
2转化率和甲醇选择性[x(CH
3OH)%

]随温度化关系如图所示:
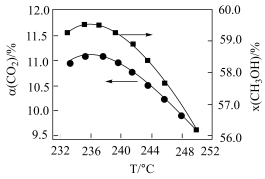
若233~251℃时催化剂的活性受温度影响不大,分析235℃后图中曲线下降的原因:
________。