福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
福建
高一
期末
2021-07-21
661次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、有机化学基础、认识化学科学、化学反应原理、化学实验基础、物质结构与性质
福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
福建
高一
期末
2021-07-21
661次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、有机化学基础、认识化学科学、化学反应原理、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
1. 环保意识是重要的公民意识,下列环境问题与氮氧化物无关的是
| A.酸雨 | B.光化学烟雾 | C.温室效应 | D.臭氧层空洞 |
您最近一年使用:0次
2021-07-15更新
|
1006次组卷
|
6卷引用:福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题(已下线)5.2.3 硝酸 酸雨及其防治-2021-2022学年高一化学课后培优练(人教版2019必修第二册)福建省福州格致中学2022-2023学年高一下学期期中考试化学试题第五章 化工生产中的重要非金属元素(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第五章 化工生产中的重要非金属元素【单元测试A卷】江苏省连云港市七校2023-2024学年高一下学期期中联考化学试题
单选题
|
适中(0.65)
名校
2. 下列叙述中,错误 的是
| A.“可燃冰”开采不当,可能会加剧温室效应 |
| B.石油的分馏与裂解、煤的液化与干馏均发生化学变化 |
| C.液化石油气(LPG)是石油的分馏产品,其主要成分是烃类 |
| D.利用油脂碱性水解可制造肥皂 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. 下列化学用语正确的是
| A.乙基的结构简式:CH3CH2— | B.乙炔的结构简式:CHCH |
C.丙烷的比例模型: | D.氨分子的电子式: |
您最近一年使用:0次
2021-07-15更新
|
125次组卷
|
2卷引用:福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 下列反应属于加成反应的是
A.2CH3CHO+O2 2CH3COOH 2CH3COOH |
B.CH2=CH2+H2O CH3CH2OH CH3CH2OH |
C. +HNO3 +HNO3  +H2O +H2O |
D.CH3COOC2H5+NaOH CH3COONa+CH3CH2OH CH3COONa+CH3CH2OH |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
5. 阿伏加德罗常数的值为NA.下列说法正确的是
| A.标准状况下,11.2L苯中含有的分子数为0.5NA |
| B.常温常压下,4.6g乙醇中C—H键的数目为0.6NA |
| C.0.1molN2与O2的混合气体中,所含原子总数为0.2NA |
| D.某容器中充入中0.1molN2与0.4molH2,一定条件下充分反应得到NH3分子数为0.2NA |
【知识点】 阿伏加德罗常数的应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. 下列各组物质互为同素异形体的是
| A.CH3COOCH3和CH3CH2COOH | B.苯与甲苯( ) ) |
| C.35Cl2和37Cl2 | D.石墨和C60 |
【知识点】 苯的同系物的组成、结构解读 酯的结构
您最近一年使用:0次
单选题
|
适中(0.65)
名校
7. 下列说法不正确的是
| A.可用溴水或酸性高锰酸钾鉴别己烯、苯和四氯化碳三种无色液体 |
| B.碳酸氢铵应保存在阴凉处,且不能与碱性肥料混合施用 |
| C.原电池加快某些反应的速率,所以用锌与稀硫酸反应制取氢气常加入少量硫酸铜 |
| D.同条件下反应物浓度越大反应越快,所以铁在浓硝酸中比在稀硝酸中溶解得快 |
您最近一年使用:0次
单选题
|
容易(0.94)
名校
解题方法
8. 肼(N2H4)可作为发射火箭的燃料。已知1g液态肼(N2H4)在空气中燃烧生成氮气和水蒸气放出16.7kJ的热量,该反应的热化学方程式是
| A.N2H4(l)+O2(g)=2H2O(g)+N2(g) ΔH=-16.7kJ·mol-1 |
| B.N2H4(l)+O2(g)=2H2O(1)+N2(g) ΔH=-534.4kJ·mol-1 |
| C.N2H4(l)+O2(g)=2H2O(g)+N2(g) ΔH=-534.4kJ·mol-1 |
| D.N2H4(l)+O2(g)=2H2O(g)+N2(g) ΔH=+534.4kJ·mol-1 |
您最近一年使用:0次
2020-08-07更新
|
494次组卷
|
8卷引用:福建省福州市2019-2020学年高一下学期期末考试化学试题
单选题
|
适中(0.65)
名校
9. 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价一物质类别关系如图,以下说法正确的是
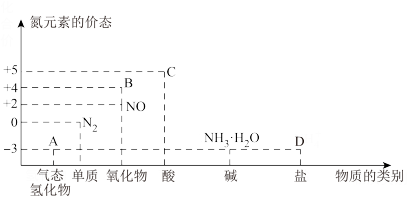

| A.物质A转化为NO需要加入氧化剂 |
| B.标准状况下,3.36L物质B与水完全反应,电子转移0.2mol |
C.物质C的浓溶液与Cu反应的离子方程式为3Cu+8H++2 =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
| D.D中阳离子的检验方法是取少量溶液于试管中,加热,生成气体能使湿润的红色石蕊试纸变蓝 |
您最近一年使用:0次
2021-07-15更新
|
315次组卷
|
2卷引用:福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
单选题
|
较易(0.85)
名校
10. 可逆反应2SO2(g)+O2(g)⇌2SO3(g)的能量变化如图所示,下列说法正确的是


| A.该反应达到平衡后,正、逆反应速率均为0 |
| B.其它条件不变,升温,正反应速率增大,逆反应速率减慢 |
| C.2SO3(g)⇌2SO2(g)+O2(g) ∆H=-(y-x)kJ/mol |
| D.2molS(g)、6molO(g)生成2molSO3(g),共放出ykJ能量 |
【知识点】 能量的相互转化 影响化学反应速率的外因
您最近一年使用:0次
11. 下列装置能达到相应实验目的的是
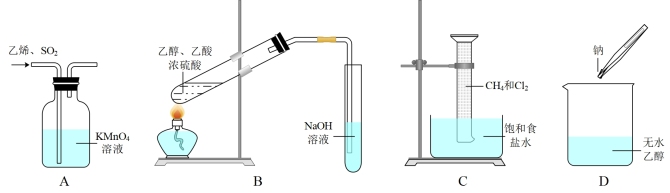

| A.除去C2H4中少量SO2 | B.制取少量乙酸乙酯 |
| C.观察甲烷与氯气在光照条件下的反应 | D.检验无水乙醇中是否有水 |
您最近一年使用:0次
2021-07-15更新
|
376次组卷
|
3卷引用:福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
单选题
|
较易(0.85)
名校
解题方法
12. 向某容积一定的密闭绝热容器中充入2molNO和1molO2,一定条件下发生反应:2NO(g)+O2(g)  2NO2(g),其反应速率与反应时间关系如下图所示,下列选项表明达到平衡状态的是
2NO2(g),其反应速率与反应时间关系如下图所示,下列选项表明达到平衡状态的是

 2NO2(g),其反应速率与反应时间关系如下图所示,下列选项表明达到平衡状态的是
2NO2(g),其反应速率与反应时间关系如下图所示,下列选项表明达到平衡状态的是
| A.NO、O2物质的量之比为2∶1 |
| B.M、N、P、Q四点中,N点时反应已达平衡状态 |
| C.混合气体的总质量不再变化 |
| D.单位时间内生成2amolNO2的同时,生成amolO2 |
【知识点】 化学平衡状态 化学平衡状态本质及特征解读 化学平衡状态的判断方法解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
13. 潜艇中使用的液氨—液氧燃料电池工作原理如图所示,下列有关说法正确的是


| A.电极b名称是负极 |
| B.电极a上发生氧化反应 |
| C.电解质溶液中OH—向b极移动 |
| D.电极b的电极反应式为:O2+4e—+4H+=2H2O |
您最近一年使用:0次
2021-07-15更新
|
355次组卷
|
2卷引用:福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
单选题
|
较易(0.85)
名校
14. 将12.8g铜与80mL10mol/L的HNO3充分反应后,溶液中含0.1molH+,由此可知
| A.生成的气体只有二氧化氮 |
| B.反应中转移的电子的物质的量为0.2mol |
| C.被还原的硝酸的物质的量为0.3mol |
D.反应后溶液中所含NO 的物质的量为0.4mol 的物质的量为0.4mol |
您最近一年使用:0次
2021-07-15更新
|
330次组卷
|
3卷引用:福建省仙游第一中学2020-2021学年高一下学期期末考试化学试题
单选题
|
较易(0.85)
名校
15. 对水样中M的分解速率的影响因素进行研究。在相同温度下,M的物质的量浓度[c(M)]随时间(t)的变化如下图所示。下列说法错误的是


| A.在0~20min内,②中M的分解速率为0.015 mol∙L−1∙min−1 |
| B.由②③得,水样酸性越强,M的分解速率越快 |
| C.由①③得,反应物浓度越大,M的分解速率越快 |
| D.水样中添加Cu2+,能加快M的分解速率 |
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
16. 元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是六种短周期元素的原子半径及主要化合价(已知铍元素的原子半径为0.089 nm)。
(1)C元素在周期表中的位置为_______ ,其离子结构示意图为:_______
(2)B的最高价氧化物对应的水化物与Y的最高价氧化物对应的水化物反应的离子方程式为_______
(3)关于C、D 两种元素说法正确的是_______ (填序号)
a.简单离子的半径D>C
b.气态氢化物的稳定性D比C强
c.最高价氧化物对应的水化物的酸性C比D强
(4)在100mL18mol/L的C的最高价氧化物对应的水化物的浓溶液中加入过量的铜片,加热使其充分反应,产生气体的体积为6.72L(标况下),则该反应过程中转移的电子数为_______
(5)比较Y元素与其同族短周期元素的氢化物的熔沸点高低_______ > _______ (填氢化物化学式),理由_______
| 元素代号 | A | B | C | D | X | Y |
| 原子半径/nm | 0.037 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
| 主要化合价 | +1 | +3 | +6,-2 | -1 | -2 | +5,-3 |
(2)B的最高价氧化物对应的水化物与Y的最高价氧化物对应的水化物反应的离子方程式为
(3)关于C、D 两种元素说法正确的是
a.简单离子的半径D>C
b.气态氢化物的稳定性D比C强
c.最高价氧化物对应的水化物的酸性C比D强
(4)在100mL18mol/L的C的最高价氧化物对应的水化物的浓溶液中加入过量的铜片,加热使其充分反应,产生气体的体积为6.72L(标况下),则该反应过程中转移的电子数为
(5)比较Y元素与其同族短周期元素的氢化物的熔沸点高低
您最近一年使用:0次
2021-06-22更新
|
372次组卷
|
2卷引用:四川省成都外国语学校2020-2021学年高一下学期第三次(6月)月考化学试题
填空题
|
适中(0.65)
名校
17. 汽车行驶、某些化工厂生产过程,会向空气中排放出NOx、CO、SO2等有害气体,影响生态环境。
I.汽油中含有某种烃A.已知A的相对分子质量为100,其中氢元素的质量分数为16%,A的分子式为_______ 。
II.为防止氮的氧化物污染空气,可用氨或活性炭还原氮氧化物。回答下列问题:
(1)为了减少重型柴油车排放NOx,向尾气处理装置内自动喷入的尿素溶液在一定条件下先转化为NH3,NH3再与NOx反应生成两种无污染的物质。
①写出其中NH3与NO在一定条件下反应的化学方程式:_______ 。
②为提高此反应的速率,下列措施可行的是_______ (填字母代号)。
A.缩小容器体积 B.降低温度 C.使用适合催化剂 D.移出产物
(2)向两个1L的密闭容器中各加入活性炭(足量)和1.0molNO,发生反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
①温度为T1℃时,0~5min内,以CO2表示的该反应的平均速率v(CO2)=_______ mol·L-1·min-1;反应达到最大限度(即平衡状态)时,混合气体中N2的物质的量分数为_______ 。从反应开始到建立平衡的过程中,体系内气体的总压强_______ (填“变大”“变小”或“不变”)。
②两容器中的温度关系为T1_______ T2(填“>”“<”或“=”)。
I.汽油中含有某种烃A.已知A的相对分子质量为100,其中氢元素的质量分数为16%,A的分子式为
II.为防止氮的氧化物污染空气,可用氨或活性炭还原氮氧化物。回答下列问题:
(1)为了减少重型柴油车排放NOx,向尾气处理装置内自动喷入的尿素溶液在一定条件下先转化为NH3,NH3再与NOx反应生成两种无污染的物质。
①写出其中NH3与NO在一定条件下反应的化学方程式:
②为提高此反应的速率,下列措施可行的是
A.缩小容器体积 B.降低温度 C.使用适合催化剂 D.移出产物
(2)向两个1L的密闭容器中各加入活性炭(足量)和1.0molNO,发生反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
| 温度/℃ | 物质的量/mol | 时间 | ||||
| 0 | 5min | 9min | 10min | 12min | ||
| T1 | NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 |
| N2 | 0 | 0.21 | 0.29 | x | x | |
| T2 | NO | 1.0 | 0.50 | 0.34 | 0.34 | |
| N2 | 0 | 0.25 | 0.33 | 0.33 | ||
①温度为T1℃时,0~5min内,以CO2表示的该反应的平均速率v(CO2)=
②两容器中的温度关系为T1
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
名校
解题方法
18. A~F各物质间转化关系如下图所示。A为常见气态烃,可作果实催熟剂,其产量可作为一个国家石油化工发展水平的标志,B和D是生活中常见有机物,B常用作消毒剂,D能跟Na2CO3溶液反应,F有香味。
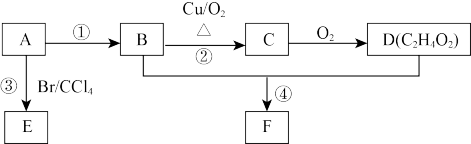
(1)D中含有的官能团_______ ,E的结构简式_______ 。
(2)反应④的反应类型为_______ 反应,写出B的同分异构体的结构简式_______ 。
(3)请写出反应②和④的化学方程式:②_______ ;④_______ 。
(4)熔喷布是口罩最核心的材料,熔喷布主要以聚丙烯为主要原料。聚丙烯可由丙烯(CH3—CH=CH2)合成。丙烯和A互为_______ (填序号)。
A.同素异形体 B.同位素 C.同系物 D.同分异构体

(1)D中含有的官能团
(2)反应④的反应类型为
(3)请写出反应②和④的化学方程式:②
(4)熔喷布是口罩最核心的材料,熔喷布主要以聚丙烯为主要原料。聚丙烯可由丙烯(CH3—CH=CH2)合成。丙烯和A互为
A.同素异形体 B.同位素 C.同系物 D.同分异构体
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
名校
19. 某研究性学习小组对实验室中NH3制取、收集、吸收,以及NH3的某些性质探究并收集少量纯净的氮气,进行了如下实验设计。
I.NH3的收集和吸收
(1)若用下图装置,排空气法收集NH3,气体应从_______ 口进入(选填“m”或“n”)。
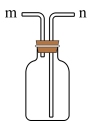
(2)已知NH3难溶于CCl4、苯。下图a~e五种装置中,不能用来吸收NH3的是_______ 。
a.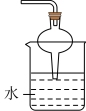 b.
b.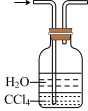 c.
c.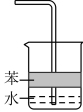 d.
d.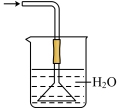 e.
e.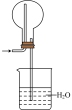
II.NH3的某些性质探究并收集少量纯净的氮气,按如下图装置进行实验(夹持仪器已略去):
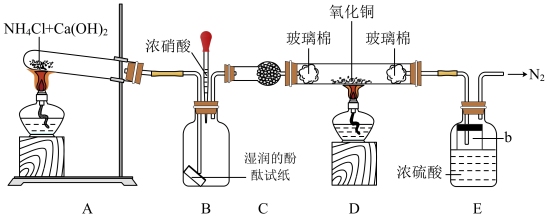
试回答下列问题:
(3)采用上图A所示装置作为NH3的发生装置,写出该反应的化学方程式_______ 。
(4)装置连接后,先检查装置气密性,然后再开始实验。装置B中观察到的现象是_______ ,挤压装置B中胶头滴管里的浓硝酸,产生的现象是_______ 。
(5)装置C中可选用的一种干燥剂_______ ;反应后装置D中固体变红,则D中发生反应的化学方程式为_______ 。装置E中仪器b的作用是_______ 和防倒吸。
(6)本实验体现了氨气的水溶液呈碱性和氨气具有_______ (填选项字母)。
A.氧化性 B.还原性 C.不稳定性
I.NH3的收集和吸收
(1)若用下图装置,排空气法收集NH3,气体应从

(2)已知NH3难溶于CCl4、苯。下图a~e五种装置中,不能用来吸收NH3的是
a.
 b.
b. c.
c. d.
d. e.
e.
II.NH3的某些性质探究并收集少量纯净的氮气,按如下图装置进行实验(夹持仪器已略去):

试回答下列问题:
(3)采用上图A所示装置作为NH3的发生装置,写出该反应的化学方程式
(4)装置连接后,先检查装置气密性,然后再开始实验。装置B中观察到的现象是
(5)装置C中可选用的一种干燥剂
(6)本实验体现了氨气的水溶液呈碱性和氨气具有
A.氧化性 B.还原性 C.不稳定性
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、有机化学基础、认识化学科学、化学反应原理、化学实验基础、物质结构与性质
试卷题型(共 19题)
题型
数量
单选题
15
填空题
2
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 硫的氧化物对人体、环境的危害 酸雨 大气污染来源及危害 大气污染的治理原理及方法 | |
| 2 | 0.65 | 油脂在碱性条件下水解 石油分馏 石油裂化、裂解 | |
| 3 | 0.65 | 结构式、结构简式、比例模型、球棍模型、最简式 共价化合物的结构及形成过程 | |
| 4 | 0.65 | 乙烯的加成反应 苯的取代反应 乙醛的催化氧化反应 酯的水解反应机理 | |
| 5 | 0.65 | 阿伏加德罗常数的应用 | |
| 6 | 0.65 | 苯的同系物的组成、结构 酯的结构 | |
| 7 | 0.65 | 硝酸的强氧化性 乙烯的加成反应 | |
| 8 | 0.94 | 反应焓变与热化学方程式的关系 热化学方程式书写及正误判断 | |
| 9 | 0.65 | 一氧化氮的化学性质 硝酸的强氧化性 | |
| 10 | 0.85 | 能量的相互转化 影响化学反应速率的外因 | |
| 11 | 0.65 | 甲烷的取代反应 乙烯与强氧化性物质的反应 物质的检验 综合实验设计与评价 | |
| 12 | 0.85 | 化学平衡状态 化学平衡状态本质及特征 化学平衡状态的判断方法 | |
| 13 | 0.65 | 原电池原理的应用 燃料电池 | |
| 14 | 0.85 | 氧化还原反应有关计算 氧化还原反应的规律 硝酸的强氧化性 铜与强氧化性酸的反应 | |
| 15 | 0.85 | 化学反应速率计算 浓度对化学反应速率的影响 催化剂对化学反应速率的影响 外因对化学反应速率影响的综合分析 | |
| 二、填空题 | |||
| 16 | 0.65 | 元素周期表提供的元素信息 由元素性质的递变规律进行相关推断 根据物质性质进行元素种类推断 | |
| 17 | 0.65 | 化学反应速率计算 影响化学反应速率的外因 化学平衡题中基于图表数据的相关计算 有关有机物分子式确定的计算 | |
| 三、解答题 | |||
| 18 | 0.65 | 单烯烃的加成反应 乙醇催化氧化 乙酸的酯化反应 有机物的推断 | 有机推断题 |
| 19 | 0.65 | 氨的还原性 氨气的实验室制法 综合实验设计与评价 | 实验探究题 |



