15. 铁黄(FeOOH)是一种重要的化工产品.由生产钛白粉废渣(主要成分为FeSO
4∙H
2O,含少量TiOSO
4和不溶物)制备铁黄的过程如下:

已知:i)TiOSO
4与水发生水解:
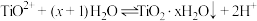
ii)Fe
2+生成Fe(OH)
2沉淀的pH:开始沉淀时pH=6.3,完全沉淀时pH=8.3;
Fe
3+生成FeOOH沉淀的pH;开始沉淀时pH=1.5,完全沉淀时pH=2.8.
(1)纯化:加入过量铁粉的作用有:①
__________;②
__________.
(2)制备晶种:为制备高品质铁黄产品,需先制备少量铁黄晶种.过程和现象是:向一定浓度FeSO
4溶液中加入氨水,产生白色沉淀,并很快变成灰绿色.滴加氨水至pH为6.0时开始通空气并记录pH变化(如图).pH≈4时制得铁黄晶种.
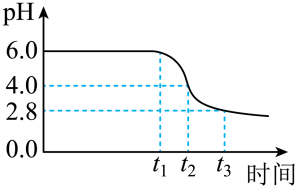
①加入氨水产生白色沉淀的离子方程式是
__________.
②0~t
2时段,Fe(OH)
2和Fe
2+转化为FeOOH制得铁黄晶种.
0~t
1时段,发生化学反应
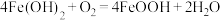
,pH几乎不变;
t
1~t
2时段,pH明显降低.用
离子方程式解释pH明显降低的原因:
__________.
(3)产品纯度测定:铁黄(FeOOH)纯度可以通过产品的耗酸量确定,实验过程如下:
wg铁黄

溶液X
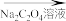
溶液Y

滴定
资料:
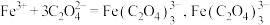
不与稀碱溶液反应;
①用NaOH标准溶液测定溶解过程中剩余的酸,当溶液中的酸恰好被NaOH完全中和时,酚酞由无色变为浅粉色(pH在8~10范围),消耗b mol∙L
-1的NaOH标准溶液V
2mL,则所得铁黄样品的纯度为
__________;(写出必要的计算过程)
②若Na
2C
2O
4过量,会使测定结果
__________(填“偏大”“偏小”或“不受影响”);