河南省林州市第一中学2019-2020学年高一6月月考化学试题
河南
高一
阶段练习
2020-08-31
253次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
一、单选题 添加题型下试题
| A.汽车轮胎 | B.涤纶外套 | C.玻璃杯 | D.棉被 |
A. 中阴离子的结构示意图为 中阴离子的结构示意图为 | B.丙烯的结构简式为 |
C. 的电子式为 的电子式为 | D.月球上富含1个中子的氦原子的符号为 |
【知识点】 有关粒子结构的化学用语 共价型分子结构式、电子式解读 烯烃 核素
 元素。下列有关说法错误的是( )
元素。下列有关说法错误的是( )A.非金属性: | B.原子半径: |
C.酸性: | D.热稳定性: |
【知识点】 元素周期表的应用 同主族元素性质递变规律
 和
和 合成
合成 ”的催化剂,其反应历程如图所示。下列说法正确的是( )
”的催化剂,其反应历程如图所示。下列说法正确的是( )
| A.该反应是吸热反应 |
| B.该反应符合绿色化学要求,原子利用率为100% |
| C.断裂化学键消耗的总能量大于形成化学键放出的总能量 |
| D.该反应断裂共价键和同时形成离子键 |
| 选项 | 事实 | 解释 |
| A | 夏天,常用冰箱保存食品和新鲜蔬菜 | 降低温度,食品和蔬菜腐烂速率减慢 |
| B | 植物油要密封保存 | 减小 的浓度,减慢植物油被氧化的速率 的浓度,减慢植物油被氧化的速率 |
| C | 烧锅炉时,常常将煤块粉碎 | 减小 和 和 气体的排放量 气体的排放量 |
| D | 酿造米酒时,在熟米饭中掺一些酒曲 | 酒曲作催化剂,加快淀粉转化成米酒 |
| A.A | B.B | C.C | D.D |
 。在恒温恒容的密闭容器中充入一定量丁烷,只发生上述反应,下列情况表明该反应一定达到平衡状态的是( )
。在恒温恒容的密闭容器中充入一定量丁烷,只发生上述反应,下列情况表明该反应一定达到平衡状态的是( )| A.气体压强保持不变 | B.混合气体的密度保持不变 |
| C.丁烷的消耗速率等于乙烷的生成速率 | D.乙烯、乙烷的浓度相等 |
【知识点】 化学平衡状态 化学平衡状态的判断方法解读 烷烃的分解解读
| 选项 | 实验操作 | 实验目的 |
| A | 向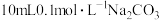 溶液中缓慢滴加 溶液中缓慢滴加 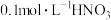 溶液 溶液 | 证明非金属性: |
| B | 在盛有 溶液的烧杯中,滴加 溶液的烧杯中,滴加 滴酚酞,然后插入一支温度计,逐滴加入 滴酚酞,然后插入一支温度计,逐滴加入 溶液 溶液 | 证明中和反应是放热反应 |
| C | 铝片、镁片在 溶液中构成原电池,观察电流计偏转方向 溶液中构成原电池,观察电流计偏转方向 | 证明镁比铝活泼 |
| D | 比较足量的 盐酸和 盐酸和 盐酸分别与等量、大小相同的锌粒反应产生 盐酸分别与等量、大小相同的锌粒反应产生 体积(相同状况下测定)的大小 体积(相同状况下测定)的大小 | 证明浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
【知识点】 能量的相互转化 化学实验方案的设计与评价
 在不同时间段的反应速率如下,其中反应速率最大的是( )
在不同时间段的反应速率如下,其中反应速率最大的是( )A.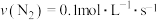 | B. |
C. | D. |
【知识点】 化学反应速率与化学计量数之间的关系解读
A.油脂在 溶液中会稳定存在 溶液中会稳定存在 |
| B.丙酸和乙酸乙酯所含的官能团相同 |
C.苯和裂化汽油都可以作碘水中 的萃取剂 的萃取剂 |
D. 与 与 丙烷在光照下反应,液态产物为混合物 丙烷在光照下反应,液态产物为混合物 |
A.简单离子的半径: | B.简单气态氢化物的热稳定性: |
C.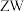 和 和 所含化学键类型完全相同 所含化学键类型完全相同 | D.X的氢化物沸点可能高于Y的氢化物 |
 。下列说法正确的是( )
。下列说法正确的是( )| A.该电池放电时将化学能全部转化为电能 | B.电池放电时, 向正极迁移 向正极迁移 |
C.正极反应式为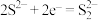 | D.消耗 时电路中转移 时电路中转移 电子 电子 |
【知识点】 原电池电极反应式书写解读 原电池原理的综合应用解读
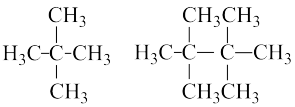
| A.M、N都不能使酸性高锰酸钾溶液褪色 |
| B.M有两种同分异构体 |
| C.M、N分子中每个碳原子都形成4个共价键 |
D.等质量的M、N在足量氧气中燃烧,完全燃烧时生成 的质量相同 的质量相同 |
 时,向
时,向 恒容密闭容器中充入
恒容密闭容器中充入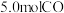 和足量镍粉,发生如下反应:
和足量镍粉,发生如下反应: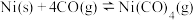 ,测得
,测得 的物质的量与时间的有关数据如表所示。
的物质的量与时间的有关数据如表所示。 | 0 | 5 | 10 | 15 | 20 |
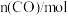 | 5.0 | 3.5 | 2.5 | 2.0 | 2.0 |
A. 时, 时,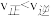 | B.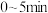 内 内 的平均反应速率 的平均反应速率 |
C.达到平衡时, | D.在该温度下,平衡状态时 |
 。下列说法错误的是
。下列说法错误的是A.R的分子式为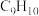 | B.R能使酸性 溶液褪色 溶液褪色 |
C.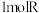 最多能与 最多能与 发生反应 发生反应 | D.R分子中苯环上的一溴代物有5种 |
二、填空题 添加题型下试题
| 元素 |  |  | B | C | N | O | F |
| X值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 |  |  |  |  | P | S |  |
| X值 | 0.9 | 1.2 | 1.5 | a | 2.1 | 2.5 | 3.0 |
(1)元素符号“B”的名称是
(2)X值大小最可能反映元素下列性质中的
a.原子半径 b.失去电子能力 c.得电子能力 d.金属性
(3)预测表格中“a”值范围为
(4)①上述元素中,简单的气态氢化物最稳定的是
②最高价氧化物对应的水化物中,碱性最强的物质的电子式为
【知识点】 元素周期律的应用
 、
、 既是燃料又是化工原料。工业上,可用煤炭在高温下与水蒸气反应制备水煤气(主要成分为
既是燃料又是化工原料。工业上,可用煤炭在高温下与水蒸气反应制备水煤气(主要成分为 和
和 ),发生的反应为
),发生的反应为 。
。(1)碳位于周期表中第
(2)在体积可变的密闭容器中发生上述反应,改变下列条件,不会改变反应速率的是
a.增大压强 b.增大炭的质量 c.增大水蒸气浓度 d.升高温度
(3)
 和
和 在一定条件下可以合成下列有机物,其中原子利用率小于100%的是
在一定条件下可以合成下列有机物,其中原子利用率小于100%的是a.
 b.
b. c.
c. d.
d.
(4)
 和
和 在
在 溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为
溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为 ;在石墨2极上发生的电极反应为
;在石墨2极上发生的电极反应为 。
。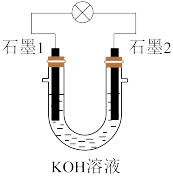
①石墨1极为
②放电时,电子流向是
a.由石墨1极流出,经外电路流向石墨2极 b.由石墨2极流出,经外电路流向石墨1极
c.由石墨1极流出,经电解质溶液流向石墨2极 d.由石墨1极流出,经电解质溶液流向石墨2极
【知识点】 影响化学反应速率的因素 氢氧燃料电池解读 元素周期表结构 能源开发利用新理念
三、解答题 添加题型下试题
 是中学实验中的常用试剂。
是中学实验中的常用试剂。实验1:甲同学设计图1装置探究硫和氯的非金属性相对强弱。

(1)A装置中发生反应的化学方程式为
 中的
中的 ,则B中的试剂是
,则B中的试剂是(2)实验过程中,C中产生浅黄色沉淀,写出C中反应的离子方程式:
实验2:乙同学设计如下实验探究影响双氧水分解反应速率的外界因素。
| 实验 | 30%的双氧水/ | 温度/℃ |  | 收集等体积的 所用时间/s 所用时间/s |
| ① |  | 25 | 0 | a |
| ② |  | 25 | 1 | b |
| ③ |  | 35 | 0 | c |
 且实验②反应后
且实验②反应后 的质量和化学性质不变,则实验结论是
的质量和化学性质不变,则实验结论是(4)设计实验①和③的目的是
实验3:为了探究在二氧化锰作用下,双氧水分解反应是放热反应还是吸热反应,进行如下实验,装置如图2所示:



(5)实验中,观察到图2烧杯中产生气泡,由此推知图3中

已知:在标准状况下,烯烃R的密度为
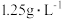 。
。(1)R的名称为
(2)A的结构简式为
(3)写出C→D的化学方程式:
(4)将R通入溴的四氯化碳溶液中,观察到的现象是
【知识点】 结合有机物性质推断有机物的结构简式解读 乙烯 乙酸的酯化反应
四、填空题 添加题型下试题
 和
和 在一定条件下反应生成
在一定条件下反应生成 。在
。在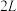 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,在一定温度下发生上述反应,反应至
,在一定温度下发生上述反应,反应至 时测得
时测得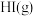 为
为 。
。(1)反应至
 时,
时, 的转化率(转化率=
的转化率(转化率= ×100%)为
×100%)为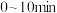 时间段内,
时间段内, 的平均反应速率为
的平均反应速率为(2)
 时气体总压强
时气体总压强(3)若起始时气体压强为
 时混合气体中
时混合气体中 的分压
的分压
 。(提示:气体分压=总压×气体的物质的量分数)
。(提示:气体分压=总压×气体的物质的量分数)
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 人工合成有机化合物的应用 常用合成高分子材料的化学成分 高分子材料 | |
| 2 | 0.65 | 有关粒子结构的化学用语 共价型分子结构式、电子式 烯烃 核素 | |
| 3 | 0.65 | 元素周期表的应用 同主族元素性质递变规律 | |
| 4 | 0.85 | 化学键与化学反应中的能量关系 吸热反应和放热反应 根据△H=反应物的键能之和-生成物的键能之和进行计算 | |
| 5 | 0.85 | 影响化学反应速率的外因 温度对化学反应速率的影响 催化剂对化学反应速率的影响 | |
| 6 | 0.85 | 元素周期表结构 元素、核素、同位素 化学键基本概念 | |
| 7 | 0.65 | 化学平衡状态 化学平衡状态的判断方法 烷烃的分解 | |
| 8 | 0.65 | 能量的相互转化 化学实验方案的设计与评价 | |
| 9 | 0.85 | 有机官能团的性质及结构 加成反应 单烯烃的加成反应 | |
| 10 | 0.85 | 化学反应速率与化学计量数之间的关系 | |
| 11 | 0.85 | 常见官能团名称、组成及结构 烷烃的取代反应 油脂 石油裂化、裂解 | |
| 12 | 0.65 | 乙醇的组成、结构 元素周期律、元素周期表的推断 根据物质性质进行元素种类推断 | |
| 13 | 0.65 | 原电池电极反应式书写 原电池原理的综合应用 | |
| 14 | 0.65 | 结合有机物性质推断有机物的结构简式 烷烃的结构特点 烷烃燃烧 利用等效变形思想解答有机物燃烧问题 | |
| 15 | 0.65 | 化学反应速率计算 化学平衡的有关计算 化学平衡建立的过程 化学平衡题中基于图表数据的相关计算 | |
| 16 | 0.65 | 有机官能团的性质及结构 同分异构体的数目的确定 芳香烃 含碳碳双键物质的性质的推断 | |
| 二、填空题 | |||
| 17 | 0.65 | 元素周期律的应用 | |
| 18 | 0.65 | 影响化学反应速率的因素 氢氧燃料电池 元素周期表结构 能源开发利用新理念 | |
| 21 | 0.65 | 化学反应速率计算 化学平衡的有关计算 化学平衡建立的过程 转化率的相关计算及判断 | |
| 三、解答题 | |||
| 19 | 0.65 | 影响化学反应速率的因素 同周期元素性质递变规律探究实验 化学实验探究 | 实验探究题 |
| 20 | 0.85 | 结合有机物性质推断有机物的结构简式 乙烯 乙酸的酯化反应 | 有机推断题 |

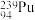 和
和 ,二者互为同位素
,二者互为同位素