四川省南充高级中学2021届高三第12次月考理综化学试题
四川
高三
阶段练习
2021-04-16
419次
整体难度:
适中
考查范围:
有机化学基础、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用
四川省南充高级中学2021届高三第12次月考理综化学试题
四川
高三
阶段练习
2021-04-16
419次
整体难度:
适中
考查范围:
有机化学基础、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 化学与生活密切相关。下列说法错误的是
| A.植物油经过物理加工可得到人造奶油 |
| B.在养鸡场鸡舍周围撒适量生石灰,可起到消毒作用 |
| C.活性炭为糖浆脱色属于物理变化 |
| D.棉、麻、丝充分燃烧都会产生二氧化碳和水 |
【知识点】 加成反应解读 淀粉和纤维素组成与结构 蛋白质组成结构
您最近一年使用:0次
2021-04-13更新
|
220次组卷
|
2卷引用:四川省南充高级中学2021届高三第12次月考理综化学试题
二、多选题 添加题型下试题
多选题
|
适中(0.65)
名校
2. 下列叙述正确的是
| A.1 mol 14C3H8与 1 mol C32H8的中子数之比为1∶1 |
| B.足量铁与1 mol 氯气完全反应,转移的电子数为3 NA |
| C.足量钠与 1 mol O2完全反应,转移电子数可能为3 NA |
| D.含 NA 个氢氧化铝胶体粒子的胶体中,氢氧化铝的质量大于78 g |
您最近一年使用:0次
三、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
3. 分子式为C7H8的某有机物,它能使酸性高锰酸钾溶液褪色,但不能与溴水反应。该有机物在一定条件下与H2完全加成,其生成物的一氯代物的种类有( )
| A.3种 | B.4种 | C.5种 | D.6种 |
【知识点】 同分异构体的数目的确定解读 苯的同系物
您最近一年使用:0次
2020-08-20更新
|
577次组卷
|
20卷引用:2011届江西省吉安市高三第三次模拟考试(理综)化学部分
(已下线)2011届江西省吉安市高三第三次模拟考试(理综)化学部分(已下线)2013-2014河南省濮阳市高三第二次模拟考试理综化学试卷2014-2015辽宁省沈阳二中高二上学期期末化学试卷2014-2015湖北省孝感高级中学高二下学期期中考试化学试卷(已下线)同步君 选修五 第二章 第二节 芳香烃(已下线)同步君 选修五 第二章 第二节 芳香烃2016-2017学年云南省云天化中学高二上学期期末考试化学(理)试卷四川省成都市双流中学2016-2017学年高二5月月考化学试题高中化学人教版 选修五 第二章 第二节 芳香烃上海外国语大学附中2016-2017学年高二下学期期中考试化学试题湖北省黄冈市黄冈中学高三理科综合化学试题宁夏回族自治区吴忠市吴忠中学2019-2020学年高二下学期期末考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高二下学期开学考试化学试题广东省珠海市2019-2020学年高二下学期期末学业质量检测化学试题(已下线)练习20 芳香烃-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)四川省南充高级中学2021届高三第12次月考理综化学试题(已下线)第33讲 烃和卤代烃(精练)-2022年高考化学一轮复习讲练测安徽省合肥市第八中学2021-2022学年高二下学期实验班开学考化学试题广东省珠海市2020-2021学年高二下学期期末考试化学试题上海市实验学校2022-2023学年高二上学期10月月考有机测试烃化学试题
单选题
|
适中(0.65)
名校
4. 一种利用生物电化学方法脱除水体中NH 的原理如图所示。
的原理如图所示。
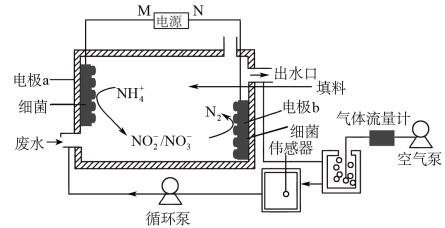
下列说法正确的是
 的原理如图所示。
的原理如图所示。
下列说法正确的是
| A.M为电源的负极,N为电源的正极 |
| B.装置工作时,电极a周围溶液的pH降低 |
C.装置内工作温度越高,NH 的脱除率一定越大 的脱除率一定越大 |
D.电极b上发生的反应之一为2NO +8H++8e-=N2↑+4H2O +8H++8e-=N2↑+4H2O |
您最近一年使用:0次
2020-08-23更新
|
295次组卷
|
4卷引用:本册综合检测(一)——2020-2021学年高二化学选修四同步单元AB卷(人教版)
(已下线)本册综合检测(一)——2020-2021学年高二化学选修四同步单元AB卷(人教版)河南省实验中学2021届高三上学期期中考试化学试题四川省南充高级中学2021届高三第12次月考理综化学试题四川省泸县第一中学2022届高三三诊模拟考试理科综合化学试题
单选题
|
适中(0.65)
名校
5. 下列实验步骤、现象及结论均正确的是
| 选项 | 实验步骤 | 现象 | 结论 |
| A | 在生锈的铁制品表面滴加适量的浓氯化铵溶液 | 没有明显现象 | 浓氯化铵溶液与铁锈不反应 |
| B | 亚硫酸滴入碳酸钠溶液中产生二氧化碳气体,将二氧化碳通入次氯酸钙中 | 产生白色沉淀 | 亚硫酸酸性强于次氯酸 |
| C | 向 AgNO3 溶液中加入等浓度等体积的 NaCl 溶液和 KI 溶液 | 先生成黄色沉淀 | Ksp(AgI)>Ksp(AgCl) |
| D | 将某气体通入溴的四氯化碳溶液中 | 溶液褪色 | 该气体一定为乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. X、Y、Z、W、R为原子序数依次增大的短周期主族元素。其中 X 元素原子的最外层电子数是其周期数的2倍;Y、W为同族元素,且W的原子序数是Y的2 倍;Z单质既能与盐酸反应,又能与NaOH溶液反应。下列说法正确的是
| A.Z与W形成的化合物难溶于水 | B.Z、W、R的简单离子半径:Z>W>R |
| C.X、Y 单质均有同素异形体 | D.W、R的氧化物对应的水化物的酸性:R>W |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
7. 某温度下,向一定体积 0.1 mol·L-1 的 NaOH 溶液中逐滴加入等浓度的醋酸,溶液中的 pH 与 pOH [pOH =-lgc(OH-)] 的变化关系如图所示。下列说法正确的是
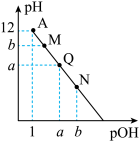

| A.该温度下Kw = 1.0×10-14 |
| B.Q点溶液中,c(CH3COO-) + c(CH3COOH) = c(Na+) |
C.加水稀释 N 点溶液, 的值变大 的值变大 |
| D.溶液从 M 点到 N 点之间,Q 点溶液中水的电离程度最大 |
【知识点】 弱电解质的电离平衡 电离平衡常数及影响因素解读
您最近一年使用:0次
2021-04-13更新
|
345次组卷
|
2卷引用:四川省南充高级中学2021届高三第12次月考理综化学试题
四、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
8. 过一硫酸氢钾(KHSO5)因其可提供超强效的非氯氧化电势和微生物效能,而被广泛应用于工业生产和消毒领域,它还具有储存稳定性好、使用安全方便等特点。实验室以过氧化氢、浓硫酸和碳酸钾为原料制备过一硫酸氢钾。
Ⅰ.过一硫酸(H2SO5)的合成
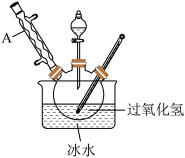
实验室用如图所示实验装置,以过氧化氢和浓硫酸为原料合成过一硫酸。
(1)仪器 A 的名称___________ ;图中采取冰水冷却的目的是___________ 。
(2)三颈烧瓶中发生的化学方程式是___________ 。
Ⅱ.过一硫酸氢钾(KHSO5)的合成
制备好的过一硫酸在适当的搅拌下加入一定量的无水碳酸钾,控制加入速度使反应温度在一定范围内,待碳酸钾完全溶解后继续恒温搅拌 20 min 使之反应完全。
(3)恒温搅拌过程必须在开放的仪器中进行,原因是___________ 。
(4)反应完全后,把所得溶液置于冰箱冷却10 h 后进行___________ ,洗涤、干燥即得到产品。
Ⅲ. 产品中活性氧含量[M(O)×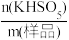 ×100%]的测定
×100%]的测定
(5)取 a g 产品放入盛放有 75 mL 蒸馏水、15 mL 10% 的硫酸和 10 mL 25% 的碘化钾溶液的碘量瓶中,摇晃碘量瓶至试样完全溶解,液封放在阴凉处 5 min,加入___________ 作指示剂,用c mol·L-1 的硫代硫酸钠标准溶液进行滴定至溶液___________ ,即到达滴定终点,此时消耗的硫代硫酸钠标准溶液的体积为 V mL。则产品的活性氧含量为___________ (已知:①2HSO =SO
=SO +H2SO4+O2↑;②4I
+H2SO4+O2↑;②4I +4H
+4H +O2 =2I2+2H2O;③I2+2S2O
+O2 =2I2+2H2O;③I2+2S2O =S4O
=S4O +2I
+2I )。
)。
Ⅰ.过一硫酸(H2SO5)的合成

实验室用如图所示实验装置,以过氧化氢和浓硫酸为原料合成过一硫酸。
(1)仪器 A 的名称
(2)三颈烧瓶中发生的化学方程式是
Ⅱ.过一硫酸氢钾(KHSO5)的合成
制备好的过一硫酸在适当的搅拌下加入一定量的无水碳酸钾,控制加入速度使反应温度在一定范围内,待碳酸钾完全溶解后继续恒温搅拌 20 min 使之反应完全。
(3)恒温搅拌过程必须在开放的仪器中进行,原因是
(4)反应完全后,把所得溶液置于冰箱冷却10 h 后进行
Ⅲ. 产品中活性氧含量[M(O)×
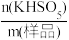 ×100%]的测定
×100%]的测定(5)取 a g 产品放入盛放有 75 mL 蒸馏水、15 mL 10% 的硫酸和 10 mL 25% 的碘化钾溶液的碘量瓶中,摇晃碘量瓶至试样完全溶解,液封放在阴凉处 5 min,加入
 =SO
=SO +H2SO4+O2↑;②4I
+H2SO4+O2↑;②4I +4H
+4H +O2 =2I2+2H2O;③I2+2S2O
+O2 =2I2+2H2O;③I2+2S2O =S4O
=S4O +2I
+2I )。
)。
【知识点】 酸碱中和滴定原理的应用解读 物质含量的测定 物质制备的探究解读
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
名校
解题方法
9. K2FeO4易溶于水,难溶于有机溶剂,是一种极强的氧化剂,常用于水的处理,其工业制法如图所示:

(1)K2FeO4的化学名称是___________ ,其中铁元素的化合价为___________ 。
(2)在氧化反应操作过程中加入试剂的先后顺序:在NaOH溶液中先___________ ,再___________ 。总反应的离子方程式为___________ ,从粗品沉淀过程来看,加入饱和KOH溶液的目的是___________ 。
(3)工业上还可以通过电解浓 KOH 溶液制备 K2FeO4,装置如图所示:

①阳极的电极反应式为___________ 。
②Ⅰ室左侧出口流出的物质是___________ ,形成的原因是___________ 。
③与第一种流程相比较,电解法得到产品的优点是___________ (写出一点即可)。

(1)K2FeO4的化学名称是
(2)在氧化反应操作过程中加入试剂的先后顺序:在NaOH溶液中先
(3)工业上还可以通过电解浓 KOH 溶液制备 K2FeO4,装置如图所示:

①阳极的电极反应式为
②Ⅰ室左侧出口流出的物质是
③与第一种流程相比较,电解法得到产品的优点是
您最近一年使用:0次
10. 据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)用CH4和催化剂还原NO2可以消除氮氧化物的污染,若用标准状况下4.48 L CH4还原 NO2至N2,则整个过程中转移电子总数为___________ (阿伏加德罗常数的数值用NA表示)。
(2)利用CO2和CH4重整可制合成气(主要成分为CO、H2),重整过程中部分反应的热化学方程式如下:
①CH4(g)=C(s)+ 2H2(g) ΔH=+75.0 kJ·mol-1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.0 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.0 kJ·mol-1
③CO(g)+H2(g) C(s)+H2O(g) ΔH=-131.0 kJ·mol-1
C(s)+H2O(g) ΔH=-131.0 kJ·mol-1
则反应CO2(g)+CH4(g) 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=___________ 。
(3)一定条件下Pd—Mg/SiO2催化剂可使CO2 “甲烷化”,从而“变废为宝”,其反应机理如图所示,该反应的化学方程式为___________ ,反应过程中碳元素的化合价为-2价的中间体是___________ 。

(4)利用水蒸气重整也是提高甲烷利用率的重要方式,重整过程中部分反应如下:
①CH4(g)+H2O(g) CO(g)+3H2 (g);
CO(g)+3H2 (g);
②CO(g)+H2O(g) CO2 (g)+H2 (g)。
CO2 (g)+H2 (g)。
一定条件下,将1 mol CH4 (g)与2 mol H2O (g)置于密闭容器中发生上述两个反应,达到平衡时测得H2 (g)的物质的量为2.2 mol,且CH4 (g)与CO2 (g)的体积比为1:1,则反应②的平衡常数K=___________ 。
(5)甲烷碱性燃料电池装置如图所示(开始时两边溶液质量相等),用电器为惰性电极电解装置,其原理如下:通电后,CN-被氧化后转化为无害气体,废水得以净化。
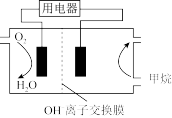
①负极的电极反应为___________ 。
②当除去1mol CN-时,燃料电池两边溶液的质量差为___________ g。
(1)用CH4和催化剂还原NO2可以消除氮氧化物的污染,若用标准状况下4.48 L CH4还原 NO2至N2,则整个过程中转移电子总数为
(2)利用CO2和CH4重整可制合成气(主要成分为CO、H2),重整过程中部分反应的热化学方程式如下:
①CH4(g)=C(s)+ 2H2(g) ΔH=+75.0 kJ·mol-1
②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.0 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.0 kJ·mol-1③CO(g)+H2(g)
 C(s)+H2O(g) ΔH=-131.0 kJ·mol-1
C(s)+H2O(g) ΔH=-131.0 kJ·mol-1则反应CO2(g)+CH4(g)
 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=(3)一定条件下Pd—Mg/SiO2催化剂可使CO2 “甲烷化”,从而“变废为宝”,其反应机理如图所示,该反应的化学方程式为

(4)利用水蒸气重整也是提高甲烷利用率的重要方式,重整过程中部分反应如下:
①CH4(g)+H2O(g)
 CO(g)+3H2 (g);
CO(g)+3H2 (g);②CO(g)+H2O(g)
 CO2 (g)+H2 (g)。
CO2 (g)+H2 (g)。一定条件下,将1 mol CH4 (g)与2 mol H2O (g)置于密闭容器中发生上述两个反应,达到平衡时测得H2 (g)的物质的量为2.2 mol,且CH4 (g)与CO2 (g)的体积比为1:1,则反应②的平衡常数K=
(5)甲烷碱性燃料电池装置如图所示(开始时两边溶液质量相等),用电器为惰性电极电解装置,其原理如下:通电后,CN-被氧化后转化为无害气体,废水得以净化。

①负极的电极反应为
②当除去1mol CN-时,燃料电池两边溶液的质量差为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
名校
解题方法
11. 钒、钛在工业上用途广泛,钒钛磁铁矿是钒、钛的主要来源。
(1)基态钒(V)原子的核外电子排布式为___________ ,其最高化合价为___________ ,与其同周期且未成对电子数相同的元素符号为___________ 。
(2)硫酸工业中,SO2氧化为SO3常用V2O5作催化剂。SO3中S原子的杂化方式为___________ 。SO2易溶于水的原因为___________ 。
(3)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
则X的配离子为___________ ,Y的配体为___________ 。
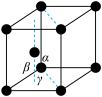
(4)金属钛的晶胞结构如图所示,已知晶胞参数α=β=90°,γ=120°,则钛原子的配位数为___________ 。设 Ti 的原子半径为 r pm,相对原子质量为M,阿伏加德罗常数的值用 NA表示,则金属钛的密度是___________ g·cm-3.(不要求计算,列出算式即可)
(1)基态钒(V)原子的核外电子排布式为
(2)硫酸工业中,SO2氧化为SO3常用V2O5作催化剂。SO3中S原子的杂化方式为
(3)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
| 原溶液 | X溶液 | X溶液 | Y溶液 | Y溶液 |
| 所加试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
| 现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
则X的配离子为
(4)金属钛的晶胞结构如图所示,已知晶胞参数α=β=90°,γ=120°,则钛原子的配位数为

您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
名校
解题方法
12. 以 A 和常见氨基酸 H 为原料制备抗糖尿病药物那格列萘的一种合成路线如下:
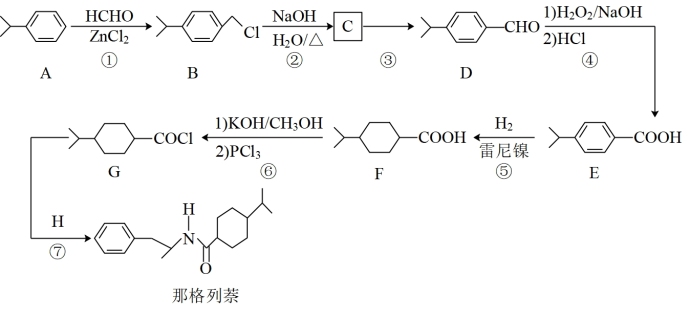
回答下列问题:
(1)A 的化学名称是___________ 。
(2)反应②、反应⑤的反应类型分别是___________ 、___________ 。
(3)反应③的化学方程式为___________ 。
(4)H 的结构简式为___________ ,那格列萘中含氧官能团名称为___________ 。
(5)X 与 E 互为同分异构体,且属于芳香酯类化合物。X 的核磁共振氢谱中有 4 组峰,其峰面积比为6:3:2:1.写出2种符合上述条件的X 的结构简式:___________ 、___________ 。
(6)设计由甲苯和环己甲酸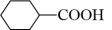 为起始原料制备环己甲酸对甲苄酯
为起始原料制备环己甲酸对甲苄酯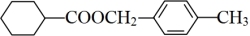 的合成路线:
的合成路线:___________ (无机试剂任用)。

回答下列问题:
(1)A 的化学名称是
(2)反应②、反应⑤的反应类型分别是
(3)反应③的化学方程式为
(4)H 的结构简式为
(5)X 与 E 互为同分异构体,且属于芳香酯类化合物。X 的核磁共振氢谱中有 4 组峰,其峰面积比为6:3:2:1.写出2种符合上述条件的X 的结构简式:
(6)设计由甲苯和环己甲酸
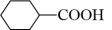 为起始原料制备环己甲酸对甲苄酯
为起始原料制备环己甲酸对甲苄酯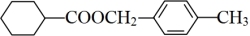 的合成路线:
的合成路线:
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:有机化学基础、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用
试卷题型(共 12题)
题型
数量
单选题
6
多选题
1
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 加成反应 淀粉和纤维素组成与结构 蛋白质组成结构 | |
| 3 | 0.65 | 同分异构体的数目的确定 苯的同系物 | |
| 4 | 0.65 | 电解池电极反应式及化学方程式的书写与判断 电解原理的应用实验 | |
| 5 | 0.65 | 盐类水解在生活、生产中的应用 溶度积规则及其应用 单烯烃的加成反应 | |
| 6 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | |
| 7 | 0.65 | 弱电解质的电离平衡 电离平衡常数及影响因素 | |
| 二、多选题 | |||
| 2 | 0.65 | 阿伏加德罗常数的应用 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 三、解答题 | |||
| 8 | 0.65 | 酸碱中和滴定原理的应用 物质含量的测定 物质制备的探究 | 实验探究题 |
| 9 | 0.65 | 氧化还原反应方程式的配平 高铁酸钠 电解池电解基本判断 电解池电极反应式及化学方程式的书写与判断 | 工业流程题 |
| 10 | 0.65 | 化学反应原理综合考查 盖斯定律及其有关计算 电解池电极反应式及化学方程式的书写与判断 电解池有关计算 | 原理综合题 |
| 11 | 0.65 | 利用杂化轨道理论判断化学键杂化类型 相似相溶原理及应用 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 根据要求书写同分异构体 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |



