若在一定条件下,容积恒定的反应室中充入amolCO与2amolH2,在催化剂作用下发生反应CO(g)+2H2(g) CH3OH(g),下列措施一定使
CH3OH(g),下列措施一定使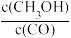 增大的是()
增大的是()
 CH3OH(g),下列措施一定使
CH3OH(g),下列措施一定使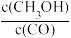 增大的是()
增大的是()| A.升高温度 | B.充入Ar(g)使体系的总压增大 |
| C.恒温恒容再充入H2 | D.恒温恒容再充入amolCO和2amolH2 |
更新时间:2020-04-10 15:46:44
|
相似题推荐
【推荐1】下列关于各图像的解释或得出的结论不正确的是


A.由甲图可知,反应在 时刻一定是使用了催化剂 时刻一定是使用了催化剂 |
| B.由乙图可知,反应在m点可能达到了平衡状态 |
C.由丙图可知,反应过程中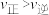 的点可能是C点 的点可能是C点 |
D.由丁图可知,交点A表示反应一定处于平衡状态,此时 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】已知反应N2(g)+3H2(g)⇌2NH3(g) ΔH=﹣92.2kJ·mol﹣1。当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示:
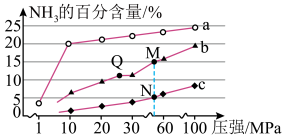
下列说法正确的是

下列说法正确的是
| A.若反应器中充入1mol N2和3mol H2,则反应达平衡时将释放92.2kJ热量 |
| B.从Q到M,平衡向右移动 |
| C.M、N、Q达到平衡所需时间关系为tN >tQ>tM |
| D.图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q)>K(N) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】天然气的主要成分为CH4,一般还含有C2H6等烃类,重要的燃料和化工原料。乙烷在一定条件可发生如下反应:C2H6(g)→C2H4(g)+H2(g) ∆H,相关物质的燃烧热数据如下表所示:
下列说法不正确的是
| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热∆H/(kJ/mol) | -1560 | -1411 | -286 |
| A.燃烧热指在101kpa时,1mol纯物质完全燃烧生成指定产物时所放出的热量 |
| B.∆H=-137kJ/mol |
| C.提高该反应平衡转化率的方法有升高温度、减小压强 |
D.容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡常数Kp=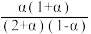 ×p(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数) ×p(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数) |
您最近一年使用:0次
【推荐1】相同温度下,容积相同的甲,乙两个恒容密闭容器均发生如下反应:N2+3H2 2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
 2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化/kJ | ||
| N2 | 3H2 | NH3 | ||
| 甲 | 1 | 3 | 0 | 放出热量:Q1 |
| 乙 | 0.9 | 2.7 | 0.2 | 放出热量:Q2 |
| A.Q2<Q1=92.4 | B.容器甲先达平衡 |
| C.两容器中反应的平衡常数相等 | D.达到平衡时NH3的体积分数:甲=乙 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应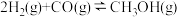 达到平衡,下列说法正确的是
达到平衡,下列说法正确的是
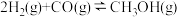 达到平衡,下列说法正确的是
达到平衡,下列说法正确的是| 容器 | 温度/K | 物质的起始浓度/(mol·L-1) | 物质的平衡浓度/(mol·L-1) | ||
| c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
| I | 400 | 0.20 | 0.10 | 0 | 0.080 |
| II | 400 | 0.40 | 0.20 | 0 | |
| III | 500 | 0 | 0 | 0.10 | 0.025 |
| A.该反应的正反应为吸热反应 |
| B.达到平衡时,容器I中反应物转化率比容器II中的小 |
| C.达到平衡时,容器III中的正反应速率比容器I中的大 |
| D.达到平衡时,容器II中c(H2)大于容器III中c(H2)的两倍 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】一定温度下,往2 L的密闭容器中加入2 mol X和3 mol Y,发生如下反应:2X(g)+3Y(g) 4Z(g)+W(g) ΔH<0,反应10 min后达到平衡,恢复至原温度,此时W的浓度为0.25 mol·L-1。下列说法正确的是
4Z(g)+W(g) ΔH<0,反应10 min后达到平衡,恢复至原温度,此时W的浓度为0.25 mol·L-1。下列说法正确的是
 4Z(g)+W(g) ΔH<0,反应10 min后达到平衡,恢复至原温度,此时W的浓度为0.25 mol·L-1。下列说法正确的是
4Z(g)+W(g) ΔH<0,反应10 min后达到平衡,恢复至原温度,此时W的浓度为0.25 mol·L-1。下列说法正确的是| A.前5 min内,反应的平均速率v(Z)=0.1 mol·L-1·min-1 |
| B.其他条件不变时,将反应容器的体积缩小一半,W的平衡浓度为0.5 mol·L-1 |
| C.保持温度不变,10 min后向容器中再加入1 mol W,重新达到平衡时,X的转化率大于50% |
| D.其他条件不变,升高温度,反应达到平衡时Y的浓度大于0.75 mol·L-1 |
您最近一年使用:0次



