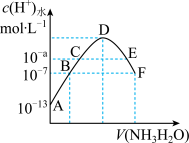
常温下,向20mL0.05mol•L-1的某稀酸H2B溶液中滴入0.1mol•L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是

| A.NaHB溶液中一定含有H2B分子 |
| B.A、B、C三点溶液的pH逐渐减小,D、E、F三点溶液的pH逐渐增大 |
| C.E溶液中离子浓度大小关系为c(NH4+)>c(B2-)>c(H+)>c(OH-) |
| D.B点溶液pH=7 |
2020·河北保定·二模 查看更多[2]
更新时间:2020-05-24 22:05:16
|
相似题推荐
单选题
|
较难
(0.4)
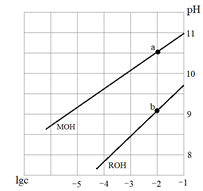
【推荐1】25℃时,用0.2mol•L-1的盐酸分别滴定20mL0.2mol•L-1的氨水和MOH碱溶液(碱性:NH3•H2O大于MOH),溶液的pOH[pOH=-lgc(OH-)]与lg 或lg
或lg 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 或lg
或lg 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是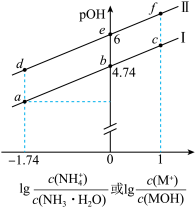
| A.曲线I对应的是滴定NH3•H2O的曲线 |
| B.a点对应的溶液pH=11 |
| C.b、e点溶液中水的电离程度:b>e |
| D.b、e点溶液中的c(Cl-)大小:b<e |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下向20mL0.10mol/L的氨水中滴加未知浓度的稀H2SO4,测得混合溶液的电导率、pH随加入稀硫酸体积的变化如下图所示。已知电导率是用来描述物质中电荷流动难易程度的参数。溶液中离子浓度越大,电导率越大。下列说法不正确的是


A.稀H2SO4的物质的量浓度为0.10 |
| B.x=11 |
C.a点时溶液中存在: |
| D.a、b、c三点对应水的电离程度:b>a>c |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,二元弱酸 溶液中含磷物种的浓度之和为0.1 mol⋅L
溶液中含磷物种的浓度之和为0.1 mol⋅L ,溶液中各含磷物种的pc-pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(
,溶液中各含磷物种的pc-pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(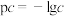 ),pOH表示
),pOH表示 的浓度的负对数
的浓度的负对数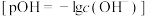 。下列有关说法正确的是
。下列有关说法正确的是
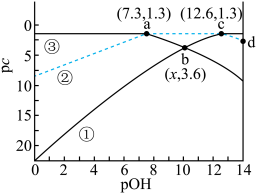
A.b点时,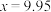 |
B.曲线②表示 随pOH的变化 随pOH的变化 |
C.d点溶液中: |
D. 溶液呈碱性是因为 溶液呈碱性是因为 离子的水解程度大于其电离程度 离子的水解程度大于其电离程度 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数 (X)=
(X)=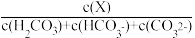 与pH的关系如图所示:
与pH的关系如图所示:
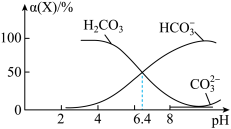
下列说法正确的是
 (X)=
(X)=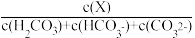 与pH的关系如图所示:
与pH的关系如图所示:
下列说法正确的是
A.反应HCO3- H++CO32-的lgK=-6.4 H++CO32-的lgK=-6.4 |
| B.pH═8的溶液中:c(Na+)>c(HCO3-) |
| C.NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-) |
| D.向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,向含有等物质的量浓度的 、NaOH混合物中滴加稀盐酸至过量,其中主要含碳物质
、NaOH混合物中滴加稀盐酸至过量,其中主要含碳物质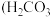 、
、 、
、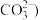 的分布分数
的分布分数 平衡时某物质的浓度占各物质浓度之和的分数
平衡时某物质的浓度占各物质浓度之和的分数 与滴加盐酸体积的关系如图所示
与滴加盐酸体积的关系如图所示 忽略滴加过程
忽略滴加过程 气体的逸出
气体的逸出 。下列说法不正确的是
。下列说法不正确的是

 、NaOH混合物中滴加稀盐酸至过量,其中主要含碳物质
、NaOH混合物中滴加稀盐酸至过量,其中主要含碳物质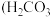 、
、 、
、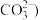 的分布分数
的分布分数 平衡时某物质的浓度占各物质浓度之和的分数
平衡时某物质的浓度占各物质浓度之和的分数 与滴加盐酸体积的关系如图所示
与滴加盐酸体积的关系如图所示 忽略滴加过程
忽略滴加过程 气体的逸出
气体的逸出 。下列说法不正确的是
。下列说法不正确的是
A.曲线B表示 |
B.在滴加盐酸过程中溶液中 与含碳各物质浓度的大小关系: 与含碳各物质浓度的大小关系: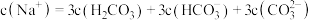 |
C.X、Y为曲线的两交叉点,若能知道X点处的pH就可以计算出 的 的 的值 的值 |
D.溶液中X、Y两点水电离出的 : : |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下,向10 mL0.01 mol/LNaCN溶液中逐滴加入0.01 mol/L的盐酸,溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如图甲所示,pH变化曲线如图乙所示。下列说法不正确的是
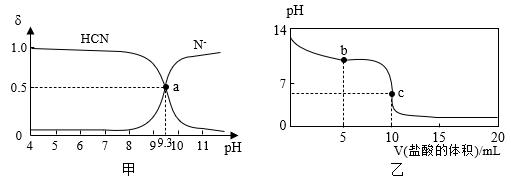

| A.Ka(HCN)=10-9.3 |
| B.图乙中c点的溶液:c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(CN-) |
| C.图乙中b点的溶液: c(CN-)>c(HCN) |
| D.图甲中a点,滴入的盐酸的体积小于5 mL |
您最近一年使用:0次

 增大
增大

