在某温度时,将n mol/L醋酸滴入10mL 1.0mo/L氢氧化钠溶液中,溶液pH和温度随加入醋酸体积变化曲线如图所示。下列有关说法正确的是


| A.n=1.0 |
| B.水的电离程度:c>b>a |
| C.25℃时,CH3COONa的水解常数为(n-1)×10-7 |
| D.b点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
更新时间:2020-06-17 12:09:00
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】常温下,分别向两个盛 盐酸的烧杯中匀速滴加
盐酸的烧杯中匀速滴加 蒸馏水、
蒸馏水、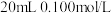 醋酸铵溶液,滴加过程用
醋酸铵溶液,滴加过程用 传感器测得溶液
传感器测得溶液 随时间变化如下图所示。已知:常温下醋酸铵溶液
随时间变化如下图所示。已知:常温下醋酸铵溶液 。下列说法
。下列说法错误 的是
 盐酸的烧杯中匀速滴加
盐酸的烧杯中匀速滴加 蒸馏水、
蒸馏水、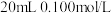 醋酸铵溶液,滴加过程用
醋酸铵溶液,滴加过程用 传感器测得溶液
传感器测得溶液 随时间变化如下图所示。已知:常温下醋酸铵溶液
随时间变化如下图所示。已知:常温下醋酸铵溶液 。下列说法
。下列说法
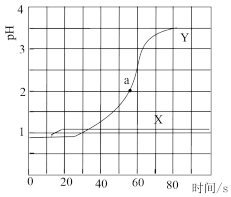
A.常温下,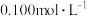 盐酸中水电离的 盐酸中水电离的 |
B.曲线Y表示盐酸中加水稀释的 变化 变化 |
C.a点对应的溶液中 |
D.盐酸中加入醋酸铵 变化主要是因为 变化主要是因为 与 与 结合成了 结合成了 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃时,下列有关电解质溶液说法正确的是( )
| A.1.0mol/L NH4HCO3溶液pH=8.0,由此可知Ka1(H2CO3)>Kb(NH3·H2O)>Ka2(H2CO3) |
B.向氨水中加入NH4C1固体,溶液中 增大 增大 |
| C.向CH3COONa溶液中滴加硫酸至中性时,c(SO42ˉ)<c(CH3COOH) |
D.下图中曲线可以表示100mL 0.01 mol/LCH3COOH溶液中逐滴加入0.02mol/L NaOH溶液的pH变化情况(溶液体积变化忽略不计)。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下向某浓度的氯水中逐滴滴入 溶液,无气体逸出,溶液pH变化如图所示,下列错误的是
溶液,无气体逸出,溶液pH变化如图所示,下列错误的是

 溶液,无气体逸出,溶液pH变化如图所示,下列错误的是
溶液,无气体逸出,溶液pH变化如图所示,下列错误的是
A.a点: |
B.b点: |
C.c点: |
D.d点: |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在50 mL 0.1mol/L Na2S 溶液中逐滴加入50 mL 0.1mol/L KHSO4溶液,所得溶液中粒子浓度关系正确的是
| A.c(SO42-)= c(HS-)= c(K+)>c(OH-)= c(H+) |
| B.c(Na+)> c(K+)> c(S2-)> c(H+)> c(OH-) |
| C.c(Na+)= c(S2-)+ c(HS-)+ c(H2S)+ c(SO42-) |
| D.c(K+)+ c(Na+)+ c(H+)= c(SO42-)+ c(S2-)+ c(HS-)+ c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】变化观念与平衡思想分析一定温度下Mg2+在不同pH的Na2CO3体系中的可能产物。
下列说法不正确的是

图2中曲线I的离子浓度关系符合c(Mg2+)•c2(OH )=Ksp[Mg(OH)2];曲线II的离子浓度关系符合c(Mg2+)•c(CO
)=Ksp[Mg(OH)2];曲线II的离子浓度关系符合c(Mg2+)•c(CO )=Ksp(MgCO3)。
)=Ksp(MgCO3)。
下列说法不正确的是
A.饱和NaHCO3溶液中c(CO )<c(H2CO3) )<c(H2CO3) |
| B.初始状态pH=11、lg[c(Mg2+)]=-6,无沉淀生成 |
C.初始状态pH=9、lg[c(Mg2+)]=-2,平衡后溶液中存在c(H2CO3)+c(HCO )+c(CO )+c(CO )=0.1mol•L-1 )=0.1mol•L-1 |
D.初始状态pH=8、lg[c(Mg2+)]=-1,发生反应:Mg2++2HCO =MgCO3↓+CO2↑+H2O =MgCO3↓+CO2↑+H2O |
您最近一年使用:0次

 0.1
0.1
 溶液中逐滴加入0.1
溶液中逐滴加入0.1 溶液,溶液中由水电离的
溶液,溶液中由水电离的 与所加
与所加





