常温下,向20mL0.2mol·L-1H2X溶液中滴加0.2mol·L-1NaOH溶液,在不同pH环境下不同形态的粒子组成分数如图所示,下列说法正确的是
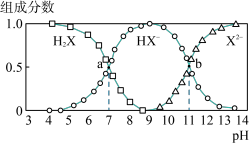

| A.水的电离程度:b点小于点a |
| B.将等物质的量的NaHX、Na2X溶于水中,所得溶液pH恰好为11 |
| C.常温下的Ka(HY)=1.1×10-10,将少量H2X溶液加入到足量NaY溶液中,发生的反应为:H2X+Y-=HY+HX- |
| D.常温下,反应X2-+H2O⇌HX-+OH-的平衡常数对数值1gK=-11 |
更新时间:2020-06-22 00:18:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述正确的是
A.50℃时, 的纯碱溶液中, 的纯碱溶液中,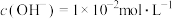 |
B.相同条件下,浓度均为 的盐酸与 的盐酸与 溶液,水的电离程度相同 溶液,水的电离程度相同 |
C.将水加热到100℃,测得其 ,则液体呈酸性 ,则液体呈酸性 |
D.常温时, 的 的 溶液与 溶液与 的 的 溶液等体积混合后 溶液等体积混合后 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积VHCl的变化关系如图所示。[比如B+的分布系数: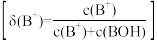
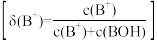

| A.滴定时,可以选择酚酞作指示剂 |
| B.BOH的电离常数Kb=1.0×10−6 |
| C.滴定过程中,水的电离程度:n<m<p |
| D.p点溶液中,粒子浓度大小为c(Cl-)>c(B+)>c(BOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用少量锌粒与0.1 mol·L-1的稀硫酸混合制备氢气时,反应速率太慢,为加快反应速率可以使用如下方法中的
①加H2O ②加KCl溶液 ③加足量锌粉 ④加少量2 mol·L-1盐酸 ⑤加少量CuCl2溶液 ⑥升高温度 ⑦加入CH3COONa溶液
①加H2O ②加KCl溶液 ③加足量锌粉 ④加少量2 mol·L-1盐酸 ⑤加少量CuCl2溶液 ⑥升高温度 ⑦加入CH3COONa溶液
| A.①③④ | B.②③④⑤⑥⑦ | C.③④⑤⑥ | D.①③④⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列微粒能通过水解产生H+的是
| A.CO32- | B.HCO3- | C.Na+ | D.NH4+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】常温下,向10 mL 0.01 mol/L NaCN溶液中逐滴加入0. 01 mol/L的盐酸,溶液中CN- 、 HCN浓度所占分数(δ)随pH变化的关系如图甲所示,pH变化曲线如图乙所示。下列说法正确的是
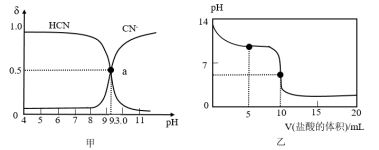

| A.图甲中a点,滴入的盐酸的体积为5 mL |
| B.HCN的电离常数Ka的数量级为10-9 |
| C.图乙中b点的溶液:c(CN-)>c(HCN) |
| D.图乙中c点的溶液:c(Na+)+c(Cl-)=2c(HCN)+2c(CN-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
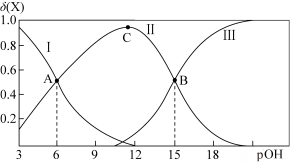
【推荐1】已知联氨(N2H4)为二元碱,25℃时向联氨水溶液中逐滴滴加盐酸溶液,混合溶液中的微粒的物质的量分数随 pOH[pOH=-lgc(OH-)]变化的关系如图所示。已知联氨的两步电离分别为: ,
, 下列叙述正确的是
下列叙述正确的是
 ,
, 下列叙述正确的是
下列叙述正确的是
| A.当N2H4和HCl按1:1反应时,pH>pOH |
B.当pOH=15时,3c(N2H )<c(Cl-) )<c(Cl-) |
C.pH=6时,c(N2H4)=c(N2H ) ) |
| D.25℃时,2.4mol·L-1的N2H6Cl2溶液的pOH为13.7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
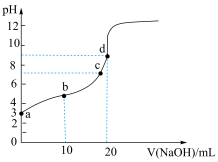
【推荐2】常温下,用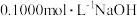 溶液滴定20.00mL
溶液滴定20.00mL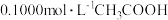 溶液过程中的pH变化曲线如图所示,下列说法错误的是
溶液过程中的pH变化曲线如图所示,下列说法错误的是
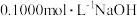 溶液滴定20.00mL
溶液滴定20.00mL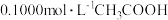 溶液过程中的pH变化曲线如图所示,下列说法错误的是
溶液过程中的pH变化曲线如图所示,下列说法错误的是
| A.可选用酚酞作指示剂 |
B.水的电离程度: |
C.醋酸电离常数的数量级为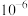 |
D.b点溶液中: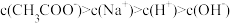 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,用0.1000mol·L-1的盐酸采用“双指示剂法"滴定25.00mL0.1000mol·L-1纯碱溶液,滴定曲线如图所示。下列说法正确的是( )


| A.开始滴定到终点①过程应采用甲基橙作指示剂 |
| B.由①到②的过程中会出现c(Na+)>2c(CO32-)+c (HCO3-) |
| C.滴定终点①处,水电离出的氢离子浓度约为10-8.7mol·L-1 |
| D.滴定过程中含碳微粒的总浓度始终保持0.1000mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关电解质溶液的说法正确的是
| A.向盐酸中加入氨水至中性,溶液中c(NH4+)/c(Cl-)<1 |
| B.在蒸馏水中滴加浓H2SO4,Kw不变 |
| C.向0.1mol/L CH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)增大 |
| D.将CH3COONa溶液从20℃升温至30℃,溶液中c(CH3COO-)/c(CH3COOH).c(OH-)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
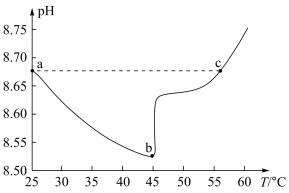
【推荐2】如图为某实验测得 溶液在升温过程中(不考虑水挥发)的
溶液在升温过程中(不考虑水挥发)的 变化曲线。下列说法正确的是
变化曲线。下列说法正确的是
 溶液在升温过程中(不考虑水挥发)的
溶液在升温过程中(不考虑水挥发)的 变化曲线。下列说法正确的是
变化曲线。下列说法正确的是
A.a点溶液的 等于c点溶液的 等于c点溶液的 |
B.a点时,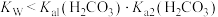 |
C.b点溶液中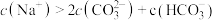 |
D.ab段,pH减小说明升温促进了 的电离,同时抑制了 的电离,同时抑制了 的水解 的水解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】室温下,通过下列实验探究NaHC2O4(Kh为NaHC2O4水解平衡常数、Ka1为H2C2O4电离平衡常数)溶液的性质。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用试纸测定0.1mol•L-1NaHC2O4溶液的pH,测得约为5.5 |
| 2 | 向含0.1molNaHC2O4稀溶液中加入0.05molBa(OH)2,产生沉淀 |
| 3 | 向0.1mol•L-1NaHC2O4溶液中通入过量HCl,无现象 |
| 4 | 向0.1mol•L-1NaHC2O4溶液中通入一定量NH3,测得溶液pH=7 |
| A.实验1的溶液中:c(OH-)=Kh•Ka1•10-5.5 |
B.实验2反应静置后的上层清液中:c(Na+)>c(C2O )>c(HC2O )>c(HC2O )>c(OH-) )>c(OH-) |
| C.实验3得到的溶液中:c(Na+)>c(Cl-)>c(H2C2O4)>c(H+) |
D.实验4所得的溶液中:c(NH )+c(H2C2O4)=c(C2O )+c(H2C2O4)=c(C2O ) ) |
您最近一年使用:0次

 、Na+
、Na+ 、NO
、NO 、S2-、Br-
、S2-、Br-

