在 100℃时,将 0.40 mol NO2气体充入 2 L 的密闭容器中,发生如下反应:2NO2(g) N2O4(g) ∆H < 0。监测反应获得如下数据:
N2O4(g) ∆H < 0。监测反应获得如下数据:
下列说法正确的是
 N2O4(g) ∆H < 0。监测反应获得如下数据:
N2O4(g) ∆H < 0。监测反应获得如下数据:| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A.0~20 s 内,v(NO2) = 0.005 mol·L-1.s-1 |
| B.若上述反应在 120℃时进行,则反应至 80 s 时,n(N2O4) < 0.08 mol |
| C.若仅将起始时充入 NO2的量增至 0.80 mol,达平衡时 NO2转化率将减少 |
| D.59 s 时,c(NO2)一定大于 0.12 mol·L-1 |
更新时间:2020-07-04 17:17:40
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】一定温度下,10mL0.4mol/LH2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表:( )
下列叙述错误的是(溶液体积变化忽略不计)
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述错误的是(溶液体积变化忽略不计)
| A.反应至6min时,c(H2O2)=0.20mol/L |
| B.反应至6min时,H2O2分解了40% |
| C.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L·min) |
| D.6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L·min) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】利用反应: 可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入
可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入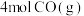 和
和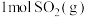 发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
 可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入
可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入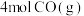 和
和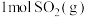 发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
A.容器Ⅰ中CO的体积分数: |
B.容器Ⅱ中 的平衡转化率是80% 的平衡转化率是80% |
C.平衡常数: |
D. 内用 内用 表示容器I中的平均反应速率为 表示容器I中的平均反应速率为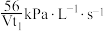 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】近似测定 氧化KI的瞬时速率公式
氧化KI的瞬时速率公式 与速率常数k的实验流程如下:
与速率常数k的实验流程如下:

加入KI后反应如下:① ;②
;②
在 耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:
耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:
下列说法正确的是
 氧化KI的瞬时速率公式
氧化KI的瞬时速率公式 与速率常数k的实验流程如下:
与速率常数k的实验流程如下:
加入KI后反应如下:①
 ;②
;②
在
 耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:
耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:| 实验编号 | 1 | 2 | 3 | 4 | 5 |
 溶液用量/mL 溶液用量/mL | 2.0 | 1.0 | 0.50 | 2.0 | 2.0 |
 溶液用量/mL 溶液用量/mL | 2.0 | 2.0 | 2.0 | 1.0 | 0.50 |
 溶液用量/mL 溶液用量/mL | 0 |  | 1.5 | 1 | 1.5 |
| 反应时间/s | 37 | 68 | 133 | 72 | 139 |
反应速率 | 2.0 | 1.1 | 0.5 | 1.0 | 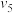 |
反应速率常数 | 3.4 | 3.8 | 3.4 | 3.4 | 4.0 |
A.上表中的速率为 完全消耗后测得的平均速率 完全消耗后测得的平均速率 |
B.由实验可知反应的速率公式为 |
C.表中数据 , ,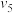 约为0.5 约为0.5 |
| D.实验测得的5组反应速率常数不完全相等,说明浓度对k有影响 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】将4mol A气体和2mol B气体在恒压密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g) ∆H<0;4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L。下列说法中正确的是
2C(g) ∆H<0;4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L。下列说法中正确的是
 2C(g) ∆H<0;4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L。下列说法中正确的是
2C(g) ∆H<0;4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L。下列说法中正确的是| A.此时A的浓度为0.6mol/L |
| B.达平衡后若通入一定量氯气,A的转化率降低 |
| C.4s内用物质B表示的反应速率为0.175mol·L-1·s-1 |
| D.达平衡后若升高温度,C的浓度将增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】快速密闭消解法测定化学耗氧量时常用HgSO4溶液掩蔽水样中的氯离子。一定温度下,HgSO4和NaCl的混合溶液中存在下列平衡关系: 、
、 、
、 、
、 ,平衡常数依次为
,平衡常数依次为 、
、 、
、 、
、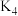 ,下图可表示不同
,下图可表示不同 范围内溶液中主要存在的含汞粒子,
范围内溶液中主要存在的含汞粒子, 。下列说法错误的是
。下列说法错误的是
 、
、 、
、 、
、 ,平衡常数依次为
,平衡常数依次为 、
、 、
、 、
、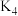 ,下图可表示不同
,下图可表示不同 范围内溶液中主要存在的含汞粒子,
范围内溶液中主要存在的含汞粒子, 。下列说法错误的是
。下列说法错误的是
| A.HgCl2是弱电解质 |
B. 的平衡常数数量级为105 的平衡常数数量级为105 |
C.当pCl=0.9时, |
D.当pCl=6.74时, |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】短周期元素W、X、Y、Z的原子序数依次增加。m、n、p 是由这些元素组成的二元化合物,W2、X2、Z2分别是元素W、X、Z的单质。已知: Ⅰ.一定条件下某密闭容器中可发生反应:aX2+bW2 cm,反应过程中物质的浓度变化如下:
cm,反应过程中物质的浓度变化如下:
Ⅱ.它们可发生如下反应:2m(g)+3Z2(g)=6n(g)+X2(g);4n(g)+Y2(g)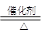 2p(l)+2Z2(g)。 下列说法正确的是
2p(l)+2Z2(g)。 下列说法正确的是
 cm,反应过程中物质的浓度变化如下:
cm,反应过程中物质的浓度变化如下:X2 | W2 | m | |
起始浓度/mol·L-1 | 0.4 | 0.4 | 0 |
平衡浓度/ mol·L-1 | 0.3 | 0.1 | 0.2 |
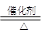 2p(l)+2Z2(g)。 下列说法正确的是
2p(l)+2Z2(g)。 下列说法正确的是| A.原子半径:W<X<Y | B.m、n、p 三种物质均为共价化合物 |
| C.X 的氧化物一定是无色气体 | D.a:b:c=3:1:2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】某温度下,E(g)+F(g) R(g)+N(g)的平衡常数K=4/9。该温度下在A、B、C三个恒容密闭容器中,投入E(g)、F(g),其起始浓度如下表,下列判断正确的是
R(g)+N(g)的平衡常数K=4/9。该温度下在A、B、C三个恒容密闭容器中,投入E(g)、F(g),其起始浓度如下表,下列判断正确的是
 R(g)+N(g)的平衡常数K=4/9。该温度下在A、B、C三个恒容密闭容器中,投入E(g)、F(g),其起始浓度如下表,下列判断正确的是
R(g)+N(g)的平衡常数K=4/9。该温度下在A、B、C三个恒容密闭容器中,投入E(g)、F(g),其起始浓度如下表,下列判断正确的是| 起始浓度 | A | B | C |
| c (E)/ mol•L-1 | 0.010 | 0.020 | 0.020 |
| c (F)/ mol•L-1 | 0.010 | 0.010 | 0.020 |
| A.平衡时,B中E的转化率为大于40% |
| B.平衡时,A中和C中F的转化率均为40% |
| C.平衡时,C中c(R)是A中的2倍,为0.012mol•L-1 |
| D.反应开始时A和C中反应速率相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】—定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g)  N2(g)+2CO2(g)各容器中起始物质的量浓度与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随间变化关系如下图所示。
N2(g)+2CO2(g)各容器中起始物质的量浓度与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随间变化关系如下图所示。

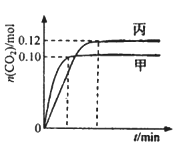
下列说法正确的是
 N2(g)+2CO2(g)各容器中起始物质的量浓度与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随间变化关系如下图所示。
N2(g)+2CO2(g)各容器中起始物质的量浓度与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随间变化关系如下图所示。

下列说法正确的是
| A.该反应的正反应为吸热反应 |
| B.乙容器中反应达到平衡时,N2的转化率小于50% |
| C.达到平衡时,乙容器中的压强一定大于甲容器的2倍 |
| D.丙容器中反应达到平衡后,再充入0.10mol NO和0.10mol CO2,此时v(正)<v(逆) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】在体积为1L的恒容容器中,用CO2和H2合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g) +H2O(g) ∆H。 相同时间内不同的温度下,将1 mol CO2和3 mol H2在反应器中反应,测定CH3OH的产率与温度的关系如图所示。下列说法正确的是


| A.图中X点v(正)>v(逆) |
| B.图中P点所示条件下,延长反应时间不能提高CH3OH的产率 |
| C.该反应的 ∆H>0 |
D.520K下,X点所对应甲醇的产率为50%,则平衡常数K= |
您最近一年使用:0次

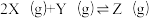
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是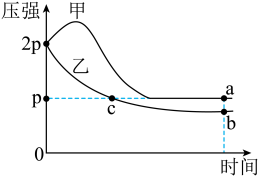
 ,25℃时调节初始浓度为
,25℃时调节初始浓度为 的
的 溶液的
溶液的 ,测定平衡时溶液中
,测定平衡时溶液中 和
和 (单位为
(单位为 ),获得如图所示的曲线。下列说法正确的是
),获得如图所示的曲线。下列说法正确的是
 的平衡转化率为40%
的平衡转化率为40% 固体,溶液由黄色变为橙色
固体,溶液由黄色变为橙色 反应的平衡常数的数量级为
反应的平衡常数的数量级为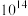
 时.体积均为
时.体积均为 的两个恒容密闭容器中发生可逆反应:
的两个恒容密闭容器中发生可逆反应:
 实验测得反应在起始、达到平衡时的有关数据如表,下列叙述正确的是
实验测得反应在起始、达到平衡时的有关数据如表,下列叙述正确的是


 Q kJ
Q kJ
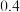

 Q kJ,达到平衡时,两个容器中C的物质的量浓度均为
Q kJ,达到平衡时,两个容器中C的物质的量浓度均为




