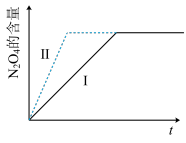
N2O4常用作火箭推进器的燃料。已知反应2NO2(g) N2O4(g) △H<0,不同条件下,N2O4的含量随时间(t)的变化如图,则反应历程从I改变为II所采取的措施可能是
N2O4(g) △H<0,不同条件下,N2O4的含量随时间(t)的变化如图,则反应历程从I改变为II所采取的措施可能是
 N2O4(g) △H<0,不同条件下,N2O4的含量随时间(t)的变化如图,则反应历程从I改变为II所采取的措施可能是
N2O4(g) △H<0,不同条件下,N2O4的含量随时间(t)的变化如图,则反应历程从I改变为II所采取的措施可能是
| A.增大NO2的浓度 | B.升高温度 | C.增大压强 | D.加入催化剂 |
更新时间:2020-08-05 13:58:38
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】20℃时,将10mL 0.1mol/L Na2S2O3溶液和10mL 0.1mol/L的H2SO4溶液混合,2min后溶液中明显出现浑浊。已知温度每升高10℃,化学反应速率增大到原来的2倍,那么50℃,上述反应要看到同样的浑浊,需要的时间是
| A.48s | B.40s | C.20s | D.15s |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列装置或操作不能达到目的的是
A.装置①验证温度对反应2NO2(g)⇌N2O4(g)平衡移动的影响 |
B.装置②验证增大反应物浓度对平衡的影响 |
C.装置③测定中和热 |
D.装置④比较Cu2+、Fe3+对H2O2分解速率的影响 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出 |
B.由 、 、 、 、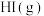 组成的平衡体系加压后颜色变深 组成的平衡体系加压后颜色变深 |
C.盛有 气体的烧瓶(带塞)浸泡在热水中颜色变深 气体的烧瓶(带塞)浸泡在热水中颜色变深 |
D.氯水中存在: ,加入NaOH溶液后溶液颜色变浅 ,加入NaOH溶液后溶液颜色变浅 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
A.密闭容器中发生:H2(g)+Br2(g) 2HBr(g),增大压强红棕色加深 2HBr(g),增大压强红棕色加深 |
| B.向氯水中加入CaCO3固体提高HClO的浓度 |
| C.实验室用排饱和食盐水的方法收集氯气 |
| D.合成氨工业中采用增大压强的方法提高NH3的产量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】有一处于平衡状态的反应:X(g)+3Y(g)  2Z(g)(正反应为放热反应)。为了使平衡向生成Z的方向移动,不能实现的是( )
2Z(g)(正反应为放热反应)。为了使平衡向生成Z的方向移动,不能实现的是( )
 2Z(g)(正反应为放热反应)。为了使平衡向生成Z的方向移动,不能实现的是( )
2Z(g)(正反应为放热反应)。为了使平衡向生成Z的方向移动,不能实现的是( )| A.降温 | B.加压 | C.加催化剂 | D.减少Z |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】体积恒定的密闭容器中发生反应:
 ,其他条件不变时,下列说法正确的是
,其他条件不变时,下列说法正确的是

 ,其他条件不变时,下列说法正确的是
,其他条件不变时,下列说法正确的是| A.升高温度可使平衡正向移动 |
| B.增大压强可使化学平衡常数增大 |
C.移走 可提高CO的平衡转化率 可提高CO的平衡转化率 |
| D.使用催化剂可提高NO的平衡转化率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】研究化学反应中的能量变化具有重要意义。下列说法正确的是
A.已知: 500° C、30MPa 下,N2(g) +3H2(g)  2NH3(g) ΔH= −92.4 kJ∙mol−1将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ 2NH3(g) ΔH= −92.4 kJ∙mol−1将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ |
| B.汽车尾气净化器中的反应为2NO(g) +2CO(g) =N2(g) +2CO2(g) ,该反应在一定条件 下能自发进行,说明该反应的 ΔH>0 |
C.已知反应2NO2(g)  N2O4(g) ΔH <0,升高温度,υ逆增大,υ正减小,平衡逆向移动 N2O4(g) ΔH <0,升高温度,υ逆增大,υ正减小,平衡逆向移动 |
| D.C2H5OH(1) 的燃烧热的热化学方程式为2C2H5OH(1) +6O2(g) =4CO2(g) +6H2O(g) ΔH= −1367.0 kJ∙mol−1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】在恒温恒容下,在一容器充入2molSO2和1molO2发生反应:2SO2(g)+O2(g)⇌2SO3(g),达到平衡后,SO3的体积分数为p%。在恒温恒容下再充入2molSO2和1molO2,再次达到平衡后,SO3的体积分数为
| A.小于p% | B.等于p% | C.大于p% | D.无法判断 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】合成氨工业的主要反应为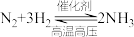 △H<0,在密闭容器中进行。下列说法正确的是
△H<0,在密闭容器中进行。下列说法正确的是
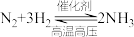 △H<0,在密闭容器中进行。下列说法正确的是
△H<0,在密闭容器中进行。下列说法正确的是| A.其他条件不变,及时分离出NH3,会降低NH3的转化率 |
| B.使用催化剂可使N2的转化率达到100% |
| C.其他条件不变,增大压强不仅能提高转化率,还能缩短到达平衡的时间 |
| D.其他条件不变,温度越高,氨气的产率越高 |
您最近一年使用:0次

 (g)+ I2(g)
(g)+ I2(g)  (g)+2HI(g)
(g)+2HI(g)


