向2L的密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且4个阶段所改变的外界条件均不相同,已知t3——t4阶段为使用催化剂。观察下图,回答下列问题:
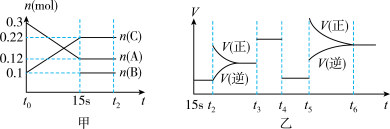
(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为____________ 。
(2)乙图中t2时引起平衡移动的条件是____________ ,t5时引起平衡移动的条件是____________ 。
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是____________ 。
(4)该反应的化学方程式可以表示为:____________ 。
(5)反应开始时加入的B的物质的量为____________ 。

(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为
(2)乙图中t2时引起平衡移动的条件是
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是
(4)该反应的化学方程式可以表示为:
(5)反应开始时加入的B的物质的量为
更新时间:2020-08-22 16:32:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在一定温度、压强下,向密闭容器中投入一定量N2和H2,发生反应:N2+3H2 2NH3 △H<0。
2NH3 △H<0。
(1)反应开始阶段,v(正)______ (填“>”“<”或“=”)v(逆),随后v(正)逐渐______ (填“增大”或“减小”,下同),v(逆)逐渐______ ,反应达到平衡时,v(正)______ (填“>”“<”或“=”)v(逆)。
(2)达到平衡后,若正反应速率用v(N2)表示,逆反应速率用v’(H2)表示,则v(N2)=____ v’(H2)。
(3)下列措施中能加快反应速率并提高氢气的转化率的是______ (填字母)。
A.其他条件不变时,压缩容器体积 B.其他条件不变时,升高反应体系温度
C.使用合适的催化剂 D.保持容器体积不变,充入一定量的氮气
(4)实际生产中往往需要将温度控制在一个合适的范围,分析温度不宜过高也不宜过低的原因是______________________________________ 。
(5)写出合成氨反应N2+3H2 2NH3的平衡常数表达式:
2NH3的平衡常数表达式:____________________ ,升高温度时K值______ (填“增大”“减小”或“不变”)。
 2NH3 △H<0。
2NH3 △H<0。(1)反应开始阶段,v(正)
(2)达到平衡后,若正反应速率用v(N2)表示,逆反应速率用v’(H2)表示,则v(N2)=
(3)下列措施中能加快反应速率并提高氢气的转化率的是
A.其他条件不变时,压缩容器体积 B.其他条件不变时,升高反应体系温度
C.使用合适的催化剂 D.保持容器体积不变,充入一定量的氮气
(4)实际生产中往往需要将温度控制在一个合适的范围,分析温度不宜过高也不宜过低的原因是
(5)写出合成氨反应N2+3H2
 2NH3的平衡常数表达式:
2NH3的平衡常数表达式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时,在2L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如图所示,由图中数据分析得:

(1)该反应的化学方程式为__________ ;
(2)反应开始至4min时,B的平均反应速率为________ , A的转化率为_____ 。
(3)4min时,反应是否达到平衡状态?________ (填“是”或“否”),8min时,v(正)________ v(逆)(填“>”、“<”或“=”)。

(1)该反应的化学方程式为
(2)反应开始至4min时,B的平均反应速率为
(3)4min时,反应是否达到平衡状态?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一定条件下,向V L密闭容器中充入 和
和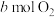 ,发生反应
,发生反应 。
。
(1)反应刚开始时,由于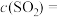
___________ ,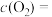
___________ ,而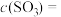
___________ ,所以化学反应速率___________ 最大,而___________ 最小(为零)(填“v(正)”或“v(逆)”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为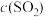
___________ (填“增大”“减小”或“不变”下同),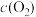
___________ ,而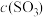
___________ ,从而化学反应速率v(正)___________ ,而v(逆)___________ 。
(3)当反应进行到时v(正)与v(逆)___________ 时,此时可逆反应达到最大限度,若保持外界条件不变时,混合物中各组分的物质的量、浓度、质量分数、体积分数及总压强都___________ 。
(4)以下是反应: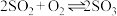 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。
试回答下列问题:
①提高该化学反应限度的途径:___________ 。
②要实现 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是___________ 。
 和
和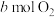 ,发生反应
,发生反应 。
。(1)反应刚开始时,由于
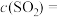
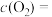
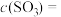
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为
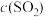
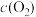
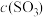
(3)当反应进行到时v(正)与v(逆)
(4)以下是反应:
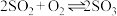 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。压强 转化率 温度 | 0.1 MPa | 0.5 MPa | 1 MPa | 10 MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
①提高该化学反应限度的途径:
②要实现
 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
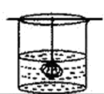
【推荐1】在一个温度不变的密闭容器内,放入一杯饱和的硫酸铜溶液,用细线吊住一块有缺口的硫酸铜晶体CuSO4▪5H218O浸在溶液中(如图)过几天后观察到:晶体上的缺口___________ (填“有”或“没有”)了;晶体的质量 ___________ (填“减小”、“增大”或“没变”);此时的硫酸铜溶液是 ___________ (填“饱和”或“不饱和”溶液)。溶液中,溶剂水中___________ (填“含有”或“不含”)18O;胆矾晶体中___________ (填“含有”或“不含”)18O。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定条件下,向2L恒容密闭容器中充入1mol PCl5,发生反应:PCl5(g) PCl3(g)+Cl2(g),反应过程中测定的部分数据见下表(反应过程中条件不变):
PCl3(g)+Cl2(g),反应过程中测定的部分数据见下表(反应过程中条件不变):
请回答下列问题:
(1)x的值是________ ;
(2)0-50s内,用PCl3的浓度变化表示的化学反应速率是________ ;
(3)250s以后,Cl2的物质的量不再改变的原因是_______________ ;
(4)250s时,容器中Cl2的物质的量是_____ ,PCl5的物质的量是______ ,PCl5的转化率是______ 。
 PCl3(g)+Cl2(g),反应过程中测定的部分数据见下表(反应过程中条件不变):
PCl3(g)+Cl2(g),反应过程中测定的部分数据见下表(反应过程中条件不变):t/s | 0 | 50 | 100 | 150 | 250 | 350 | 450 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 | x | |
(1)x的值是
(2)0-50s内,用PCl3的浓度变化表示的化学反应速率是
(3)250s以后,Cl2的物质的量不再改变的原因是
(4)250s时,容器中Cl2的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】资源的可持续发展是化学家的重要研究方向。甲醇是优质的清洁燃料,可制作燃料电池。CO2经催化加氢可生成甲醇,主要有以下两个反应:
反应①:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.6kJ•mol-1
CH3OH(g)+H2O(g) ΔH=-49.6kJ•mol-1
反应②:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ•mol-1
CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ•mol-1
(1)反应①的活化能Ea(正)_____ Ea(逆)(填“>”、“<”或“=”)。
(2)一定温度下,在某一恒容密闭容器中充入一定量的CO2和H2,发生反应①。下列能说明该反应已达到平衡状态的是_____ (填序号)。
(3)在T温度下,将2.5molCO2和5.5molH2充入2L的恒容密闭容器中发生反应①和②,达到平衡状态时CH3OH(g)和CH3OCH3(g)的物质的量分别为1mol和0.25mol。计算该温度下反应①的平衡常数K=_____ 。
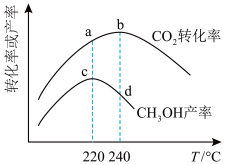
(4)催化剂作用下,充入CO2和H2同时发生反应①和反应②,经相同反应时间,测得不同温度下CO2转化率和CH3OH产率的变化曲线如图。220℃~240℃温度区间CO2转化率和CH3OH产率的变化不一致的可能原因是_____ 。
(5)向2L密闭容器中充入1molCO2和3molH2,在一定条件下,发生反应:CO2(g)+3H2(g) CH3OH(l)+H2O(l) ΔH<0,CO2的浓度随时间(0~t2)变化如图所示。其他条件不变,在t2时间将容器体积缩小至原来的一半,t3时重新达到平衡。请画出t2~t4时段内CO2浓度的变化曲线
CH3OH(l)+H2O(l) ΔH<0,CO2的浓度随时间(0~t2)变化如图所示。其他条件不变,在t2时间将容器体积缩小至原来的一半,t3时重新达到平衡。请画出t2~t4时段内CO2浓度的变化曲线_____ 。(在答题卷对应区域作图)

反应①:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.6kJ•mol-1
CH3OH(g)+H2O(g) ΔH=-49.6kJ•mol-1反应②:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ•mol-1
CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ•mol-1(1)反应①的活化能Ea(正)
(2)一定温度下,在某一恒容密闭容器中充入一定量的CO2和H2,发生反应①。下列能说明该反应已达到平衡状态的是
| A.混合气体的密度不再随时间变化而改变 |
| B.气体的压强不再随时间变化而改变 |
| C.CH3OH的物质的量不再随时间变化而改变 |
| D.单位时间内每形成1.5molH-H键,同时形成1molC-H键 |
(4)催化剂作用下,充入CO2和H2同时发生反应①和反应②,经相同反应时间,测得不同温度下CO2转化率和CH3OH产率的变化曲线如图。220℃~240℃温度区间CO2转化率和CH3OH产率的变化不一致的可能原因是

(5)向2L密闭容器中充入1molCO2和3molH2,在一定条件下,发生反应:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) ΔH<0,CO2的浓度随时间(0~t2)变化如图所示。其他条件不变,在t2时间将容器体积缩小至原来的一半,t3时重新达到平衡。请画出t2~t4时段内CO2浓度的变化曲线
CH3OH(l)+H2O(l) ΔH<0,CO2的浓度随时间(0~t2)变化如图所示。其他条件不变,在t2时间将容器体积缩小至原来的一半,t3时重新达到平衡。请画出t2~t4时段内CO2浓度的变化曲线
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学平衡图像分析
(1)对于反应
 ,
,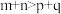
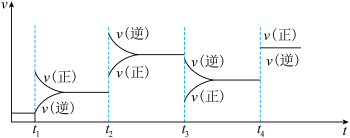
上图中各时间点改变的条件是
_______ ;
_______ ;
_______ 。
(2)可逆反应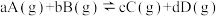
 ,同时符合下列两图中各曲线,
,同时符合下列两图中各曲线,

则
_______ 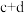

_______ 

_______ 0(填“>”、“<”或“=”)
(3)某化学科研小组研究在其他条件不变时,改变某一条件对反应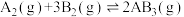 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)

根据图像得出的结论,若正反应吸热,则
_______  (填“>”、“<”或“=”),对于a、b、c三点:
(填“>”、“<”或“=”),对于a、b、c三点: 的平衡体积分数由大到小为
的平衡体积分数由大到小为_______ , 的平衡转化率由大到小为
的平衡转化率由大到小为_______ , 的平衡转化率由大到小为
的平衡转化率由大到小为_______ 。
(4)对于化学反应 ,L线上所有的点都是平衡点。
,L线上所有的点都是平衡点。

则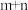
_______ 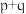 ,E点
,E点
_______  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(1)对于反应

 ,
,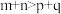

上图中各时间点改变的条件是



(2)可逆反应
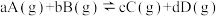
 ,同时符合下列两图中各曲线,
,同时符合下列两图中各曲线,
则

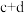



(3)某化学科研小组研究在其他条件不变时,改变某一条件对反应
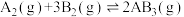 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
根据图像得出的结论,若正反应吸热,则

 (填“>”、“<”或“=”),对于a、b、c三点:
(填“>”、“<”或“=”),对于a、b、c三点: 的平衡体积分数由大到小为
的平衡体积分数由大到小为 的平衡转化率由大到小为
的平衡转化率由大到小为 的平衡转化率由大到小为
的平衡转化率由大到小为(4)对于化学反应
 ,L线上所有的点都是平衡点。
,L线上所有的点都是平衡点。
则
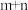
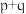 ,E点
,E点
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在2 L密闭容器内,800℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)800℃,反应达到平衡时,NO的物质的量浓度为__________ mol/L;升高温度,NO的浓度增大,则该反应是________ (填“放热”或“吸热”)反应。
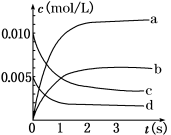
(2)如下图中表示NO2变化的曲线是________ (填字母序号a、b、c、d)。用O2表示从0~2 s内该反应的平均速率v=________ mol/(L·s)。
(3)能说明该反应已达到平衡状态的是________ 。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________ 。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度为

(2)如下图中表示NO2变化的曲线是
(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) △H=akJ ·mol-1
2Fe(s)+3CO2(g) △H=akJ ·mol-1
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H1=+489.0kJ·mol-1
②C(石墨)+CO2(g)=2CO(g) △H2=+172.5kJ·mol-1
则a=__________
(2)冶炼铁反应的平衡常数表达式K=____________ ,温度升高后,K值____ (填“增大”、“不变”或“减小”)。
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
①甲容器中CO的平衡转化率为__________ 。
②下列说法正确的是__________ (填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲、乙容器中,CO的平衡浓度之比为2:3
c.增加Fe2O3可以提高CO2的转化率
 2Fe(s)+3CO2(g) △H=akJ ·mol-1
2Fe(s)+3CO2(g) △H=akJ ·mol-1(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H1=+489.0kJ·mol-1
②C(石墨)+CO2(g)=2CO(g) △H2=+172.5kJ·mol-1
则a=
(2)冶炼铁反应的平衡常数表达式K=
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
| Fe2O3 | CO | Fe | CO2 | ||
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 | |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 | |
①甲容器中CO的平衡转化率为
②下列说法正确的是
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲、乙容器中,CO的平衡浓度之比为2:3
c.增加Fe2O3可以提高CO2的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:

(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为______ mol/(L·min)。
(2)根据上图写出该反应的化学方程式________ ,该反应的平衡常数表达式为K=________ 。
(3)①第5min时,升高温度,A、B、D的物质的量变化如上图,则该反应的正反应是___ (填“放热”或“吸热”)反应,反应的平衡常数______ (填“增大”“减小”或“不变”,下同)。
②若在第7min时增加D的物质的量,A的物质的量变化正确的是____ (用图中a、b、c的编号回答)。

(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为
(2)根据上图写出该反应的化学方程式
(3)①第5min时,升高温度,A、B、D的物质的量变化如上图,则该反应的正反应是
②若在第7min时增加D的物质的量,A的物质的量变化正确的是
您最近一年使用:0次
【推荐2】某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_______________ 。
(2) 反应开始至2 min,以气体Z表示的平均反应速率为________ 。
(3)若X、Y、Z均为气体,2 min后反应达到平衡, 反应达平衡时:
①此时体系的压强是开始时的_______ 倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时_________ (填“增大”“减小”或“相等”)。
(4)可以判断上述反应已经达到平衡的是________ 。
A.v(A):v(B):v(C)等于化学计量系数之比
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.混合气体的平均相对分子质量不再改变
E.n(A) :n(B) :n(C)等于化学计量系数之比

(1)该反应的化学方程式为
(2) 反应开始至2 min,以气体Z表示的平均反应速率为
(3)若X、Y、Z均为气体,2 min后反应达到平衡, 反应达平衡时:
①此时体系的压强是开始时的
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时
(4)可以判断上述反应已经达到平衡的是
A.v(A):v(B):v(C)等于化学计量系数之比
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.混合气体的平均相对分子质量不再改变
E.n(A) :n(B) :n(C)等于化学计量系数之比
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】燃料电池和锂离子电池在生产生活中占据重要地位,甲醇是常见的燃料电池原料,CO2催化氢化可合成甲醇。反应为:CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) +48.9kJ,完成下列填空:
CH3OH(g) + H2O(g) +48.9kJ,完成下列填空:
(1)反应的平衡常数 K=_________ 。
(2)在 2L 容器中充入 4 mol CO2和 H2的混合气体,反应 10 min 后,气体的总物质的量变为原来的75 %,则 0~10 min 内,H2的平均反应速率为_________ ,前 5min 内的 v 逆(CH3OH)________ 前 10min 内的 v 逆(CH3OH) (选填“大于” “等于”或“小于”),原因是________ 。
(3)在恒容密闭容器发生上述反应,下图是反应过程中两个物理量变化关系图象,曲线上各点均已达到平衡状态。

若 x 轴表示温度,则 y 轴可表示_____ ,(任写一个),一定温度下,若 x 轴为原料投料比[n(H2)/n(CO2)],则 y 轴是______ 的转化率。
(4)工业生产或实验室制备中,通常加大某一反应物的用量,以提高另一反应物的转化率,举一例说明________________________ 。
 CH3OH(g) + H2O(g) +48.9kJ,完成下列填空:
CH3OH(g) + H2O(g) +48.9kJ,完成下列填空:(1)反应的平衡常数 K=
(2)在 2L 容器中充入 4 mol CO2和 H2的混合气体,反应 10 min 后,气体的总物质的量变为原来的75 %,则 0~10 min 内,H2的平均反应速率为
(3)在恒容密闭容器发生上述反应,下图是反应过程中两个物理量变化关系图象,曲线上各点均已达到平衡状态。

若 x 轴表示温度,则 y 轴可表示
(4)工业生产或实验室制备中,通常加大某一反应物的用量,以提高另一反应物的转化率,举一例说明
您最近一年使用:0次



