物质的量浓度相同(0.1mol·L-1)的弱酸HX和NaX溶液等体积混合后,溶液中微粒浓度关系错误的是
| A.c(Na+)+c(H+)=c(X-)+c(OH-) |
| B.c(HX)+c(X-)=2c(Na+) |
| C.若溶液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) |
| D.若溶液呈碱性,则c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+) |
更新时间:2020-09-04 08:41:19
|
相似题推荐
单选题
|
适中
(0.65)
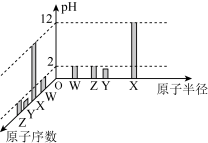
【推荐1】常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01 )的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
)的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
 )的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
)的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
| A.简单离子半径:Y>Z>W>X | B.单质的沸点:Y>Z |
| C.X与Y形成的化合物的水溶液呈酸性 | D. 可作为自来水的消毒剂 可作为自来水的消毒剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作能达到实验目的是
| 选项 | 实验操作 | 实验目的 |
| A | 向银镜反应后的试管中加入适量稀硝酸,微热 | 除去试管内壁附着的单质银 |
| B | 称取24 g CuSO·5H2O固体配制溶液 | 配制480 mL 0.2 mol·L-1CuSO4溶液 |
| C | 将MgCl2溶液置于蒸发皿中加热蒸干 | 由MgCl2溶液制得MgCl2固体 |
| D | 用pH试纸测CH3COONa溶液pH =9,NaNO2溶液pH=8 | 判断HNO2和CH3COOH酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】硫代二乙酸( )可用作抗氧剂,并用于生产硫代酯类抗氧剂。常温下,将NaOH溶液滴入硫代二乙酸(简写为H2R)溶液中,混合溶液中的离子浓度随溶液pH变化的关系如图所示。下列说法正确的是
)可用作抗氧剂,并用于生产硫代酯类抗氧剂。常温下,将NaOH溶液滴入硫代二乙酸(简写为H2R)溶液中,混合溶液中的离子浓度随溶液pH变化的关系如图所示。下列说法正确的是

 )可用作抗氧剂,并用于生产硫代酯类抗氧剂。常温下,将NaOH溶液滴入硫代二乙酸(简写为H2R)溶液中,混合溶液中的离子浓度随溶液pH变化的关系如图所示。下列说法正确的是
)可用作抗氧剂,并用于生产硫代酯类抗氧剂。常温下,将NaOH溶液滴入硫代二乙酸(简写为H2R)溶液中,混合溶液中的离子浓度随溶液pH变化的关系如图所示。下列说法正确的是
A.甲表示−lg 随溶液pH变化的关系 随溶液pH变化的关系 |
| B.Ka2(H2R)的数量级为10−6 |
| C.NaHR溶液中,c(H2R)>c(R2−) |
| D.M点溶液中,c(Na+)+c(H+)=c(OH−)+2.1c(R2−) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,向0.01mol/L的醋酸溶液中滴入pH=7的醋酸铵稀溶液,溶液pH随滴入醋酸铵溶液体积变化的曲线示意图如下图所示,下列分析正确的是


| A.ac段,溶液pH增大是CH3COOH==CH3COO-+H+逆向移动的结果 |
| B.a点,pH=2 |
C.b点,c(CH3COO-)>c( ) ) |
| D.c点,pH可能大于7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
A.25 ℃时,pH=7的NH4Cl与NH3·H2O混合溶液:c(H+)=c(OH-)=c( )=c(Cl-) )=c(Cl-) |
| B.25 ℃时,向10 mL pH=12的NaOH溶液中滴加等体积pH=2的CH3COOH溶液: c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.0.1 mol·L-1的CH3COONa溶液与0.1 mol·L-1的CaCl2溶液等体积混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
D.浓度均为0.1 mol·L-1的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2溶液中,c( )的大小顺序为③>②>① )的大小顺序为③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】草酸(H2C2O4)是二元弱酸,NaHC2O4溶液呈酸性。常温下,向10 mL 0.01 mol/L NaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系错误的是
| A.V(NaOH) = 0时,c(H+) >1×10-7mol/L |
| B.V(NaOH)<10 mL时,可能存在c(Na+) = 2c(C2O42-)+c(HC2O4- ) |
| C.V(NaOH) = 10 mL时,溶液的pH为9,则10-9= 10-5-2c(H2C2O4)-c(HC2O4-) |
| D.V(NaOH)>10 mL时,可能存在c(OH- )>c(Na+)>c(C2O42-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,下列溶液中粒子浓度关系正确的是
| A.Na2S溶液:c(Na+)>c(S2-)>c(HS-)>c(OH-)>c(H2S) |
B.NaHC2O4溶液:c(H+)+c(H2C2O4)=c(OH-)+c(C2O ) ) |
C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO )+c(OH-) )+c(OH-) |
D.等浓度Na2CO3和NaHCO3的混合溶液:3c(Na+)=2c(CO )+2c(HCO )+2c(HCO )+2c(H2CO3) )+2c(H2CO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
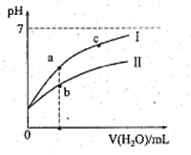
【推荐2】下表为25℃时某些弱酸的电离平衡常数;图象表示25℃时,稀释CH3COOH、HClO两种酸的稀溶液,溶液pH随加水量的变化。常温下,有关说法正确的是

| 弱酸的电离平衡常数(25℃) | |
| CH3COOH | HClO |
| Ka=1.8×10-5 | Ka=3.0×10-8 |
| A.图象中,a点酸的总浓度>b点酸的总浓度 |
| B.图象中,c(H+):c(R-)的值:a点>c点(HR代表CH3COOH或HClO) |
| C.pH相同的CH3COONa溶液和NaClO溶液的浓度关系:c(CH3COOHNa)<c(NaClO) |
| D.两溶液浓度相等,CH3COONa溶液的c(OH- )+c(CH3COO-) > NaClO溶液的c(OH-)+c(C1O-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】谷氨酸( )的解离反应式:
)的解离反应式:


向10.00 0.1000
0.1000 谷氨酸溶液中通入
谷氨酸溶液中通入 或加入
或加入 固体,所得溶液
固体,所得溶液 随加入酸或碱的物质的量变化曲线如图。下列说法不正确的是
随加入酸或碱的物质的量变化曲线如图。下列说法不正确的是
 )的解离反应式:
)的解离反应式:

向10.00
 0.1000
0.1000 谷氨酸溶液中通入
谷氨酸溶液中通入 或加入
或加入 固体,所得溶液
固体,所得溶液 随加入酸或碱的物质的量变化曲线如图。下列说法不正确的是
随加入酸或碱的物质的量变化曲线如图。下列说法不正确的是A.  |
B.水的电离程度:b点 点 点 |
C.d点存在关系: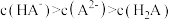 |
D.当谷氨酸所带净电荷为0(即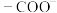 与 与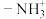 数目相等)时,溶液 数目相等)时,溶液 为3.22 为3.22 |
您最近一年使用:0次



