一定条件下,H2O2在水溶液中发生分解反应:2H2O2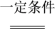 2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:
2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:
(1)该反应__ (填“是”或者“不是”)氧化还原反应。
(2)该分解反应0~20min的平均反应速率v(H2O2)为__ mol/(L·min)。
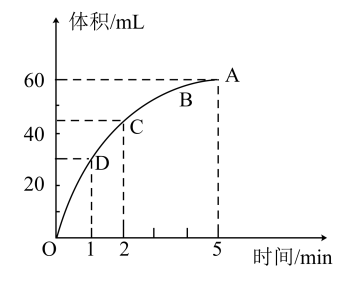
(3)加入0.1mol的MnO2粉末于50mL过氧化氢的溶液中(密度为1.1g/mL),在标准状况下放出气体的体积和时间的关系如图所示;反应放出 气体所需要的时间为
气体所需要的时间为__ ;A、B、C、D四点化学反应速率快慢的顺序为__ 。
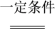 2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:
2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:| t/min | 0 | 20 | 40 | 60 | 80 |
| c(H2O2)/(mol/L) | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |
(1)该反应
(2)该分解反应0~20min的平均反应速率v(H2O2)为
(3)加入0.1mol的MnO2粉末于50mL过氧化氢的溶液中(密度为1.1g/mL),在标准状况下放出气体的体积和时间的关系如图所示;反应放出
 气体所需要的时间为
气体所需要的时间为
更新时间:2020-09-09 11:01:34
|
相似题推荐
【推荐1】针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑ D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅体现氧化性的反应是________ (填序号,下同),H2O2仅体现还原性的反应是________ ,H2O2既体现氧化性又体现还原性的反应是________ ,H2O2既不作氧化剂又不作还原剂的反应是________ 。
A.Na2O2+HCl→H2O2+NaCl B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑ D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅体现氧化性的反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有下列一组物质:He、Cl2、CH4、Na2O2、Ba(OH)2、NO2、KNO3、H2SO4,请从中选择,用化学式填写下列空白:
(1)只含有共价键,不含其他化学键的化合物有__________ ;
(2)既含有共价键又含有离子键的物质有__________ ;
(3)能在水中发生氧化还原反应的有____________ 。
(1)只含有共价键,不含其他化学键的化合物有
(2)既含有共价键又含有离子键的物质有
(3)能在水中发生氧化还原反应的有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氧化还原反应在生产和生活中使用非常广泛。回答下列问题:
(1)氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应属于区域3的是___________(填字母)。

(2) 外观和食盐相似,又有咸味,容易使人误食中毒。已知
外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: 。
。
①上述反应中氧化剂是___________ (填化学式,下同),氧化产物是___________ ,还原剂和氧化剂的物质的量之比是___________ 。
②若反应中有 (标准状况下)气体生成,则反应中转移电子的物质的量为
(标准状况下)气体生成,则反应中转移电子的物质的量为_____ 。
③某厂废液中,含有 的
的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是___________ (填字母)。
A. B.
B. C.
C. D.浓
D.浓
(3)过氧化氢俗名双氧水,在生产、生活中有多种用途。涉及的化学反应如下:
A.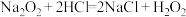
B.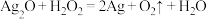
C.
D.
①上述反应中, 仅体现氧化性的是
仅体现氧化性的是___________ (填字母,下同), 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是___________ , 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是___________ 。
②某酸性反应体系中发生一个氧化还原反应,反应物和生成物共六种微粒: 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生了如下过程:
只发生了如下过程: 。则该反应的离子方程式为
。则该反应的离子方程式为___________ 。
(1)氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应属于区域3的是___________(填字母)。

A. |
B.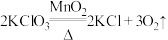 |
C. |
D. |
 外观和食盐相似,又有咸味,容易使人误食中毒。已知
外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: 。
。①上述反应中氧化剂是
②若反应中有
 (标准状况下)气体生成,则反应中转移电子的物质的量为
(标准状况下)气体生成,则反应中转移电子的物质的量为③某厂废液中,含有
 的
的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是A.
 B.
B. C.
C. D.浓
D.浓
(3)过氧化氢俗名双氧水,在生产、生活中有多种用途。涉及的化学反应如下:
A.
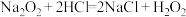
B.
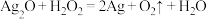
C.

D.

①上述反应中,
 仅体现氧化性的是
仅体现氧化性的是 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是②某酸性反应体系中发生一个氧化还原反应,反应物和生成物共六种微粒:
 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生了如下过程:
只发生了如下过程: 。则该反应的离子方程式为
。则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在某一容积为5 L的密闭容器内,加入0.2mol 的CO和0.2mol的H2O(g),在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。

(1)根据图中数据,从反应开始至达到平衡时,CO的化学反应速率为__ mol·(L·min)-1;反应平衡时c(H2)=__ mol·L-1。
(2)判断该反应达到平衡的依据是________(填序号)。
 CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
(1)根据图中数据,从反应开始至达到平衡时,CO的化学反应速率为
(2)判断该反应达到平衡的依据是________(填序号)。
| A.CO减少的化学反应速率和CO2减少的化学反应速率相等 | B.CO、H2O、CO2、H2的浓度都相等 |
| C.CO、H2O、CO2、H2的浓度都不再发生变化 | D.正、逆反应速率都为零 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】汽车尾气中的CO、NO2在一定条件下可以发生反应:4CO(g)+2NO2(g)4CO2(g)+N2(g) ΔH=−1 200 kJ·mol-1。在一定温度下,向容积固定为2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示:

(1)0~10 min内该反应的平均速率v(CO)=________ ,从11 min起其他条件不变,压缩容器的容积变为1 L,则n(NO2)的变化曲线可能为图中的______ (填字母)。
(2)恒温恒容条件下,不能说明该反应已达到平衡状态的是________ (填字母)。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2)
D.容器内混合气体密度保持不变

(1)0~10 min内该反应的平均速率v(CO)=
(2)恒温恒容条件下,不能说明该反应已达到平衡状态的是
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2)
D.容器内混合气体密度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】将等物质的量的A、B混合于2L密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g)。经5min后,测得D的浓度为0.5mol•L-1,c(A):c(B)=3:5,C的平均反应速率为0.1mol·L-1·min-1。求:
(1)x=_______ ;反应开始前放入容器中的A的物质量是_______ 。
(2)浓度c(A)=_______ ;5min内B的平均速率v(B)=_______ ;
(3)某时刻D的浓度为0.6mol•L-1,则A的转化率α(A)=_______ 。已知:转化率α(A)=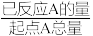 ×100%
×100%
(1)x=
(2)浓度c(A)=
(3)某时刻D的浓度为0.6mol•L-1,则A的转化率α(A)=
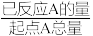 ×100%
×100%
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在一定条件下,容积为2L的密闭容器中,将2molL气体和3molM气体混合,发生如下反应:2L(g)+3M(g) xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1。计算:
xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1。计算:
(1)10s末L的物质的量浓度为_______ 。
(2)前10s内用M表示的化学反应速率为_______ 。
(3)化学方程式中x值为_______ 。
(4)L(g)的转化率为_______ 。
(5)在恒温恒容条件下,往容器中加入1mol氦气,反应速率________ 。(填“增大”、“减小”或“不变”,下同)。
(6)在恒温恒压条件,往容器中加入1mol氦气,反应速率________ 。
 xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1。计算:
xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1。计算:(1)10s末L的物质的量浓度为
(2)前10s内用M表示的化学反应速率为
(3)化学方程式中x值为
(4)L(g)的转化率为
(5)在恒温恒容条件下,往容器中加入1mol氦气,反应速率
(6)在恒温恒压条件,往容器中加入1mol氦气,反应速率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。下图是废旧钴酸锂电池材料(主要成分为LiCoO2,含少量铁、铝、铜等元素的化合物)回收工艺流程:

“沉钴”过程中,(NH4)2C2O4的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:


根据图分析:沉钴时应控制n(C2O )∶n(Co2+)为
)∶n(Co2+)为_______ ,温度控制在_______ ℃左右

“沉钴”过程中,(NH4)2C2O4的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:


根据图分析:沉钴时应控制n(C2O
 )∶n(Co2+)为
)∶n(Co2+)为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】运用化学反应原理研究氮及其化合物的反应有重要意义。
(1)写出NH3的电子式____ ,NH3催化氧化的化学方程式为____ 。
(2)合成氨反应N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ·mol-1,在工业生产中温度常控制在480℃,而非常温。请从化学反应速率和催化剂的角度加以解释
2NH3(g)△H=-92.4kJ·mol-1,在工业生产中温度常控制在480℃,而非常温。请从化学反应速率和催化剂的角度加以解释____ 。
(3)合成氨过程中发生的反应机理如下:
I.2xFe+N2 2FexN(慢);
2FexN(慢);
II.2FexN+3H2(g) 2xFe+2NH3(g)(快)
2xFe+2NH3(g)(快)
回答下列问题:
合成氨反应的速率快慢主要取决于____ (填“I”或“II”)。
②合成氨反应的催化剂是____ (填化学式)。
③反应I的活化能_____ 反应II的活化能(填“>”“=”或“<”)。
④使用催化剂前后,合成氮反应的△H___ (填“增大”“减小”或“不变”)。
(1)写出NH3的电子式
(2)合成氨反应N2(g)+3H2(g)
 2NH3(g)△H=-92.4kJ·mol-1,在工业生产中温度常控制在480℃,而非常温。请从化学反应速率和催化剂的角度加以解释
2NH3(g)△H=-92.4kJ·mol-1,在工业生产中温度常控制在480℃,而非常温。请从化学反应速率和催化剂的角度加以解释(3)合成氨过程中发生的反应机理如下:
I.2xFe+N2
 2FexN(慢);
2FexN(慢);II.2FexN+3H2(g)
 2xFe+2NH3(g)(快)
2xFe+2NH3(g)(快)回答下列问题:
合成氨反应的速率快慢主要取决于
②合成氨反应的催化剂是
③反应I的活化能
④使用催化剂前后,合成氮反应的△H
您最近一年使用:0次



