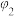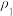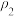某温度时,N2+3H2⇌2NH3的平衡常数K=16,则此温度下,NH3⇌ H2+
H2+ N2的平衡常数为( )
N2的平衡常数为( )
 H2+
H2+ N2的平衡常数为( )
N2的平衡常数为( )| A.0.25 | B.4 | C.2 | D.256 |
20-21高二上·全国·课时练习 查看更多[1]
(已下线)2.2.1 化学平衡状态 化学平衡常数(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)
更新时间:2020-09-18 22:07:25
|
相似题推荐
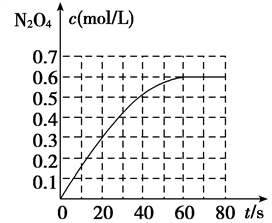
【推荐1】298 K时,在2 L固定体积的密闭容器中,发生可逆反应:2NO2(g)  N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
 N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
| A.v(正)>v(逆) |
| B.v(正)<v(逆) |
| C.v(正)=v(逆) |
| D.v(正)、v(逆)大小关系不确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.0.1 mol·L-1 NH4Cl溶液加水稀释, 的值减小 的值减小 |
| B.常温下,反应2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)能自发进行,该反应ΔH<0 |
| C.反应C(s)+H2O(g)⇌CO(g)+H2(g)达平衡后,缩小容器体积,H2O(g)平衡转化率不变 |
| D.由CH4、O2和KOH溶液组成的燃料电池,负极反应为CH4+8OH--8e-=CO2+6H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在 溶液中存在平衡:
溶液中存在平衡: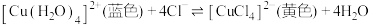
 ,下列说法正确的是
,下列说法正确的是
 溶液中存在平衡:
溶液中存在平衡: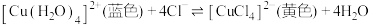
 ,下列说法正确的是
,下列说法正确的是| A.该反应的反应类型为氧化还原反应 |
B.该反应的平衡常数表达式为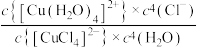 |
C.仅增大 的浓度,反应达到平衡后,该反应的平衡常数增大 的浓度,反应达到平衡后,该反应的平衡常数增大 |
D.仅适当升高温度,反应达到平衡后, 的物质的量增大 的物质的量增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,在恒容密闭容器中,加入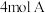 和
和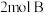 进行如下反应:
进行如下反应: 。反应一段时间后达到平衡,测得生成
。反应一段时间后达到平衡,测得生成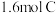 ,且反应前后的压强之比为5:4。下列说法正确的是
,且反应前后的压强之比为5:4。下列说法正确的是
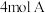 和
和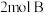 进行如下反应:
进行如下反应: 。反应一段时间后达到平衡,测得生成
。反应一段时间后达到平衡,测得生成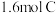 ,且反应前后的压强之比为5:4。下列说法正确的是
,且反应前后的压强之比为5:4。下列说法正确的是A.该反应的平衡常数表达式为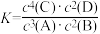 |
| B.平衡时,B的转化率为40% |
| C.增加生成物C的量,B的转化率变小 |
| D.增大压强,平衡向右移动,化学平衡常数K增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】K、Ka、Kw分别表示化学平衡常数、弱酸的电离常数和水的离子积常数,下列判断正确的是
| A.在500℃、20MPa条件下,在5L密闭容器中进行合成氨的反应,使用催化剂后K增大 |
| B.室温下Ka(HCN)<Ka(CH3COOH),说明CH3COOH的电离度一定比HCN的大 |
| C.25℃时,pH均为4的盐酸和NH4I溶液中Kw不相等 |
| D.2SO2+O2⇌2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知2NO2(g)+O3(g) N2O5(g)+O2(g) △H<0,在一定温度下将2molNO2和1molO3充入一恒容密闭容器中进行反应,直至t1时达到平衡状态。下列图象正确的是
N2O5(g)+O2(g) △H<0,在一定温度下将2molNO2和1molO3充入一恒容密闭容器中进行反应,直至t1时达到平衡状态。下列图象正确的是
 N2O5(g)+O2(g) △H<0,在一定温度下将2molNO2和1molO3充入一恒容密闭容器中进行反应,直至t1时达到平衡状态。下列图象正确的是
N2O5(g)+O2(g) △H<0,在一定温度下将2molNO2和1molO3充入一恒容密闭容器中进行反应,直至t1时达到平衡状态。下列图象正确的是A.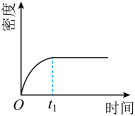 | B.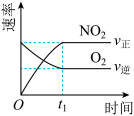 |
C.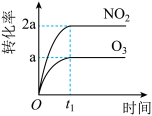 | D.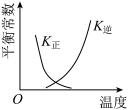 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】加热N2O5依次发生的分解反应为:①N2O5(g) N2O3(g)+O2(g),②N2O3(g)
N2O3(g)+O2(g),②N2O3(g) N2O(g)+O2(g);在2L密闭容器中充入8molN2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应②的平衡常数约为
N2O(g)+O2(g);在2L密闭容器中充入8molN2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应②的平衡常数约为
 N2O3(g)+O2(g),②N2O3(g)
N2O3(g)+O2(g),②N2O3(g) N2O(g)+O2(g);在2L密闭容器中充入8molN2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应②的平衡常数约为
N2O(g)+O2(g);在2L密闭容器中充入8molN2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应②的平衡常数约为| A.3.7mol/L | B.8.5mol/L | C.9.6mol/L | D.10.2mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于反应AX3(g)+X2(g) AX5(g)在容积为10L的密闭容器中进行。起始时
AX5(g)在容积为10L的密闭容器中进行。起始时 和
和 均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法
均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法不正确 的是
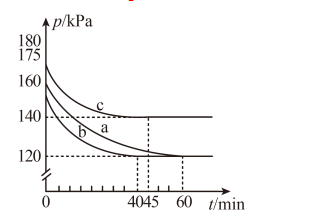
 AX5(g)在容积为10L的密闭容器中进行。起始时
AX5(g)在容积为10L的密闭容器中进行。起始时 和
和 均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法
均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法
| A.比较实验a、c可判断升高温度反应速率加快 |
| B.实验a条件下,用浓度表示的平衡常数为100 |
| C.该反应的∆H>0 |
D.实验c条件下,从反应开始至达到平衡时 的平均速率为1.8×10-4mol/(L·min) 的平均速率为1.8×10-4mol/(L·min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在3个2 L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)  2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
下列说法不正确的是
 2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:容器 | 甲 | 乙 | 丙 |
反应物的投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4 mol N2 | 2 mol NH3 |
达到平衡的时间/min | 5 | 8 | |
平衡时N2的浓度/ |
| 1.5 | |
NH3的体积分数 |
|
| |
混合气体的密度/ |
|
|
| A.容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol·L-1·min-1 |
| B.2c1<1.5 |
C.在该温度下甲容器中反应的平衡常数K=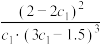 |
| D.2ρ1=ρ2 |
您最近一年使用:0次

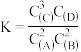
 2NO(g),曲线a表示该反应在温度T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。叙述正确的是(
2NO(g),曲线a表示该反应在温度T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。叙述正确的是(
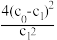
 7N2(g)+12H2O(l)
7N2(g)+12H2O(l)