向恒温恒容密闭容器中充入气体A,发生反应:xA(g) yB(g)+zC(g),各物质的浓度随时间的变化如表所示。重庆一中化学组刘卫兵老师看了看你的草稿,推了下你的胳膊,暗示了你一下,那么“这道题正确的是......”( )
yB(g)+zC(g),各物质的浓度随时间的变化如表所示。重庆一中化学组刘卫兵老师看了看你的草稿,推了下你的胳膊,暗示了你一下,那么“这道题正确的是......”( )
 yB(g)+zC(g),各物质的浓度随时间的变化如表所示。重庆一中化学组刘卫兵老师看了看你的草稿,推了下你的胳膊,暗示了你一下,那么“这道题正确的是......”( )
yB(g)+zC(g),各物质的浓度随时间的变化如表所示。重庆一中化学组刘卫兵老师看了看你的草稿,推了下你的胳膊,暗示了你一下,那么“这道题正确的是......”( )| 时间/s | c(A)/(mol•L-1) | c(B)/(mol•L-1) | c(C)/(mol•L-1) |
| 0 | 0.540 | 0 | 0 |
| 5 | 0.530 | 0.015 | 0.020 |
| 15 | 0.514 | 0.039 | 0.052 |
| 30 | 0.496 | 0.066 | 0.088 |
| A.0~30s内B的平均生成速率为2.2×10-3mol·L-1·s-1 |
| B.x+y=3 |
| C.若起始时在容器中通入氦气,使容器压强增大,各物质反应速率均加快 |
| D.随着反应的进行,A的反应速率不断减慢,是因为该反应是吸热反应 |
更新时间:2020-10-21 12:10:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】由 羟基丁酸
羟基丁酸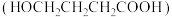 生成
生成 丁内酯的反应如下:
丁内酯的反应如下:
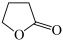
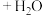 .在
.在 时,水溶液中
时,水溶液中 羟基丁酸的初始浓度为
羟基丁酸的初始浓度为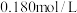 ,随着反应的进行,测得
,随着反应的进行,测得 丁内酯的浓度随时间的变化如下表所示:
丁内酯的浓度随时间的变化如下表所示:
下列说法不正确的是
 羟基丁酸
羟基丁酸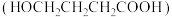 生成
生成 丁内酯的反应如下:
丁内酯的反应如下:

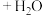 .在
.在 时,水溶液中
时,水溶液中 羟基丁酸的初始浓度为
羟基丁酸的初始浓度为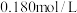 ,随着反应的进行,测得
,随着反应的进行,测得 丁内酯的浓度随时间的变化如下表所示:
丁内酯的浓度随时间的变化如下表所示:
| 21 | 50 | 80 | 100 | 120 | 160 | 220 |
|
| 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
A.在 内,以 内,以 丁内酯的浓度变化表示的反应速率为 丁内酯的浓度变化表示的反应速率为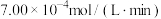 |
B.在 时,该反应的平衡常数 时,该反应的平衡常数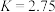 |
C.及时移出了 丁内酯,平衡时 丁内酯,平衡时 羟基丁酸的转化率提高,反应速率加快 羟基丁酸的转化率提高,反应速率加快 |
D.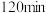 时, 时, 羟基丁酸㢩转化率为 羟基丁酸㢩转化率为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知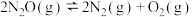 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关)。实验测得,
(k为速率常数,只与温度、催化剂有关)。实验测得, 在催化剂X表面反应的变化数据如下:
在催化剂X表面反应的变化数据如下:
下列说法正确的是
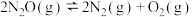 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关)。实验测得,
(k为速率常数,只与温度、催化剂有关)。实验测得, 在催化剂X表面反应的变化数据如下:
在催化剂X表面反应的变化数据如下:| t/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
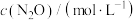 | 0.100 | 0.080 |  | 0.040 | 0.020 |  | 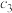 | 0 |
A. , ,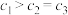 |
B.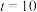 min时, min时, |
C.相同条件下,增大 的浓度或催化剂X的表面积,都能加快反应速率 的浓度或催化剂X的表面积,都能加快反应速率 |
D.保持其他条件不变,若 起始浓度为0.200mol·L 起始浓度为0.200mol·L ,当浓度减至一半时共耗时不到50min ,当浓度减至一半时共耗时不到50min |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
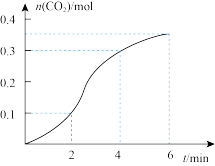
【推荐3】 与稀盐酸反应生成
与稀盐酸反应生成 的量与反应时间的关系如图所示。下列结论中不正确的是
的量与反应时间的关系如图所示。下列结论中不正确的是
 与稀盐酸反应生成
与稀盐酸反应生成 的量与反应时间的关系如图所示。下列结论中不正确的是
的量与反应时间的关系如图所示。下列结论中不正确的是
A.反应在 min内生成 min内生成 的平均反应速率为 的平均反应速率为  |
| B.反应开始4 min内,温度变化比浓度变化对反应速率的影响更大 |
C.4min后,反应速率减小的主要原因是 减小 减小 |
D.图中反应在 内的平均反应速率最小 内的平均反应速率最小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】2SO2+O2 2SO3是工业制硫酸的一步重要反应,下列关于该反应的说法正确的是
2SO3是工业制硫酸的一步重要反应,下列关于该反应的说法正确的是
 2SO3是工业制硫酸的一步重要反应,下列关于该反应的说法正确的是
2SO3是工业制硫酸的一步重要反应,下列关于该反应的说法正确的是| A.使用催化剂不影响反应速率 |
| B.升高体系温度能加快反应速率 |
| C.减小SO2的浓度能加快反应的速率 |
| D.若反应在密闭容器中进行,SO2和O2能100%转化为SO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法中不正确的有( )个
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g) B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g)
 B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
| A.2 个 | B.3 个 | C.4 个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在2 L密闭恒容容器内,500℃时发生反应: ,体系中n(NO)随时间的变化如表:
,体系中n(NO)随时间的变化如表:
下列说法正确的是
 ,体系中n(NO)随时间的变化如表:
,体系中n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 |
| A.2 s内消耗氧气的平均速率为3.0×10-3 mol/(L·s) |
| B.反应达到平衡时,2v(NO)=v(O2) |
| C.当容器内气体的密度或气体颜色不再发生变化时,该反应达到平衡状态 |
| D.若K500℃>K550℃,第4 s后升温至达到新平衡过程中逆反应速率先增大后减小(K表示平衡常数) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知反应A(s)+B(g)  C(g)+D(g)的化学平衡常数和温度的关系如下:
C(g)+D(g)的化学平衡常数和温度的关系如下:
下列说法正确的是
 C(g)+D(g)的化学平衡常数和温度的关系如下:
C(g)+D(g)的化学平衡常数和温度的关系如下:| 温度(℃) | 700 | 800 | 830 | 1 000 | 1 200 |
| 化学平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A.该反应的化学平衡常数表达式为:K= |
| B.该反应为吸热反应 |
| C.830℃下,体系中有适量A,且c(B)=c(C)=c(D)=1mol/L时,该体系状态是平衡状态 |
| D.其他条件不变时,增大体系压强,化学平衡常数减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一定温度下(T2>T1),在3个体积均为2.0 L的恒容密闭容器中反应 (正反应放热)达到平衡,下列说法正确的是
(正反应放热)达到平衡,下列说法正确的是
 (正反应放热)达到平衡,下列说法正确的是
(正反应放热)达到平衡,下列说法正确的是| 容器编号 | 温度/K | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
| c(NO) | c(Cl2) | c(ClNO) | c(ClNO) | ||
| Ⅰ | T1 | 0.20 | 0.10 | 0 | 0.04 |
| Ⅱ | T1 | 0.20 | 0.10 | 0.20 | c1 |
| Ⅲ | T2 | 0 | 0 | 0.20 | c2 |
A.达到平衡时,容器Ⅱ中 比容器Ⅰ中的大 比容器Ⅰ中的大 |
| B.达到平衡时,容器Ⅲ中ClNO的转化率小于80% |
| C.达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为1:2 |
| D.若温度从T1变到T2,平衡常数K值增大 |
您最近一年使用:0次



 溶于一定量水中,溶液呈蓝色(溶液①)。加入少量浓
溶于一定量水中,溶液呈蓝色(溶液①)。加入少量浓 ,溶液变为黄色(溶液②)。已知:
,溶液变为黄色(溶液②)。已知: ;浓度较小时
;浓度较小时 用
用 表示。取以上溶液进行如下实验,对实验现象分析正确的是
表示。取以上溶液进行如下实验,对实验现象分析正确的是 ,证明
,证明 生成
生成 与
与 对溶液颜色变化、
对溶液颜色变化、 后,黄色褪去,说明
后,黄色褪去,说明 能抑制
能抑制

