原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29,回答下列问题:
(1)W2+基态核外电子排布式为______ 。
(2)Y2X2分子中Y原子轨道的杂化类型为_______ ,1molY2X2含有σ键的数目为____ ;化合物ZX3的沸点比化合物YX4的高,其主要原因是____ 。
(3)元素Y的一种氧化物与元素Z的一种氧化物电子总数相同,则元素Z的这种氧化物的分子式是_ 。
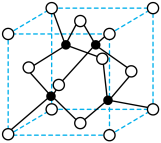
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是_____ ,它可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,反应的化学方程式为______ 。
(1)W2+基态核外电子排布式为
(2)Y2X2分子中Y原子轨道的杂化类型为
(3)元素Y的一种氧化物与元素Z的一种氧化物电子总数相同,则元素Z的这种氧化物的分子式是
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是

更新时间:2020-11-12 20:19:51
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】A. 海底热液研究(图1)处于当今科研的前沿。海底热液活动区域“黑烟囱”的周围常存在FeS、黄铜矿及锌矿等矿物。
(1) Ni2+的核外电子排布式是____________________ 。
(2) 分析下表,铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,基主要原因是____________________ 。
(3) 下列说法正确的是________ 。
A. 电负性:N>O>S>C B. CO2与COS(硫化羰)互为等电子体
C. NH3分子中氮原子采用sp3杂化 D. CO、H2S、HCN都是极性分子
(4) “酸性热液”中大量存在一价阳离子,结构如图2,它的化学式为________________ 。
(5) FeS与NaCl均为离子晶体,晶胞相似,前者熔点为985℃,后者801℃,其原因是____________________ 。在FeS晶胞中,与Fe2+距离相等且最近的S2-围成的多面体的空间构型为________________ 。

(1) Ni2+的核外电子排布式是
(2) 分析下表,铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,基主要原因是
| 电离能/kJ·mol-1 | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
(3) 下列说法正确的是
A. 电负性:N>O>S>C B. CO2与COS(硫化羰)互为等电子体
C. NH3分子中氮原子采用sp3杂化 D. CO、H2S、HCN都是极性分子
(4) “酸性热液”中大量存在一价阳离子,结构如图2,它的化学式为
(5) FeS与NaCl均为离子晶体,晶胞相似,前者熔点为985℃,后者801℃,其原因是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氨及其化合物与人类生产、生活息息相关。其中尿素(H2NCONH2)是人类最早合成的有机物,工业上生产尿素的反应为 ,
, 。回答下列问题:
。回答下列问题:
(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu在周期表中的位置为___________ ,基态Cu2+的电子排布式为___________ ,Zn位于元素周期表的___________ 区。
(2)C、N、O三种元素电负性从大到小的顺序是___________ 。
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是______ ,原因是_______ 。
(4)尿素分子中,C原子杂化轨道类型是______ ,1mol尿素分子中含σ键数目为______ 个。
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼如图(a)和六方氮化硼(b),前者类似于金刚石,后者与石墨相似。
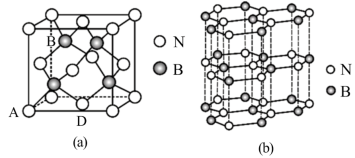
①X—射线衍射实验测得立方氮化硼晶胞参数为mpm,则立方氮化硼晶体N与B的原子半径之和表达式为_______ pm。
②已知六方氮化硼同层中B、N原子距离为acm,密度为dg/cm3,则层与层之间距离的计算表达式为________ pm。
 ,
, 。回答下列问题:
。回答下列问题:(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu在周期表中的位置为
(2)C、N、O三种元素电负性从大到小的顺序是
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是
(4)尿素分子中,C原子杂化轨道类型是
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼如图(a)和六方氮化硼(b),前者类似于金刚石,后者与石墨相似。

①X—射线衍射实验测得立方氮化硼晶胞参数为mpm,则立方氮化硼晶体N与B的原子半径之和表达式为
②已知六方氮化硼同层中B、N原子距离为acm,密度为dg/cm3,则层与层之间距离的计算表达式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】在铜、银催化下,乙烯与氧气反应生成环氧乙烷( )和乙醛,下图是该反应的部分历程。
)和乙醛,下图是该反应的部分历程。

(2)鉴别以上产物乙醛和环氧乙烷可以用___________。
| A.原子发射光谱 | B.原子吸收光谱 | C.核磁共振氢谱 | D.红外光谱 |
(3)以下电子排布式和价电子轨道表示式中,正确且对应微粒为基态原子的是___________。
A.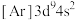 | B.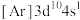 |
C. | D.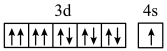 |
(4)已知
 的熔点为1235℃,
的熔点为1235℃, 的熔点为1130℃,二者晶体结构类似,且熔点都较高,但
的熔点为1130℃,二者晶体结构类似,且熔点都较高,但 熔点比
熔点比 高,其原因是
高,其原因是(5)
 晶胞结构如图所示,其中
晶胞结构如图所示,其中 代表的原子是
代表的原子是 ,晶胞参数为a pm,则阿伏加德罗常数值
,晶胞参数为a pm,则阿伏加德罗常数值
 和a的代数式表示)
和a的代数式表示)
 可以形成一种配位化合物,其结构如下图所示。以下说法正确的是___________。
可以形成一种配位化合物,其结构如下图所示。以下说法正确的是___________。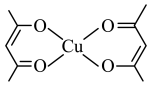
A. 的配位数是2 的配位数是2 |
| B.此配合物中存在配位键、极性键、非极性键 |
| C.配体中O原子提供空轨道 |
D. 提供孤电子对 提供孤电子对 |
(7)已知:常温下,①
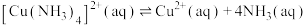
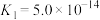 ;
;②


则常温下
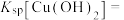
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)将乙炔通入 溶液生成
溶液生成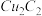 红棕色沉淀。
红棕色沉淀。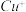 基态核外电子排布式为
基态核外电子排布式为____________ 。
(2) Ca2+的离子结构示意图:__________________________ ;已知CaC2中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______ ;1mol 中含有的
中含有的 键数目为
键数目为___________ 。
(3)乙炔与氢氰酸反应可得丙烯腈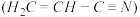 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是___________ ;分子中处于同一直线上的原子数目最多为__________ 。
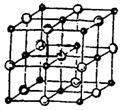
(4) 晶体的晶胞结构与
晶体的晶胞结构与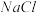 晶体的相似(如下图所示),但CaC2晶体中含有的哑铃形
晶体的相似(如下图所示),但CaC2晶体中含有的哑铃形 的存在,使晶胞沿一个方向拉长。CaC2晶体中1个
的存在,使晶胞沿一个方向拉长。CaC2晶体中1个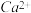 周围距离最近的
周围距离最近的 数目为
数目为__________ 。
(1)将乙炔通入
 溶液生成
溶液生成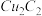 红棕色沉淀。
红棕色沉淀。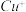 基态核外电子排布式为
基态核外电子排布式为(2) Ca2+的离子结构示意图:
 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的
中含有的 键数目为
键数目为(3)乙炔与氢氰酸反应可得丙烯腈
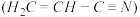 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是(4)
 晶体的晶胞结构与
晶体的晶胞结构与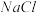 晶体的相似(如下图所示),但CaC2晶体中含有的哑铃形
晶体的相似(如下图所示),但CaC2晶体中含有的哑铃形 的存在,使晶胞沿一个方向拉长。CaC2晶体中1个
的存在,使晶胞沿一个方向拉长。CaC2晶体中1个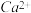 周围距离最近的
周围距离最近的 数目为
数目为
您最近一年使用:0次
【推荐2】锰的单质及其化合物的用途非常广泛.回答下列问题:
(1)基态锰原子的核外电子排布式为_______ ,其d轨道中未成对电子数为__________ .
(2)MnO的熔点(1650℃)比MnS的熔点(1610℃)高,它们都属于___ 晶体。前者熔点较高的原因是_____________ 。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

① 与Mn2+形成配位键的原子为_______ (填元素符号)。
② BH4-的空间构型为_______ ,其中B原子的杂化轨道类型为________ 。
③ 写出两种与BH4-互为等电子体的分子或离子:___________ 。
(4)一种磁性材料的单晶胞结构如图所示。
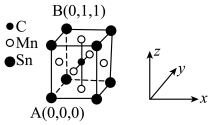
① 该晶胞中碳原子的原子坐标为________ 。
② Mn在晶体中的堆积方式为________ (填“简单立方”“体心立方”“面心立方最密”或“六方最密") 堆积。
③ 若该晶胞的边长为a pm,NA表示阿伏伽德罗常数的数值,则该晶体密度的表达式为ρ=_____ 。
(1)基态锰原子的核外电子排布式为
(2)MnO的熔点(1650℃)比MnS的熔点(1610℃)高,它们都属于
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

① 与Mn2+形成配位键的原子为
② BH4-的空间构型为
③ 写出两种与BH4-互为等电子体的分子或离子:
(4)一种磁性材料的单晶胞结构如图所示。

① 该晶胞中碳原子的原子坐标为
② Mn在晶体中的堆积方式为
③ 若该晶胞的边长为a pm,NA表示阿伏伽德罗常数的数值,则该晶体密度的表达式为ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】高氯酸三碳酰肼合镍{[Ni(CHZ)3](C104)2}是一种新型的起爆药。
(1)Ni2+核外电子排布式为___ 。
(2)ClO4-空间构型是___ ;与ClO4-互为等电子体的一种分子为___ (填化学式)。
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为___ ;C、N、O三种元素的电负性由大到小的顺序为___ 。
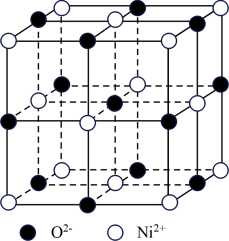
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为___ 。
(1)Ni2+核外电子排布式为
(2)ClO4-空间构型是
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】【选修3—物质的结构与性质】在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,第二周期元素B原子的核外成对电子数是未成对电子数的2倍,C原子的最外层p轨道的电子为半充满结构,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有—个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图为_______________ 。
(2)B、C、D三元素第一电离能由小到大的顺序为(用元素符号表示)______________ ;
(3)B的最高价氧化物对应的水化物分子中,其中心原子杂化轨道的类型为____________ 杂化;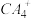 的空间构型为
的空间构型为__________ (用文字描述)。
(4)C的单质与化合物BD是等电子体,写出化合物BD的电子式______________ ;1mol BC-中含有π键的数目为___________________ 。
(5)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为(用元素符号表示)______________ ;若相邻D原子和F原子间的距离为a cm,阿伏加德罗常数为NA,则该晶体的密度为_____________ g/cm3(用含a、NA的符号表示)。

(1)基态E原子的价电子排布图为
(2)B、C、D三元素第一电离能由小到大的顺序为(用元素符号表示)
(3)B的最高价氧化物对应的水化物分子中,其中心原子杂化轨道的类型为
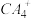 的空间构型为
的空间构型为(4)C的单质与化合物BD是等电子体,写出化合物BD的电子式
(5)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为(用元素符号表示)

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】镍是一种用途广泛的金属,常用于电镀工业和制造电池。镍易形成Ni(CO)4、[Ni(NH3)6]SO4等配合物。
(1)镍基态原子的核外电子排布式为________ 。
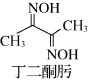
(2)Ni2+可用丁二酮肟检验。丁二酮肟的结构如图所示,其分子中碳原子轨道的杂化类型为________ 。
(3)与CO互为等电子体的阴离子的化学式为__________________ 。
(4)1 mol [Ni(NH3)6]SO4中σ键的数目为________ 。氨的沸点高于膦(PH3),原因是____________________________ 。
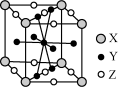
(5)镧镍合金是较好的储氢材料。储氢后所得晶体的化学式为LaNi5H6,晶胞结构如图所示,X、Y、Z表示储氢后的三种微粒,则图中Z表示的微粒为________ (填化学式)。
(1)镍基态原子的核外电子排布式为
(2)Ni2+可用丁二酮肟检验。丁二酮肟的结构如图所示,其分子中碳原子轨道的杂化类型为

(3)与CO互为等电子体的阴离子的化学式为
(4)1 mol [Ni(NH3)6]SO4中σ键的数目为
(5)镧镍合金是较好的储氢材料。储氢后所得晶体的化学式为LaNi5H6,晶胞结构如图所示,X、Y、Z表示储氢后的三种微粒,则图中Z表示的微粒为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Ti及其化合物在航天工业上有重要的应用,回答下列问题:
(1)基态Ti原子的价电子排布式为_______ ,基态Ti原子核外存在_______ 对自旋相反的电子。
(2)TiCl4熔点为−23℃,沸点为136℃,TiCl4晶体属于_______ 晶体。TiCl4可由TiO2与COCl2在一定条件下反应得到,反应的化学方程式为_______ ,COCl2中共价键类型为_______ ,C原子的杂化轨道类型是_______ ,与COCl2互为等电子体的分子为_______ 。C、O、Cl的电负性由小到大的顺序为_______ 。
(3)金红石型TiO2晶胞如图,如果晶胞的边长为apm,则它的密度为_______ g/cm3(列出计算式即可)。

(1)基态Ti原子的价电子排布式为
(2)TiCl4熔点为−23℃,沸点为136℃,TiCl4晶体属于
(3)金红石型TiO2晶胞如图,如果晶胞的边长为apm,则它的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
(2)第四周期主族元素中,第一电离能介于Ga、As之间的元素有___________ 种。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是___________ 。
(4)氧是地壳中含量最多的元素。H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因为___________ 。
(5)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是___________ 。
②若该晶胞的晶胞边长为d nm,则该合金的密度为___________  。(不用化简)
。(不用化简)
③若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下H2的体积约为__________ 。
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
| A.1s22s22p43s1 | B.1s22s22p43d2 | C.1s22s22p5 | D.1s22s22p6 |
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
| 电离能/kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(4)氧是地壳中含量最多的元素。H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因为
(5)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是
②若该晶胞的晶胞边长为d nm,则该合金的密度为
 。(不用化简)
。(不用化简)③若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下H2的体积约为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料。D与A位于同一主族,是构成地球上矿物质的主要元素。请回答下列问题:
(1)元素A能形成多种单质,其中的一种单质能用作电极、润滑剂与制造铅笔等。A与D所形成的化合物属于_______ 晶体,其中心原子是以_________ 杂化成键;
(2)B的核外电子排布式为_________________ ,
(3)向含有C的硫酸盐中逐滴滴加氨水,所观察到的现象是________________________ ;再向上述溶液中加入乙醇,有______________ ;原因是_______________________ ;
(4)A的氢化物比D的氢化物相比,熔点高是的________ (填化学式),理由是__________
(5)下列说法正确的是( )
a.晶体析出规则是晶格能高的晶体最后析出
b.铜型和钾型都是密置层堆积方式
c.在干冰晶体中,每一个CO2周围有12个紧邻的CO2分子
d.邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
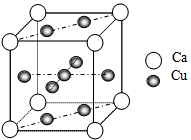
(6)下图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为_____________ ,已知两个最近的Ca原子之间的距离为apm,则该合金的密度为_____________ g/cm3,(用含NA和a的代数式表示)。
(1)元素A能形成多种单质,其中的一种单质能用作电极、润滑剂与制造铅笔等。A与D所形成的化合物属于
(2)B的核外电子排布式为
(3)向含有C的硫酸盐中逐滴滴加氨水,所观察到的现象是
(4)A的氢化物比D的氢化物相比,熔点高是的
(5)下列说法正确的是
a.晶体析出规则是晶格能高的晶体最后析出
b.铜型和钾型都是密置层堆积方式
c.在干冰晶体中,每一个CO2周围有12个紧邻的CO2分子
d.邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
(6)下图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】我国科学家在大分子合成方面又有新突破,以1,4-二咪唑-丁烷为有机胺模板剂,利用中温水热合成方法获得三维镉超分子化合物。该化合物中含有C、H、O、Se、Cd、Co、Ca等元素。回答下列问题:
(1)基态钴原子的价电子轨道表示式为___________ 。
(2)苯分子中含有大π键,可记为 (右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为
(右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,该分子中的大π键,可表示为
,不能使溴的四氯化碳溶液褪色,该分子中的大π键,可表示为__________ ,Se的杂化方式为___________ 。
(3)金属离子配合物的颜色主要与分裂能有关。1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,用△表示,中心离子带电荷数越多,与配体距离越近,则作用越强,△越大。分裂能(△):
___________ (填“>”“<”或“=”)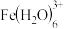 ,理由是
,理由是___________ 。
(4) 晶体属四方晶系,晶胞如图所示,
晶体属四方晶系,晶胞如图所示,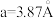 ,
,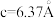 (
(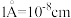 ),晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,在位于原点的钙离子上面的碳原子的分数坐标为(0,0,0.406)。一个
),晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,在位于原点的钙离子上面的碳原子的分数坐标为(0,0,0.406)。一个 周围距离最近的
周围距离最近的 有
有___________ 个, 基团中C-C键长为
基团中C-C键长为___________  (保留小数点后两位),最短的Ca-C距离为
(保留小数点后两位),最短的Ca-C距离为___________  (列出计算式)。
(列出计算式)。

(1)基态钴原子的价电子轨道表示式为
(2)苯分子中含有大π键,可记为
 (右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为
(右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,该分子中的大π键,可表示为
,不能使溴的四氯化碳溶液褪色,该分子中的大π键,可表示为(3)金属离子配合物的颜色主要与分裂能有关。1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,用△表示,中心离子带电荷数越多,与配体距离越近,则作用越强,△越大。分裂能(△):

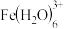 ,理由是
,理由是(4)
 晶体属四方晶系,晶胞如图所示,
晶体属四方晶系,晶胞如图所示,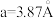 ,
,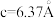 (
(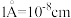 ),晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,在位于原点的钙离子上面的碳原子的分数坐标为(0,0,0.406)。一个
),晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,在位于原点的钙离子上面的碳原子的分数坐标为(0,0,0.406)。一个 周围距离最近的
周围距离最近的 有
有 基团中C-C键长为
基团中C-C键长为 (保留小数点后两位),最短的Ca-C距离为
(保留小数点后两位),最短的Ca-C距离为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次



