工业合成氨的反应:N2+3H3 2NH3是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量。
2NH3是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量。
(1)相同条件下,1 mol N2和3 mol H2所具有的能量________ (“大于”、“小于”、“等于”)2 molNH3具有的能量;
(2)如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量_______ (“大于”、“小于”、“等于”)上述数值,其原因是_____________ ;
(3)实验室模拟工业合成氨时,在容器为2L的密闭容器内,反应经过10min后,生成10 mol NH3,则用N2表示的该反应速率为:_____________ ;
(4)一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是_______
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值
d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等
 2NH3是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量。
2NH3是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量。(1)相同条件下,1 mol N2和3 mol H2所具有的能量
(2)如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量
(3)实验室模拟工业合成氨时,在容器为2L的密闭容器内,反应经过10min后,生成10 mol NH3,则用N2表示的该反应速率为:
(4)一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值
d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等
更新时间:2020-11-14 10:41:39
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】I.请将符合题意的下列变化的序号填在对应的横线上:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解。
(1)化学键没有被破坏的是____ ;
(2)仅发生离子键破坏的是_____ ;
(3)既发生离子键又发生共价键破坏的是_____ ;
(4)已知拆开 键、
键、 、
、 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、 、
、 。则由
。则由 和
和 反应生成
反应生成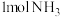 需要放出
需要放出____ 的热量。
II.A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(条件及其他物质略):A B
B C
C D
D
(1)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸暂时变红,则A为___ 。写出A→B转化的化学方程式:____ 。
(2)若A为活泼金属元素的单质,D为强碱,焰色反应都显黄色,则A是____ 。A跟水发生反应的离子方程式为:____ 。
(1)化学键没有被破坏的是
(2)仅发生离子键破坏的是
(3)既发生离子键又发生共价键破坏的是
(4)已知拆开
 键、
键、 、
、 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、 、
、 。则由
。则由 和
和 反应生成
反应生成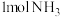 需要放出
需要放出II.A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(条件及其他物质略):A
 B
B C
C D
D(1)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸暂时变红,则A为
(2)若A为活泼金属元素的单质,D为强碱,焰色反应都显黄色,则A是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】当今世界多国相继规划了碳达峰、碳中和的时间节点,中国承诺2030年前,二氧化碳的排放不再增长,达到峰值之后逐步降低。2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。因此,降低空气中二氧化碳含量成为研究热点,其中研发二氧化碳的利用技术,将二氧化碳转化为能源是缓解环境和解决能源问题的方案之一、
I.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。
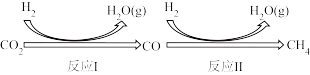
已知:总反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1=-205kJ/mol
CH4(g)+2H2O(g) ∆H1=-205kJ/mol
反应Ⅱ:CO(g)+3H2(g) CH4+H2O(g) ∆H2=-246kJ/mol
CH4+H2O(g) ∆H2=-246kJ/mol
(1)则反应Ⅰ的热化学方程式为___________ 。
(2)一定条件下,向2L恒容密闭容器中加入1mol CO2和5mol H2只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率v(H2)=___________ 。
Ⅱ.在催化剂作用下CO2加氢还可制得甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H=+50kJ/mol。
CH3OH(g)+H2O(g) ∆H=+50kJ/mol。
(3)能说明反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H=+50kJ/mol已达平衡状态的是
CH3OH(g)+H2O(g) ∆H=+50kJ/mol已达平衡状态的是___________ (填字母)。
A.单位时间内生成1mol CH3OH(g)的同时消耗了3mol H2(g)
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在恒温恒压的容器中,气体的平均摩尔质量不再变化
Ⅲ.CO2与H2催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ∆H<0;
CH3OCH3(g)+3H2O(g) ∆H<0;
②CO2(g)+H2(g) CO(g)+H2O(g) ∆H>0。
CO(g)+H2O(g) ∆H>0。
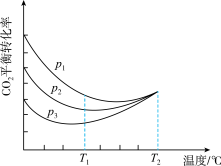
(4)向密闭容器中以物质的量之比为1:3充入CO2与H2实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为___________ ;T2℃时主要发生反应___________ 。(填“①”或“②”),CO2平衡转化率随温度变化先降后升的原因___________ 。
I.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。
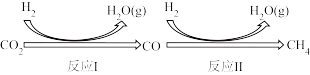
已知:总反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1=-205kJ/mol
CH4(g)+2H2O(g) ∆H1=-205kJ/mol反应Ⅱ:CO(g)+3H2(g)
 CH4+H2O(g) ∆H2=-246kJ/mol
CH4+H2O(g) ∆H2=-246kJ/mol(1)则反应Ⅰ的热化学方程式为
(2)一定条件下,向2L恒容密闭容器中加入1mol CO2和5mol H2只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率v(H2)=
Ⅱ.在催化剂作用下CO2加氢还可制得甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H=+50kJ/mol。
CH3OH(g)+H2O(g) ∆H=+50kJ/mol。(3)能说明反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H=+50kJ/mol已达平衡状态的是
CH3OH(g)+H2O(g) ∆H=+50kJ/mol已达平衡状态的是A.单位时间内生成1mol CH3OH(g)的同时消耗了3mol H2(g)
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在恒温恒压的容器中,气体的平均摩尔质量不再变化
Ⅲ.CO2与H2催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) ∆H<0;
CH3OCH3(g)+3H2O(g) ∆H<0;②CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H>0。
CO(g)+H2O(g) ∆H>0。(4)向密闭容器中以物质的量之比为1:3充入CO2与H2实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列问题。
(1)23 g C2H6O(l)和一定量的氧气混合点燃,恰好完全反应,生成CO2(g)和H2O(l),放出683.5 kJ的热量,其热化学方程式:___________ 。
(2)1 mol C(s,石墨)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3 kJ热量,请写出该反应的热化学方程式:___________ 。
(3)在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)。(填“增大”“减小”或“不变”)
①保持容器容积不变,向其中充入1 mol H2,反应速率___________ ,H2的转化率___________ 。
②保持温度不变,扩大容器体积,反应速率___________ 。
③保持容器体积不变,向其中充入1 mol N2,反应速率___________ 。
(1)23 g C2H6O(l)和一定量的氧气混合点燃,恰好完全反应,生成CO2(g)和H2O(l),放出683.5 kJ的热量,其热化学方程式:
(2)1 mol C(s,石墨)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3 kJ热量,请写出该反应的热化学方程式:
(3)在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)。(填“增大”“减小”或“不变”)
①保持容器容积不变,向其中充入1 mol H2,反应速率
②保持温度不变,扩大容器体积,反应速率
③保持容器体积不变,向其中充入1 mol N2,反应速率
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题
Ⅰ.已知:断裂 化学键吸收的能量或者形成
化学键吸收的能量或者形成 化学键放出的能量叫该化学键的键能。根据下表回答问题:
化学键放出的能量叫该化学键的键能。根据下表回答问题:
(1)已知 ,每生成
,每生成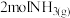 放出
放出 的热量,则上表中
的热量,则上表中 的数值为
的数值为___________ 。
(2)关于反应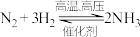 的下列说法正确的是___________。
的下列说法正确的是___________。
(3)检验生成的 的方法是
的方法是___________ 。氨的催化氧化是工业合成硝酸的基础,该反应方程式为___________ 。
Ⅱ.已知:反应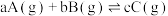 ,某温度下,在
,某温度下,在 的密闭容器中投入一定量的
的密闭容器中投入一定量的 和
和 ,两种气体的物质的量浓度随时间变化的曲线如图所示,C未画出。
,两种气体的物质的量浓度随时间变化的曲线如图所示,C未画出。
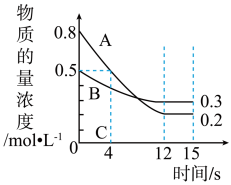
(4) 时间内
时间内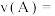
___________ 。
(5)经测定,前 内
内 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(6)下列叙述能说明该反应达到化学平衡状态的是___________ 。
A.混合气体的总物质的量不随时间变化而变化
B.单位时间内每消耗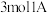 ,同时生成
,同时生成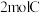
C.
D.混合气体的密度不随时间变化而变化
E.混合气体的平均摩尔质量不随时间变化而变化
Ⅰ.已知:断裂
 化学键吸收的能量或者形成
化学键吸收的能量或者形成 化学键放出的能量叫该化学键的键能。根据下表回答问题:
化学键放出的能量叫该化学键的键能。根据下表回答问题:| 化学键 |  |  |  |
键能( ) ) | 435 | 390 |  |
 ,每生成
,每生成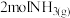 放出
放出 的热量,则上表中
的热量,则上表中 的数值为
的数值为(2)关于反应
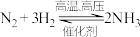 的下列说法正确的是___________。
的下列说法正确的是___________。| A.在其他条件不变时,升高温度,正反应速率会增大,逆反应速率会减小 |
B.在恒温恒容的密闭容器中,充入 气使压强增大,该反应速率增大 气使压强增大,该反应速率增大 |
| C.使用催化剂是为了增大反应速率,提高生产效率 |
D.若需要制备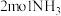 通入的氮气的物质的量应大于 通入的氮气的物质的量应大于 |
 的方法是
的方法是Ⅱ.已知:反应
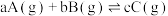 ,某温度下,在
,某温度下,在 的密闭容器中投入一定量的
的密闭容器中投入一定量的 和
和 ,两种气体的物质的量浓度随时间变化的曲线如图所示,C未画出。
,两种气体的物质的量浓度随时间变化的曲线如图所示,C未画出。
(4)
 时间内
时间内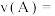
(5)经测定,前
 内
内 ,写出该反应的化学方程式
,写出该反应的化学方程式(6)下列叙述能说明该反应达到化学平衡状态的是
A.混合气体的总物质的量不随时间变化而变化
B.单位时间内每消耗
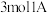 ,同时生成
,同时生成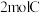
C.

D.混合气体的密度不随时间变化而变化
E.混合气体的平均摩尔质量不随时间变化而变化
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】 温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。

(1)写出容器中发生反应的方程式___________ ;正反应为___________ 反应(填“放热”或“吸热”)。
(2)当 时,该反应
时,该反应___________ 达到平衡状态(填“已”或“未”);由图Ⅰ,若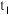 为10min,则
为10min,则 时间内,
时间内,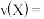
___________ ; 时平衡常数K=
时平衡常数K=___________ (保留小数点后一位)。
(3)其它条件不变,再充入一定量X,平衡___________ 移动(填“正向”、“逆向”、或“不”),X的转化率___________ (填“增大”、“减小”、或“不变”)。
 温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。
(1)写出容器中发生反应的方程式
(2)当
 时,该反应
时,该反应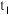 为10min,则
为10min,则 时间内,
时间内,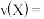
 时平衡常数K=
时平衡常数K=(3)其它条件不变,再充入一定量X,平衡
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学小组运用控制变量法研究外界条件对化学反应速率的影响,做了如下实验。请按要求回答下列问题:
(1)室温下,探究影响 分解速率的因素,见下表和如图:
分解速率的因素,见下表和如图:
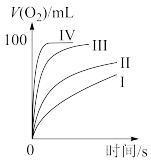
①表中x为_______ ;
②实验Ⅱ、Ⅲ探究的是_______ 对 分解速率的影响,根据图上图,得出的结论是
分解速率的影响,根据图上图,得出的结论是_______ 。
③根据上图,实验Ⅰ、Ⅳ对比得出的结论是_______ 。
(2)为进一步研究离子对 分解的影响,小组同学又做了比较
分解的影响,小组同学又做了比较 和
和 对
对 分解影响的下列实验:
分解影响的下列实验:
①定性分析:用如图装置可通过观察_______ ,定性得出结论。
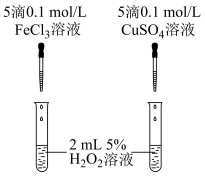
某同学认为将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是_______ .
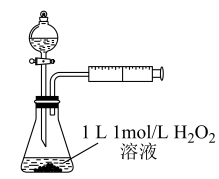
②定量分析:为了更精确地研究催化剂对反应速率的影响,利用如图装置进行定量实验。实验测得,在硫酸铜催化下过 发生分解反应,2min时生成气体1.12L(气体体积已换算为标准状况),则
发生分解反应,2min时生成气体1.12L(气体体积已换算为标准状况),则 的分解速率为
的分解速率为_______  。
。
(1)室温下,探究影响
 分解速率的因素,见下表和如图:
分解速率的因素,见下表和如图:
| 实验 | 所用试剂 | |
| Ⅰ | 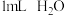 |  |
| Ⅱ | 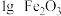 | 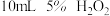 |
| Ⅲ | 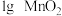 | 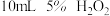 |
| Ⅳ |  | 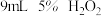 |
②实验Ⅱ、Ⅲ探究的是
 分解速率的影响,根据图上图,得出的结论是
分解速率的影响,根据图上图,得出的结论是③根据上图,实验Ⅰ、Ⅳ对比得出的结论是
(2)为进一步研究离子对
 分解的影响,小组同学又做了比较
分解的影响,小组同学又做了比较 和
和 对
对 分解影响的下列实验:
分解影响的下列实验:①定性分析:用如图装置可通过观察

某同学认为将
 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是②定量分析:为了更精确地研究催化剂对反应速率的影响,利用如图装置进行定量实验。实验测得,在硫酸铜催化下过
 发生分解反应,2min时生成气体1.12L(气体体积已换算为标准状况),则
发生分解反应,2min时生成气体1.12L(气体体积已换算为标准状况),则 的分解速率为
的分解速率为 。
。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】含氮化合物对工业生产有多种影响,化学工作者设计了如下再利用的方案:
I.以 和
和 为原料合成化肥-尿素
为原料合成化肥-尿素 ,两步反应的能量变化如图:
,两步反应的能量变化如图:

(1)该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
(2)已知第二步反应决定了生产尿素的快慢,可推测
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(3)下列措施能提高该反应 的平衡转化率的是_______。
的平衡转化率的是_______。
II.氨的催化氧化过程发生以下两种反应,该过程易受催化剂选择性的影响。
①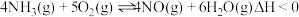
②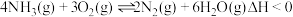
在容积固定的密闭容器中充入 和
和 ,一定时间内,在催化剂作用下发生上述反应。生成物和的物质的量随温度的变化曲线如图。
,一定时间内,在催化剂作用下发生上述反应。生成物和的物质的量随温度的变化曲线如图。
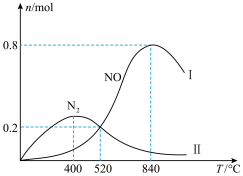
(4)当温度低于400℃时, 的物质的量增大的幅度高于
的物质的量增大的幅度高于 ,其原因是
,其原因是_______ 。
(5)840℃时, 的转化率约为
的转化率约为_______ 若520℃时平衡压强为 ,列出520℃反应②平衡常数
,列出520℃反应②平衡常数 的计算式
的计算式
_______ (无需化简)。
I.以
 和
和 为原料合成化肥-尿素
为原料合成化肥-尿素 ,两步反应的能量变化如图:
,两步反应的能量变化如图:
(1)该反应在
(2)已知第二步反应决定了生产尿素的快慢,可推测

 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。(3)下列措施能提高该反应
 的平衡转化率的是_______。
的平衡转化率的是_______。| A.选用更有效的催化剂 | B.升高反应体系的温度 |
| C.降低反应体系的温度 | D.缩小容器的体积 |
II.氨的催化氧化过程发生以下两种反应,该过程易受催化剂选择性的影响。
①
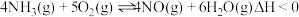
②
在容积固定的密闭容器中充入
 和
和 ,一定时间内,在催化剂作用下发生上述反应。生成物和的物质的量随温度的变化曲线如图。
,一定时间内,在催化剂作用下发生上述反应。生成物和的物质的量随温度的变化曲线如图。
(4)当温度低于400℃时,
 的物质的量增大的幅度高于
的物质的量增大的幅度高于 ,其原因是
,其原因是(5)840℃时,
 的转化率约为
的转化率约为 ,列出520℃反应②平衡常数
,列出520℃反应②平衡常数 的计算式
的计算式
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】已知断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B的键能。如表列出了一些化学键的键能(E):
(1)反应H2(g)+ O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=______ 。
(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
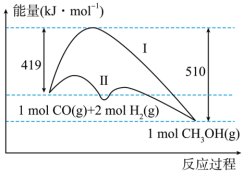
①计算当反应生成1.5molCH3OH(g)时,能量变化值是______ kJ。
②推测反应CH3OH(g) CO(g)+2H2(g)是
CO(g)+2H2(g)是______ (填“吸热”或“放热”)反应。
(3)为发展低碳经济,还有科学家提出可以用氧化锆锌作催化剂,将CO2转化为重要有机原料CH3OH,该反应的化学方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
①表中,a为______ mol。
②由表可知,3~6min内,v(CO2)=______ mol•L-1•min-1。
③对于上述反应,下列叙述正确的是______ 。
A.当各气体的浓度不再改变时,该反应一定已达平衡状态
B.当该反应达到平衡后,n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
C.由表可知,3min时CH3OH的生成速率大于12min时CH3OH的分解速率
| 化学键 | H-H | O=O | O-H |
| E/(kJ•mol-1) | 436 | x | 463 |
 O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
①计算当反应生成1.5molCH3OH(g)时,能量变化值是
②推测反应CH3OH(g)
 CO(g)+2H2(g)是
CO(g)+2H2(g)是(3)为发展低碳经济,还有科学家提出可以用氧化锆锌作催化剂,将CO2转化为重要有机原料CH3OH,该反应的化学方程式为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH) | 0mol | 0.50mol | 0.65mol | 0.75mol | 0.75mol |
| n(CO2) | 1mol | 0.50mol | 0.35mol | a | 0.25mol |
②由表可知,3~6min内,v(CO2)=
③对于上述反应,下列叙述正确的是
A.当各气体的浓度不再改变时,该反应一定已达平衡状态
B.当该反应达到平衡后,n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
C.由表可知,3min时CH3OH的生成速率大于12min时CH3OH的分解速率
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】已知NO2和N2O4之间发生可逆反应: 2NO2 (g) (红棕色)  N2O4(g) (无色)
N2O4(g) (无色)
(1)在烧瓶A和B中盛有相同浓度的NO2与N2O4的混合气体,中间用止水夹夹紧,浸入到盛有水的烧杯中,如图所示。
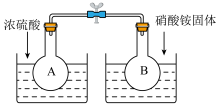
分别向两个烧杯中加入浓硫酸和NH4NO3固体,观察到的现象是:A中气体红棕色加深,B中_____________ 。这说明,当条件改变时,原来的化学平衡将被破坏,并在新的条件下建立起新的平衡,即发生__________ 。
(2)下图是在一定温度下,某固定容积的密闭容器中充入一定量的NO2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是_______________________ 。
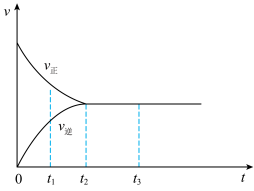
a.t1时,反应未达到平衡, NO2浓度在减小
b.t2时,反应达到平衡,反应不再进行
c.t2~t3,各物质浓度不再变化
d.t2~t3,各物质的浓度相等
e.0~t2,N2O4浓度增大
f.反应过程中气体的颜色不变
(3)某容积2L的密闭容器中充入一定量的NO2和N2O4的混合气体,在一定温度压强下,两者物质的量随时间变化如图所示。
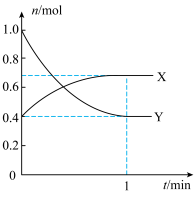
①表示NO2变化的曲线是___ (填“X”或“Y”)。
②在0到1 min内用Y的浓度变化表示的该反应的
反应速率是___ mol·L-1·min-1
 N2O4(g) (无色)
N2O4(g) (无色)(1)在烧瓶A和B中盛有相同浓度的NO2与N2O4的混合气体,中间用止水夹夹紧,浸入到盛有水的烧杯中,如图所示。

分别向两个烧杯中加入浓硫酸和NH4NO3固体,观察到的现象是:A中气体红棕色加深,B中
(2)下图是在一定温度下,某固定容积的密闭容器中充入一定量的NO2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是

a.t1时,反应未达到平衡, NO2浓度在减小
b.t2时,反应达到平衡,反应不再进行
c.t2~t3,各物质浓度不再变化
d.t2~t3,各物质的浓度相等
e.0~t2,N2O4浓度增大
f.反应过程中气体的颜色不变
(3)某容积2L的密闭容器中充入一定量的NO2和N2O4的混合气体,在一定温度压强下,两者物质的量随时间变化如图所示。

①表示NO2变化的曲线是
②在0到1 min内用Y的浓度变化表示的该反应的
反应速率是
您最近一年使用:0次



