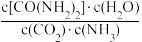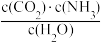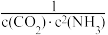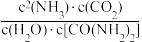铁及其化合物与生产、生活关系密切,已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。若在2L密闭容器中加入0.02mol FeO(s),并通入xmol CO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x的值为( )
Fe(s)+CO2(g)的平衡常数K=0.25。若在2L密闭容器中加入0.02mol FeO(s),并通入xmol CO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x的值为( )
 Fe(s)+CO2(g)的平衡常数K=0.25。若在2L密闭容器中加入0.02mol FeO(s),并通入xmol CO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x的值为( )
Fe(s)+CO2(g)的平衡常数K=0.25。若在2L密闭容器中加入0.02mol FeO(s),并通入xmol CO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x的值为( )A.0.1 | B.0.05 | C.0.04  | D.0.02 |
更新时间:2020-11-25 19:17:13
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】已知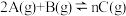 ,在密闭容器中进行,K(300℃)>K(350℃),某温度下,A的平衡转化率(
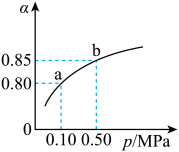
,在密闭容器中进行,K(300℃)>K(350℃),某温度下,A的平衡转化率( )与体系总压强(p)的关系如图所示。下列说法正确的是
)与体系总压强(p)的关系如图所示。下列说法正确的是
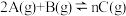 ,在密闭容器中进行,K(300℃)>K(350℃),某温度下,A的平衡转化率(
,在密闭容器中进行,K(300℃)>K(350℃),某温度下,A的平衡转化率( )与体系总压强(p)的关系如图所示。下列说法正确的是
)与体系总压强(p)的关系如图所示。下列说法正确的是
| A.容器内气体的平均相对分子质量不变,说明反应达到化学平衡状态 |
| B.该反应正反应是吸热反应 |
| C.反应温度升高,A的转化率增大 |
| D.平衡状态由a变到b时,平衡正向移动,化学平衡常数K增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】“甲烷还原”可减少 污染。将
污染。将 、
、 、
、 混合物按一定体积比通入恒压容器中,发生如下主要反应:
混合物按一定体积比通入恒压容器中,发生如下主要反应:
①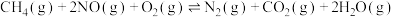

②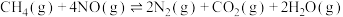

③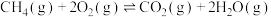
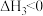
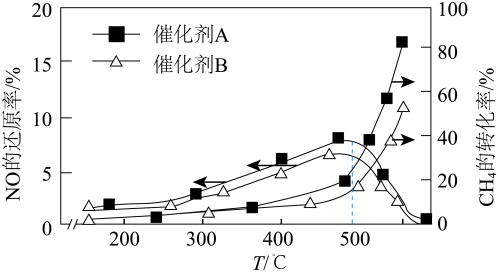
在催化剂A和B的分别作用下, 的还原率和
的还原率和 的转化率和温度的关系分别如图所示。
的转化率和温度的关系分别如图所示。
下列有关说法正确的是
 污染。将
污染。将 、
、 、
、 混合物按一定体积比通入恒压容器中,发生如下主要反应:
混合物按一定体积比通入恒压容器中,发生如下主要反应:①
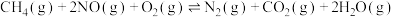

②
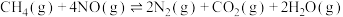

③
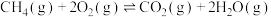
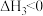
在催化剂A和B的分别作用下,
 的还原率和
的还原率和 的转化率和温度的关系分别如图所示。
的转化率和温度的关系分别如图所示。
下列有关说法正确的是
A.使用催化剂可增大 的平衡转化率 的平衡转化率 |
| B.温度越高,反应②的平衡常数K越大 |
| C.温度高于500℃时,体系中以反应③为主 |
D.由图可知,消除 的最佳条件是500℃和催化剂B 的最佳条件是500℃和催化剂B |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】密闭容器中一定量的混合气体发生反应:mA(g)+nB(g) pC(g),平衡时,测得A的浓度为0.50mol·L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30mol·L-1,有关叙述不正确的是
pC(g),平衡时,测得A的浓度为0.50mol·L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30mol·L-1,有关叙述不正确的是
 pC(g),平衡时,测得A的浓度为0.50mol·L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30mol·L-1,有关叙述不正确的是
pC(g),平衡时,测得A的浓度为0.50mol·L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30mol·L-1,有关叙述不正确的是| A.平衡一定向右移动 | B.B的转化率降低 |
| C.m+n>p | D.C的体积分数降低 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】某固定体积的密闭容器中,加入—定量的A达化学平衡: aA(g) B(g)+c(g),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是
B(g)+c(g),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是
 B(g)+c(g),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是
B(g)+c(g),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是| A.若a=b+c时,B的物质的量分数变大 | B.若a=b+c时,B的物质的量分数不变 |
| C.若a>b+c时,A的转化率不变 | D.若a<b+c时,A的转化率变大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】关于化学平衡常数K的叙述正确的是
| A.K值越大,表示化学反应速率越大 |
| B.对任一可逆反应,温度升高,则K值增大 |
| C.一般情况下K值越大,可逆反应进行得越彻底 |
| D.增大反应物的浓度时,K值增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】制备水煤气的反应
 ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.该反应的反应物的键能总和低于生成物的键能总和 |
| B.为了加快反应速率,可将块状的碳换成粉末状 |
C.该反应的平衡常数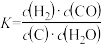 |
D.及时移除部分 , ,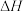 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】向容积为 的真空密闭容器中加入活性炭(足量)和
的真空密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应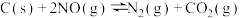
 ,
, 和
和 的物质的量变化如表所示,
的物质的量变化如表所示, ℃、
℃、 ℃下分别达到平衡时容器的总压强分别为
℃下分别达到平衡时容器的总压强分别为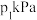 、
、 。说法错误的是
。说法错误的是
 的真空密闭容器中加入活性炭(足量)和
的真空密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应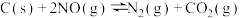
 ,
, 和
和 的物质的量变化如表所示,
的物质的量变化如表所示, ℃、
℃、 ℃下分别达到平衡时容器的总压强分别为
℃下分别达到平衡时容器的总压强分别为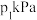 、
、 。说法错误的是
。说法错误的是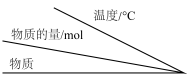 |  |  | |||||
| 0 |  |  |  |  | 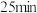 |  | |
 | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
A. ℃时, ℃时,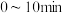 内,以 内,以 表示的反应速率 表示的反应速率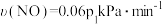 |
B. ℃下,反应的平衡常数为 ℃下,反应的平衡常数为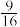 |
C.第 后,温度调整到 后,温度调整到 ℃,数据变化如表所示,则 ℃,数据变化如表所示,则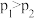 |
D.若 时,保持 时,保持 ℃不变,再加入三种气体物质各 ℃不变,再加入三种气体物质各 ,再次达到平衡时 ,再次达到平衡时 的体积分数为20% 的体积分数为20% |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】乙烯(C2H4)、丙烯(C3H6)、丁烯(C4H8)都是基础化工原料,这三种烯烃之间存在下列三个反应:
反应Ⅰ:3C4H8(g) 4C3H6(g) △H1=+78kJ•mol-1
4C3H6(g) △H1=+78kJ•mol-1
反应Ⅱ:2C3H6(g) 3C2H4(g) △H2=+117kJ•mol-1
3C2H4(g) △H2=+117kJ•mol-1
反应Ⅲ:C4H8(g) 2C2H4(g) △H3
2C2H4(g) △H3
在恒压密闭容器中,反应达到平衡时,三种组分的物质的量分数随温度T的变化关系如图所示。
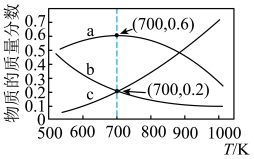
下列说法错误的是
反应Ⅰ:3C4H8(g)
 4C3H6(g) △H1=+78kJ•mol-1
4C3H6(g) △H1=+78kJ•mol-1反应Ⅱ:2C3H6(g)
 3C2H4(g) △H2=+117kJ•mol-1
3C2H4(g) △H2=+117kJ•mol-1反应Ⅲ:C4H8(g)
 2C2H4(g) △H3
2C2H4(g) △H3在恒压密闭容器中,反应达到平衡时,三种组分的物质的量分数随温度T的变化关系如图所示。

下列说法错误的是
| A.反应Ⅲ的△H3=+104kJ•mol-1 |
| B.700K时,反应Ⅱ的物质的量分数的平衡常数K≈2.22×10-2(以物质的量分数代替平衡浓度) |
| C.提高C4H8的物质的量分数,需研发低温条件下活性好且耐高压的催化剂 |
| D.超过700K后曲线a下降的原因可能是随着温度升高反应Ⅰ逆向移动,反应Ⅱ正向移动 |
您最近一年使用:0次
【推荐3】由γ-羟基丁酸( HOCH2CH2CH2COOH)生成γ-丁内酯(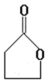 )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH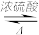
 + H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。
+ H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。
下列说法正确的是
 )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH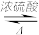
 + H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。
+ H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。| t/ min | 21 | 50 | 80 | 100 | 120 | 160 | ∞ |
| c/( mol·L-1) | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.132 |
A.50~ 100 min内,γ-丁内酯的反应速率为 mol·L-1 mol·L-1 |
B.在120 min时,γ-羟基丁酸的转化率为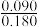 ×100% ×100% |
| C.控制温度、加压和分离产品都可以提高原料的转化率 |
D.25 ℃ 时,该反应的平衡常数为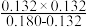 mol·L-1 mol·L-1 |
您最近一年使用:0次

 ,反应:
,反应:

 ,在低温下获得高转化率与高反应速率。反应部分过程如图所示:
,在低温下获得高转化率与高反应速率。反应部分过程如图所示: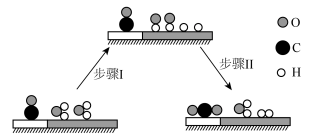

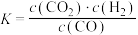
 2C(g)。一段时间后达到平衡,生成amolC。下列说法不正确的是(
2C(g)。一段时间后达到平衡,生成amolC。下列说法不正确的是(
 CO(NH2)2(s)+H2O(1)的平衡常数表达式书写正确的是
CO(NH2)2(s)+H2O(1)的平衡常数表达式书写正确的是