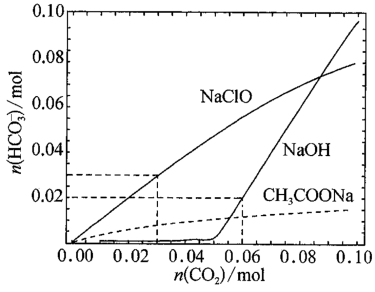
分别向体积均为100mL、浓度均为1mol/L的NaClO、NaOH、CH3COONa的三种溶液中通入CO2,测得各溶液中n( )的变化如下图所示:下列分析正确的是
)的变化如下图所示:下列分析正确的是
 )的变化如下图所示:下列分析正确的是
)的变化如下图所示:下列分析正确的是
A.CO2通入NaClO溶液的反应:2ClO-+CO2+H2O= +2HClO +2HClO |
B.CO2通入CH3COONa溶液的反应:CO2+H2O+CH3COO-= +CH3COOH +CH3COOH |
C.通入n(CO2)=0.06mol时,NaOH溶液中的反应:2OH-+CO2= +H2O +H2O |
D.通入n(CO2)=0.03mol时,三种溶液中:n( )+n( )+n( )+n(H2CO3)=0.03mol )+n(H2CO3)=0.03mol |
更新时间:2020-11-29 19:32:45
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下,向20mL0.1mol•L-1Na2X溶液中缓慢滴加0.1mol•L-1盐酸溶液(不逸出H2X),溶液pH与溶液中lg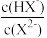 之间关系如图所示。下列说法错误的是( )
之间关系如图所示。下列说法错误的是( )
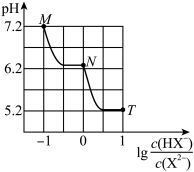
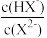 之间关系如图所示。下列说法错误的是( )
之间关系如图所示。下列说法错误的是( )
| A.M点:c(X2-)>c(HX-)>c(OH-)>c(H+) |
| B.常温下,0.1molNa2X和1molNaHX同时溶于水得到溶液pH=5.2 |
| C.N点:c(Na+)<3c(X2-)+c(Cl-) |
| D.常温下,X2-第一步水解常数Kh1的数量级为10-8 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用0.1000mol·L-1醋酸溶液滴定20.00mL0.1000mol·L-1MOH溶液过程中的pH变化曲线如图所示。下列说法正确的是
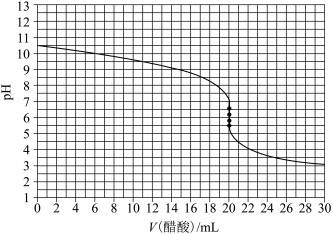

| A.MOH为强碱 |
| B.常温下,MOH的电离常数Kb的数量级为10-4 |
C.V(醋酸)=20.00mL时,混合溶液中: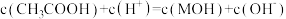 |
D.pH=4时,混合溶液中: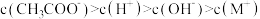 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值。下列说法正确的是
A.1 L 1 mol·L-1的溴化铵水溶液中NH 与H+离子数之和大于NA 与H+离子数之和大于NA |
| B.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同 |
C.1 L 0.1 mol·L-1的氨水中有0.1NA个NH |
| D.0.1 mol·L-1的HClO4溶液中含有的H+数为0.1NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列说法正确的是
A.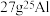 中含有的中子数为12NA 中含有的中子数为12NA |
B.2molNO与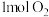 在密闭容器中充分反应后的分子数为2NA 在密闭容器中充分反应后的分子数为2NA |
| C.标准状况下,11.2L由甲烷和乙烯组成的混合气体含极性键的数目为2NA |
D.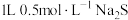 溶液中含 溶液中含 和 和 的离子总数为0.5NA 的离子总数为0.5NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下,将 通入
通入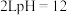 的KOH溶液中。溶液中水电离出的
的KOH溶液中。溶液中水电离出的 离子浓度
离子浓度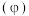 与通入的
与通入的 的体积
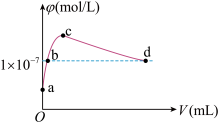
的体积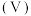 的关系如图所示。下列叙述不正确的是
的关系如图所示。下列叙述不正确的是
 A
A
 通入
通入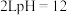 的KOH溶液中。溶液中水电离出的
的KOH溶液中。溶液中水电离出的 离子浓度
离子浓度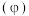 与通入的
与通入的 的体积
的体积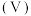 的关系如图所示。下列叙述不正确的是
的关系如图所示。下列叙述不正确的是 A
AA.a点溶液中:水电离出的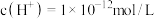 |
B.b点溶液中: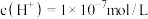 |
C.c点溶液中: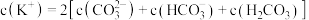 |
D.d点溶液中: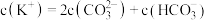 |
您最近半年使用:0次

 )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)

