碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+ Cl2(g)=CH2ClCHClCH3(g) ΔH1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2= CHCH2Cl(g)+HCl(g) ΔH2 = -100 kJ·mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+ HCl(g)=CH2ClCHClCH3(g) ΔH3的逆反应的活化能Ea(逆)为165 kJ·mol-1,则正反应的活化能Ea (正)为______ kJ·mol-1
(2)查阅资料得知:反应CH3CHO(aq)=CH4(g)+CO(g)在含少量I2的溶液中分两步进行:
第I步反应为:CH3CHO(aq)+I2(aq)→CH3(l)+HI(aq)+CO(g) (慢反应)
第II步为快反应,增大I2的浓度能明显增大总反应的平均速率,理由为______ 。
(3)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

在其他条件相同时,催化剂中添加不同Na、K、Cu助剂(助剂也起催化作用)经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
由以上信息可知:在催化剂中添加不同的助剂可改变反应的______ 性,欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加 ______ 助剂效果最好。
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是______ (列举一条)。N点对应温度下,该反应的Kp=______ (MPa)2(Kp为以分压表示的平衡常数)
(5)合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为______ 。

(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+ Cl2(g)=CH2ClCHClCH3(g) ΔH1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2= CHCH2Cl(g)+HCl(g) ΔH2 = -100 kJ·mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+ HCl(g)=CH2ClCHClCH3(g) ΔH3的逆反应的活化能Ea(逆)为165 kJ·mol-1,则正反应的活化能Ea (正)为
(2)查阅资料得知:反应CH3CHO(aq)=CH4(g)+CO(g)在含少量I2的溶液中分两步进行:
第I步反应为:CH3CHO(aq)+I2(aq)→CH3(l)+HI(aq)+CO(g) (慢反应)
第II步为快反应,增大I2的浓度能明显增大总反应的平均速率,理由为
(3)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

在其他条件相同时,催化剂中添加不同Na、K、Cu助剂(助剂也起催化作用)经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
由以上信息可知:在催化剂中添加不同的助剂可改变反应的
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
(5)合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为

更新时间:2020-12-21 20:17:31
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】CO、CO2是化石燃料燃烧后的主要产物。
(1)将等体积的CO2和CO混合气体通入有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃,将残留固体溶于水,所得溶质的化学式是___________________ 。
(2)已知:CO(g)+O2(g) CO2 (g)+O(g) △H1=-33.5kJ·mol─1;
CO2 (g)+O(g) △H1=-33.5kJ·mol─1;
键能E(O=O)=499.0 kJ·mol─1
2CO(g)+O2(g) = 2CO2 (g)的△H2=_____________ kJ·mol─1。
(3)在恒容密闭容器中,控制不同温度进行CO2分解实验:2CO2 (g) 2CO(g)+O2(g)。以CO2起始浓度均为c mol•L─1 测定CO2的转化率,结果如图所示。图中甲曲线表示CO2的平衡转化率与温度的关系,乙曲线表示不同温度下反应10min所测CO2的转化率。
2CO(g)+O2(g)。以CO2起始浓度均为c mol•L─1 测定CO2的转化率,结果如图所示。图中甲曲线表示CO2的平衡转化率与温度的关系,乙曲线表示不同温度下反应10min所测CO2的转化率。

①在1300℃时反应10min到达A点,反应的平均速率v(O2)=________ 。随温度升高,曲线乙向曲线甲靠近的原因是________________________________________ 。要让B点CO2的转化率增大,除升高温度外,还可以采取_______________ 措施(任填一个)。
②下列不能说明上述反应达到平衡状态的是_______________ 。
a.单位时间内生成n mol O2的同时生成2n mol CO; b.混合气体的密度不再改变;
c.CO2的转化率不再变化; d.密闭容器中压强不再改变;
e.混合气体的平均相对分子质量不再改变。
(4)利用电化学还原CO2制取ZnC2O4的示意图如图所示,电解液不参加反应,则Zn与电源的_____ 极相连,Pb极上的电极反应式是_____________________________ 。

(1)将等体积的CO2和CO混合气体通入有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃,将残留固体溶于水,所得溶质的化学式是
(2)已知:CO(g)+O2(g)
 CO2 (g)+O(g) △H1=-33.5kJ·mol─1;
CO2 (g)+O(g) △H1=-33.5kJ·mol─1;键能E(O=O)=499.0 kJ·mol─1
2CO(g)+O2(g) = 2CO2 (g)的△H2=
(3)在恒容密闭容器中,控制不同温度进行CO2分解实验:2CO2 (g)
 2CO(g)+O2(g)。以CO2起始浓度均为c mol•L─1 测定CO2的转化率,结果如图所示。图中甲曲线表示CO2的平衡转化率与温度的关系,乙曲线表示不同温度下反应10min所测CO2的转化率。
2CO(g)+O2(g)。以CO2起始浓度均为c mol•L─1 测定CO2的转化率,结果如图所示。图中甲曲线表示CO2的平衡转化率与温度的关系,乙曲线表示不同温度下反应10min所测CO2的转化率。
①在1300℃时反应10min到达A点,反应的平均速率v(O2)=
②下列不能说明上述反应达到平衡状态的是
a.单位时间内生成n mol O2的同时生成2n mol CO; b.混合气体的密度不再改变;
c.CO2的转化率不再变化; d.密闭容器中压强不再改变;
e.混合气体的平均相对分子质量不再改变。
(4)利用电化学还原CO2制取ZnC2O4的示意图如图所示,电解液不参加反应,则Zn与电源的

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】铁及其化合物在生产、生活中有着广泛的应用。
(1)下图是研究海水对铁闸不同部位腐蚀情况的剖面示意图。

在图中A、B、C、D四个部位中,生成铁锈最多的部位________ (填字母)。
(2)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=
Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=____________ ;t℃时,反应达到平衡时n(CO):n(CO2) =_______ ;t℃时,若在1L密闭容器中加入0.02 mol FeO(s)、xmol CO,发生反应,当反应达到平衡时FeO(s)的转化率为50%,则x=________ 。
(3)高铁酸钾是一种高效、多功能的水处理剂。工业上常采用NaClO氧化法生产,有关
反应原理为:
3NaClO+2Fe(NO3)3+l0NaOH=2Na2FeO4 ↓+3NaCl+6NaNO3+5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
实验证明,反应的温度、原料的浓度及配比对高铁酸钾的产率都有影响。图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图2为一定温度下,NaClO不同质量浓度对K2FeO4生成率的影响。

①工业生产中,反应进行的适宜温度为_________ ℃;此时Fe(NO3)3与NaClO两种溶液的理想的质量浓度之比是____________ 。
②高铁酸钾做水处理剂时的作用主要有__________________ (答出2条即可)。
(1)下图是研究海水对铁闸不同部位腐蚀情况的剖面示意图。

在图中A、B、C、D四个部位中,生成铁锈最多的部位
(2)已知t℃时,反应FeO(s)+CO(g)
 Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=
Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=(3)高铁酸钾是一种高效、多功能的水处理剂。工业上常采用NaClO氧化法生产,有关
反应原理为:
3NaClO+2Fe(NO3)3+l0NaOH=2Na2FeO4 ↓+3NaCl+6NaNO3+5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
实验证明,反应的温度、原料的浓度及配比对高铁酸钾的产率都有影响。图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图2为一定温度下,NaClO不同质量浓度对K2FeO4生成率的影响。

①工业生产中,反应进行的适宜温度为
②高铁酸钾做水处理剂时的作用主要有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式_______ 。该反应需要在加压下进行,原因是_______ 。
(2)已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_______ 。
(3)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应:AsO (aq)+I2(aq)+2OH−(aq)⇌AsO
(aq)+I2(aq)+2OH−(aq)⇌AsO (aq)+2I−(aq)+ H2O(l)。溶液中c(AsO
(aq)+2I−(aq)+ H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
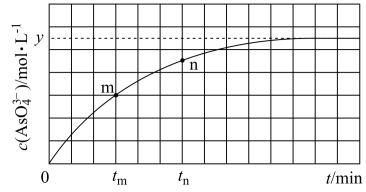
①下列可判断反应达到平衡的是_______ (填标号)。
a.溶液的pH不再变化 b.v(I−)=2v(AsO )
)
c.c(AsO )/c(AsO
)/c(AsO )不再变化 d.c(I−)=y mol·L−1
)不再变化 d.c(I−)=y mol·L−1
②tm时,v正_______ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_______ tn时v逆(填“大于”“小于”或“等于”),理由是_______ 。
④若平衡时溶液的pH=14,则该反应的平衡常数K为_______ 。
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
(2)已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+
 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH22As(s)+
 O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =
(3)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应:AsO
 (aq)+I2(aq)+2OH−(aq)⇌AsO
(aq)+I2(aq)+2OH−(aq)⇌AsO (aq)+2I−(aq)+ H2O(l)。溶液中c(AsO
(aq)+2I−(aq)+ H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化 b.v(I−)=2v(AsO
 )
)c.c(AsO
 )/c(AsO
)/c(AsO )不再变化 d.c(I−)=y mol·L−1
)不再变化 d.c(I−)=y mol·L−1②tm时,v正
③tm时v逆
④若平衡时溶液的pH=14,则该反应的平衡常数K为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)工业生产中可利用 还原
还原 制备清洁能源甲醇。
制备清洁能源甲醇。
①已知 和
和 的燃烧热分别为283.0
的燃烧热分别为283.0 、285.8
、285.8 。
。 与
与 合成甲醇的能量变化如图甲所示,则用
合成甲醇的能量变化如图甲所示,则用 和
和 制备甲醇和液态水的热化学方程式为
制备甲醇和液态水的热化学方程式为_______ 。
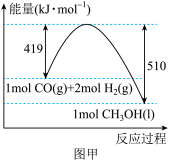
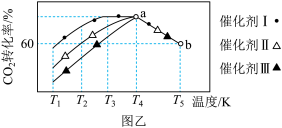
②将一定量的 和
和 充入某恒容密闭容器中,测得在不同催化剂作用下,相同时间内
充入某恒容密闭容器中,测得在不同催化剂作用下,相同时间内 的转化率与温度的变化如图乙所示,该反应在a点达到平衡状态,a点的转化率比b点的高,其原因
的转化率与温度的变化如图乙所示,该反应在a点达到平衡状态,a点的转化率比b点的高,其原因_______ 。
(2)利用 和水蒸气可生产
和水蒸气可生产 ,反应的化学方程式为CO(g)+H2O(g)
,反应的化学方程式为CO(g)+H2O(g)  CO2(g)+H2(g) 。将不同量的
CO2(g)+H2(g) 。将不同量的 和
和 分别通入体积为2L的恒容密闭容器中进行上述反应,得到数据如下表所示
分别通入体积为2L的恒容密闭容器中进行上述反应,得到数据如下表所示
①该反应的正反应为_______ 反应(填“放热”或“吸热”)。
②900℃时,从开始到达平衡时的反应速率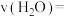
_______ (保留2位小数),达到平衡时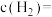
_______ 。
(3)利用废弃的 的热分解可生产
的热分解可生产 :2H2S(g)
:2H2S(g)  2H2(g)+ S2(g)。现将0.20
2H2(g)+ S2(g)。现将0.20
 通入某恒压(压强
通入某恒压(压强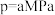 )密闭容器中,在不同温度下测得
)密闭容器中,在不同温度下测得 的平衡转化率如图所示。
的平衡转化率如图所示。
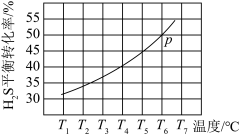
已知:对于气相反应,用某组分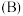 的平衡压强
的平衡压强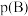 代替物质的量浓度
代替物质的量浓度 也可表示平衡常数。温度为T 6℃时,该反应的平衡常数
也可表示平衡常数。温度为T 6℃时,该反应的平衡常数
_______ (用a的代数式表示)。
(1)工业生产中可利用
 还原
还原 制备清洁能源甲醇。
制备清洁能源甲醇。①已知
 和
和 的燃烧热分别为283.0
的燃烧热分别为283.0 、285.8
、285.8 。
。 与
与 合成甲醇的能量变化如图甲所示,则用
合成甲醇的能量变化如图甲所示,则用 和
和 制备甲醇和液态水的热化学方程式为
制备甲醇和液态水的热化学方程式为

②将一定量的
 和
和 充入某恒容密闭容器中,测得在不同催化剂作用下,相同时间内
充入某恒容密闭容器中,测得在不同催化剂作用下,相同时间内 的转化率与温度的变化如图乙所示,该反应在a点达到平衡状态,a点的转化率比b点的高,其原因
的转化率与温度的变化如图乙所示,该反应在a点达到平衡状态,a点的转化率比b点的高,其原因(2)利用
 和水蒸气可生产
和水蒸气可生产 ,反应的化学方程式为CO(g)+H2O(g)
,反应的化学方程式为CO(g)+H2O(g)  CO2(g)+H2(g) 。将不同量的
CO2(g)+H2(g) 。将不同量的 和
和 分别通入体积为2L的恒容密闭容器中进行上述反应,得到数据如下表所示
分别通入体积为2L的恒容密闭容器中进行上述反应,得到数据如下表所示| 温度/℃ | 起始量 | 达到平衡 | |||
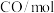 | 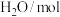 | 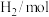 |  转化率 转化率 | 时间/min | |
| 650 | 4 | 2 | 1.6 | 6 | |
| 900 | 3 | 2 |  | 3 | |
②900℃时,从开始到达平衡时的反应速率
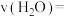
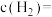
(3)利用废弃的
 的热分解可生产
的热分解可生产 :2H2S(g)
:2H2S(g)  2H2(g)+ S2(g)。现将0.20
2H2(g)+ S2(g)。现将0.20
 通入某恒压(压强
通入某恒压(压强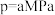 )密闭容器中,在不同温度下测得
)密闭容器中,在不同温度下测得 的平衡转化率如图所示。
的平衡转化率如图所示。
已知:对于气相反应,用某组分
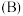 的平衡压强
的平衡压强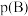 代替物质的量浓度
代替物质的量浓度 也可表示平衡常数。温度为T 6℃时,该反应的平衡常数
也可表示平衡常数。温度为T 6℃时,该反应的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】CO2的充分利用和转化为其他化学品,对于环境和能源等意义重大。回答下列问题:
(1)CO2可制备二甲醚(CH3OCH3),涉及热化学方程式如下:
Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
①反应Ⅰ的
___________  ,该反应的活化能
,该反应的活化能 (正)
(正)___________ (填“大于”或“小于”) (逆)。
(逆)。
②对于反应Ⅱ、Ⅲ,在一定条件下,若反应Ⅱ中,CO2的转化率为98%、反应Ⅲ的转化率为40%,则CH3CH2OH的产率为___________ 。
(2)利用CO2与CH4反应可制备合成气。在恒容密闭容器中通入物质的量均为nmol的CH4与CO2,在一定条件下发生反应 ,测得CO2的平衡转化率与温度及压强的关系如图1所示。
,测得CO2的平衡转化率与温度及压强的关系如图1所示。 、
、 、
、 、
、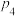 由大到小的顺序为
由大到小的顺序为___________ ,理由是___________ 。
②在压强为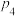 、1100℃的条件下,X点平衡常数
、1100℃的条件下,X点平衡常数
___________ (用含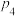 的代数式表示,其中用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
的代数式表示,其中用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)金属Cu/La复合电极材料电催化还原CO2制备甲醛和乙醇的可能机理如图2所示。研究表明,在不同电极材料上形成中间体的部分反应相对能量(活化能)如图3所示。___________ 。
②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原CO2的优点是___________ 。
(1)CO2可制备二甲醚(CH3OCH3),涉及热化学方程式如下:
Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。①反应Ⅰ的

 ,该反应的活化能
,该反应的活化能 (正)
(正) (逆)。
(逆)。②对于反应Ⅱ、Ⅲ,在一定条件下,若反应Ⅱ中,CO2的转化率为98%、反应Ⅲ的转化率为40%,则CH3CH2OH的产率为
(2)利用CO2与CH4反应可制备合成气。在恒容密闭容器中通入物质的量均为nmol的CH4与CO2,在一定条件下发生反应
 ,测得CO2的平衡转化率与温度及压强的关系如图1所示。
,测得CO2的平衡转化率与温度及压强的关系如图1所示。
 、
、 、
、 、
、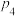 由大到小的顺序为
由大到小的顺序为②在压强为
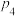 、1100℃的条件下,X点平衡常数
、1100℃的条件下,X点平衡常数
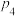 的代数式表示,其中用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
的代数式表示,其中用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(3)金属Cu/La复合电极材料电催化还原CO2制备甲醛和乙醇的可能机理如图2所示。研究表明,在不同电极材料上形成中间体的部分反应相对能量(活化能)如图3所示。

②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原CO2的优点是
您最近一年使用:0次
【推荐3】碳及其含碳化合物在人们的生产生活中应用广泛。
(1)天然气是人们日常生活中的清洁能源。
已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l) △H1=-890.3kJ·mol-1
②2 CO(g)+O2(g)=2CO2(g) △H2=-566 kJ·mol-1
则反应2 CH4(g)+3O2(g)=2CO (g)+4H2O(l)的△H=_____________ 。
(2)甲烷燃料电池的化学方程式为CH4+2O2=CO2+2H2O。某甲烷燃料电池以甲烷为燃料,以空气为氧化剂,以熔融的K2CO3(其中不含O2-和HCO3—)为电解质,以具有催化作用和导电性能的稀土金属为电极。该燃料电池的负极电极反应式为:CH4-8e-+4CO32—=5CO2+2H2O,则其正极电极反应式为____________ ;为使电解质的组成保持稳定,使该燃料电池长时间稳定运行,在通入的空气中必须加入________________ 物质。
(3)以该燃料电池为电源,以铂作电极电解1000g 4.55%的NaOH溶液,一段时间后,溶液中溶质的质量分数变为5.00%,则阳极产生的气体在标准状况下的体积为_______ L。
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
①实验A中以v(H2)表示的反应速率为___________________ 。
②通过计算可知,CO的转化率实验A_______________ 实验B(填“大于”、“等于”或“小于”),该反应的正反应为______________ 热反应(填“吸”或“放”)。
③若实验C要达到与实验B相同的平衡状态,则a、b应满足的关系是_________________ (用含a、b的数学式表示)。
(1)天然气是人们日常生活中的清洁能源。
已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l) △H1=-890.3kJ·mol-1
②2 CO(g)+O2(g)=2CO2(g) △H2=-566 kJ·mol-1
则反应2 CH4(g)+3O2(g)=2CO (g)+4H2O(l)的△H=
(2)甲烷燃料电池的化学方程式为CH4+2O2=CO2+2H2O。某甲烷燃料电池以甲烷为燃料,以空气为氧化剂,以熔融的K2CO3(其中不含O2-和HCO3—)为电解质,以具有催化作用和导电性能的稀土金属为电极。该燃料电池的负极电极反应式为:CH4-8e-+4CO32—=5CO2+2H2O,则其正极电极反应式为
(3)以该燃料电池为电源,以铂作电极电解1000g 4.55%的NaOH溶液,一段时间后,溶液中溶质的质量分数变为5.00%,则阳极产生的气体在标准状况下的体积为
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO2 | CO | |||
| A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| C | 900 | a | b | c | d | t |
①实验A中以v(H2)表示的反应速率为
②通过计算可知,CO的转化率实验A
③若实验C要达到与实验B相同的平衡状态,则a、b应满足的关系是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
根据表中数据判断PM2.5的酸碱性为_______ ,试样的pH=_______ 。
(2)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。已知:
H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
C(s)+ O2(g)=CO(g)ΔH=-110.5kJ·mol-1
O2(g)=CO(g)ΔH=-110.5kJ·mol-1
则C(s)+H2O(g)=CO(g)+H2(g)的ΔH=________ kJ·mol-1。
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g) 2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=
2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=_______ 。汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是________ 。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:_________ 。
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断PM2.5的酸碱性为
(2)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。已知:
H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1C(s)+
 O2(g)=CO(g)ΔH=-110.5kJ·mol-1
O2(g)=CO(g)ΔH=-110.5kJ·mol-1则C(s)+H2O(g)=CO(g)+H2(g)的ΔH=
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)
 2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=
2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】今年,雾霾阴影笼罩全国。二氧化硫、氮氧化物和可吸入颗粒物是雾霾的主要组成成分,综合治理其污染是环境化学当前的重要研究内容。
(1)汽车尾气中的 NO(g)和CO(g)在一定温度和催化剂的条件下可净化。发生的反应如下:2NO(g)+2CO(g) 2CO2 (g)+N2 (g)
2CO2 (g)+N2 (g)
①已知:N2(g)+O2 (g)=2NO(g)ΔH=+180.0 kJ/mol。部分化学键的键能如下(键能指气态原子形成1mol化学键释放的最小能量)
则反应:2NO(g)+2CO(g) 2CO2 (g)+N2 (g) ΔH=
2CO2 (g)+N2 (g) ΔH=__________ kJ/mol
②若上述反应在绝热、恒容的密闭体系中进行,并在t1时刻达到平衡状态,则下列示意图不符合题意的是__________ (填选项序号)。(图中 ω、M、v 正 分别表示质量分数、混合气体平均相对分子质量、正反应速率)

(2)尾气中的SO2可先催化氧化生成SO3,再合成硫酸。已知:2SO2(g)+O2 (g) 2SO3(g) ΔH=-196.0 kJ/mol。
2SO3(g) ΔH=-196.0 kJ/mol。
①在一定温度的密闭容器中,SO2的转化率随时间的变化关系如图所示:

则A点的v逆(SO2 )__________ (填大于、小于或等于)B 点的 v正(SO2)。
②在某温度时,向10L的密闭容器中加入4.0 molSO2和10.0 molO2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平衡浓度和原来平衡浓度相同的是______ (填选项序号)。
A.在其他条件不变时,减小容器的容积
B.保持温度和容器内压强不变,再充入2.0 mol SO2和5.0 mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍
(3)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,其原理如下图所示。

该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用。石墨Ⅱ是电池的____ 极,石墨Ⅰ附近发生的电极反应式为________________________ 。相同条件下,消耗的O2和NO2的体积比为_____ 。
(4)尾气中氮氧化物(NO和NO2 )也可用尿素[CO(NH2)2 ]溶液除去,反应生成对大气无污染的气体。1 mol 尿素能吸收工业尾气中氮氧化物(假设 NO、NO2体积比为 1∶1)的质量为___________ g。
(1)汽车尾气中的 NO(g)和CO(g)在一定温度和催化剂的条件下可净化。发生的反应如下:2NO(g)+2CO(g)
 2CO2 (g)+N2 (g)
2CO2 (g)+N2 (g)①已知:N2(g)+O2 (g)=2NO(g)ΔH=+180.0 kJ/mol。部分化学键的键能如下(键能指气态原子形成1mol化学键释放的最小能量)
| 化学键 | O=O | C O O | C=O |
| 键能(kJ/mol) | 497 | 1072 | 803 |
则反应:2NO(g)+2CO(g)
 2CO2 (g)+N2 (g) ΔH=
2CO2 (g)+N2 (g) ΔH=②若上述反应在绝热、恒容的密闭体系中进行,并在t1时刻达到平衡状态,则下列示意图不符合题意的是

(2)尾气中的SO2可先催化氧化生成SO3,再合成硫酸。已知:2SO2(g)+O2 (g)
 2SO3(g) ΔH=-196.0 kJ/mol。
2SO3(g) ΔH=-196.0 kJ/mol。①在一定温度的密闭容器中,SO2的转化率随时间的变化关系如图所示:

则A点的v逆(SO2 )
②在某温度时,向10L的密闭容器中加入4.0 molSO2和10.0 molO2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平衡浓度和原来平衡浓度相同的是
A.在其他条件不变时,减小容器的容积
B.保持温度和容器内压强不变,再充入2.0 mol SO2和5.0 mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍
(3)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,其原理如下图所示。

该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用。石墨Ⅱ是电池的
(4)尾气中氮氧化物(NO和NO2 )也可用尿素[CO(NH2)2 ]溶液除去,反应生成对大气无污染的气体。1 mol 尿素能吸收工业尾气中氮氧化物(假设 NO、NO2体积比为 1∶1)的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】在加热、加压条件下,利用金属锰的水热反应可将CO2转化为甲酸(HCOOH),转化关系示意图如下:
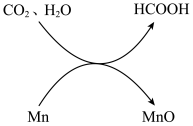
(1)HCOOH的官能团是羧基。HCOOH分子中与碳原子形成共价键的原子的数目是_______ 。
(2)转化过程可认为分两步反应进行:
反应I. Mn + H2O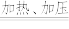 MnO + H2↑; 反应Ⅱ. ……
MnO + H2↑; 反应Ⅱ. ……
写出加热、加压条件下反应Ⅱ的化学方程式:_______ 。
(3)反应一段时间后,生成HCOOH的速率增大,可能的原因是_______ (填字母)。
A.反应放热使温度升高
B.反应I得到的MnO对HCOOH的生成有催化作用
C.H2能将MnO转化为MnO2

(1)HCOOH的官能团是羧基。HCOOH分子中与碳原子形成共价键的原子的数目是
(2)转化过程可认为分两步反应进行:
反应I. Mn + H2O
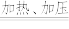 MnO + H2↑; 反应Ⅱ. ……
MnO + H2↑; 反应Ⅱ. ……写出加热、加压条件下反应Ⅱ的化学方程式:
(3)反应一段时间后,生成HCOOH的速率增大,可能的原因是
A.反应放热使温度升高
B.反应I得到的MnO对HCOOH的生成有催化作用
C.H2能将MnO转化为MnO2
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】某研究小组为探讨反应A(g)+2B(g)  2C(g)+D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图:图中C%为反应气体混合物中C的体积百分含量(所有实验的反应时间相同)。
2C(g)+D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图:图中C%为反应气体混合物中C的体积百分含量(所有实验的反应时间相同)。
(1)该反应的反应热为ΔH_____ 0(填“>”、“<”或“=”)。
(2)点M和点N处平衡常数K的大小是:KM______ KN(填“>”、“<”或“=”)。
(3)工业上进行该反应获得产品C的适宜条件是:度为______ ℃,选择该温度的理由是________________ ,压强为______ ,选择该压强的理由是__________________ 。
(4)试解释图中350℃前C%变化平缓而后急剧增大、500℃以后又缓慢增加的可能原因:_____________ 。
 2C(g)+D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图:图中C%为反应气体混合物中C的体积百分含量(所有实验的反应时间相同)。
2C(g)+D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图:图中C%为反应气体混合物中C的体积百分含量(所有实验的反应时间相同)。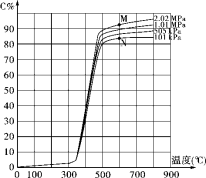
(1)该反应的反应热为ΔH
(2)点M和点N处平衡常数K的大小是:KM
(3)工业上进行该反应获得产品C的适宜条件是:度为
(4)试解释图中350℃前C%变化平缓而后急剧增大、500℃以后又缓慢增加的可能原因:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】科学家利用“组合转化”等技术对CO2进行综合利用。如用H2和CO2在一定条件下可以合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g) △H=akJ/mol(1)
CH2=CH2(g)+4H2O(g) △H=akJ/mol(1)
已知:①H2和CH2=CH2的燃烧热分别为285.8kJ/mol和1411kJ/mol
②H2O(g)=H2O(l) △H=-44kJ/mol
则a=_______ kJ/mol。
(2)不同温度对CO2的转化率及催化剂的效率影响如图所示:

下列有关说法不正确的是_______ (填序号)。
①M点的速率最大
②温度低于250℃时,随温度升高乙烯的产率增大
③M点时平衡常数比N点时平衡常数大
④为提高CO2的转化率应在尽可能低的温度下进行反应
(3)若在密闭容器中充入体积比为3:1的H2和CO2,则图中M点时,产物CH2=CH2的体积分数为_______ (保留二位有效数字);若要进一步提高乙烯的体积分数,可采取的措施有_______ 。
(3)科学家开发了一种新型陶瓷(主要成分为Li4SiO4),在500℃时可高效吸收CO2,同时生成Li2CO3;该材料在700℃时可再生循环。请写出表示该过程的化学方程式_______ 。
 CH2=CH2(g)+4H2O(g) △H=akJ/mol(1)
CH2=CH2(g)+4H2O(g) △H=akJ/mol(1)已知:①H2和CH2=CH2的燃烧热分别为285.8kJ/mol和1411kJ/mol
②H2O(g)=H2O(l) △H=-44kJ/mol
则a=
(2)不同温度对CO2的转化率及催化剂的效率影响如图所示:

下列有关说法不正确的是
①M点的速率最大
②温度低于250℃时,随温度升高乙烯的产率增大
③M点时平衡常数比N点时平衡常数大
④为提高CO2的转化率应在尽可能低的温度下进行反应
(3)若在密闭容器中充入体积比为3:1的H2和CO2,则图中M点时,产物CH2=CH2的体积分数为
(3)科学家开发了一种新型陶瓷(主要成分为Li4SiO4),在500℃时可高效吸收CO2,同时生成Li2CO3;该材料在700℃时可再生循环。请写出表示该过程的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】二氧化锰是化学工业中常用的氧化剂和催化剂。我国主要以贫菱锰矿(有效成分为MnCO3)为原料,通过热解法进行生产。
(1)碳酸锰热解制二氧化锰分两步进行:
i.MnCO3(s) MnO(s)+CO2(g) ΔH1=+a kJ·mol−1
MnO(s)+CO2(g) ΔH1=+a kJ·mol−1
ii.2MnO(s)+O2(g) 2MnO2(s) ΔH2=+b kJ·mol−1
2MnO2(s) ΔH2=+b kJ·mol−1
①反应i的化学平衡常数表达式K=_________ 。
②焙烧MnCO3制取MnO2的热化学方程式是_________ 。
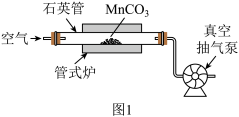
(2)焙烧(装置如图1)时持续通入空气,并不断抽气的目的是_________ 。
(3)在其他条件不变时,某科研团队对影响MnCO3转化率的生产条件进行了研究,结果如图2、图3所示。
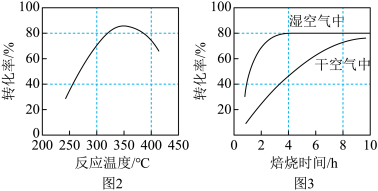
①图2是在常压(0.1 MPa)下的研究结果,请在图2中用虚线画出10 MPa下MnCO3转化率与反应温度的关系图_________ 。
②常压下,要提高MnCO3的转化率,应选择的生产条件是_________ 焙烧6~8h。
(1)碳酸锰热解制二氧化锰分两步进行:
i.MnCO3(s)
 MnO(s)+CO2(g) ΔH1=+a kJ·mol−1
MnO(s)+CO2(g) ΔH1=+a kJ·mol−1ii.2MnO(s)+O2(g)
 2MnO2(s) ΔH2=+b kJ·mol−1
2MnO2(s) ΔH2=+b kJ·mol−1①反应i的化学平衡常数表达式K=
②焙烧MnCO3制取MnO2的热化学方程式是
(2)焙烧(装置如图1)时持续通入空气,并不断抽气的目的是

(3)在其他条件不变时,某科研团队对影响MnCO3转化率的生产条件进行了研究,结果如图2、图3所示。

①图2是在常压(0.1 MPa)下的研究结果,请在图2中用虚线画出10 MPa下MnCO3转化率与反应温度的关系图
②常压下,要提高MnCO3的转化率,应选择的生产条件是
您最近一年使用:0次



