(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为___________ 。又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是___________ kJ。
(2)已知:2NO2(g) N2O4(g) ΔH1 , 2NO2(g)
N2O4(g) ΔH1 , 2NO2(g) N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母)
N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母)___________ 。
A.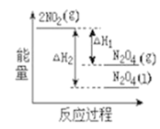 B.
B.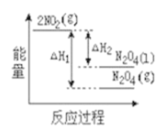 C.
C.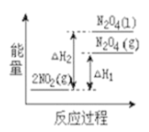
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599 kJ·mol-1
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变(列出简单的表达式并计算结果):___________ 。
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体(结构简式为CH3OH)。 已知某些化学键的键能数据如下表:
已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为___________ 。
(2)已知:2NO2(g)
 N2O4(g) ΔH1 , 2NO2(g)
N2O4(g) ΔH1 , 2NO2(g) N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母)
N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母)A.
 B.
B. C.
C.
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599 kJ·mol-1
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变(列出简单的表达式并计算结果):
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体(结构简式为CH3OH)。 已知某些化学键的键能数据如下表:
| 化学键 | C—C | C—H | H—H | C—O | C≡O | H—O |
| 键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
15-16高二上·江西南昌·阶段练习 查看更多[6]
第一章化学反应的热效应(已下线)第1章 化学反应的热效应(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)江西省宜春市第九中学2020-2021学年高二上学期期中考试化学试题江西省新余市八校2019-2020学年高二上学期期中考试化学试题江西省南康中学2019-2020学年高二上学期期中考试化学试题2015-2016学年江西省南昌二中高二上第一次月考化学试卷
更新时间:2021-01-06 13:28:42
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作做制冷剂等,对臭氧层无破坏作用.工业上以水煤气(CO、H2)为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
2H2(g)+CO(g) CH3OH(g)△H=-90.0kJ·mol-1 ①
CH3OH(g)△H=-90.0kJ·mol-1 ①
2CH3OH(g) CH3OCH(g)+H2O (g)△H=-24.5kJ·mol-1②
CH3OCH(g)+H2O (g)△H=-24.5kJ·mol-1②
CO(g)+H2O(g) CO2(g)+H2(g)△H=-41.1kJ·mol-1③
CO2(g)+H2(g)△H=-41.1kJ·mol-1③
回答下列问题:
(1)新工艺的总反应3H2+3CO CH3OCH3+CO2的热化学方程式为
CH3OCH3+CO2的热化学方程式为____________________ 。
(2)已知一些共价键的键能如下:
运用反应①计算一氧化碳中碳氧共价键的键能____________ kJ•mol-1。
(3)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K=____________ 。
2H2(g)+CO(g)
 CH3OH(g)△H=-90.0kJ·mol-1 ①
CH3OH(g)△H=-90.0kJ·mol-1 ①2CH3OH(g)
 CH3OCH(g)+H2O (g)△H=-24.5kJ·mol-1②
CH3OCH(g)+H2O (g)△H=-24.5kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g)△H=-41.1kJ·mol-1③
CO2(g)+H2(g)△H=-41.1kJ·mol-1③回答下列问题:
(1)新工艺的总反应3H2+3CO
 CH3OCH3+CO2的热化学方程式为
CH3OCH3+CO2的热化学方程式为(2)已知一些共价键的键能如下:
| 化学键 | H-H | C-H | C-O | O-H |
| 键能(kJ·mol-1) | 436 | 414 | 326 | 464 |
运用反应①计算一氧化碳中碳氧共价键的键能
(3)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)25℃、101kPa时,使1.0g乙烯与足量的氧气反应,生成CO2和液态H2O并放出50KJ的热量,表示乙烯燃烧热的热化学方程式为_____________________________________ 。
(2)比较下列热化学方程式中△H的大小关系。
CH4(g)+2O2(g)═CO2(g)+2H2O(l) △H1
CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H2
则△H1____ △H2
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) △H1
2H2(g)+O2(g )=2H2O(l) △H2
2C2H2(g)+5O2(g )=4CO2(g)+2H2O(1) △H3
则2C(s,石墨)+H2(g)=C2H2(g)反应的△H的表达式为:△H=____ 。
(4)已知热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=﹣25kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=﹣48kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+18kJ/mol
写出FeO(s)被CO(g)还原成Fe(g)和CO2(g)的热化学方程式________________ 。
(5)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应N2(g)+3H2(g) 2NH3(g)△H=a kJ/mol。试根据表中所列键能数据计算a为
2NH3(g)△H=a kJ/mol。试根据表中所列键能数据计算a为_______ 。
(6)已知:①Al2O3(s)+3C(s)===2Al(s)+3CO(g) ΔH1=+1 344.1 kJ·mol-1
②2AlCl3(g)===2Al(s)+3Cl2(g) ΔH2=+1 169.2 kJ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为__________________________________________ 。
(1)25℃、101kPa时,使1.0g乙烯与足量的氧气反应,生成CO2和液态H2O并放出50KJ的热量,表示乙烯燃烧热的热化学方程式为
(2)比较下列热化学方程式中△H的大小关系。
CH4(g)+2O2(g)═CO2(g)+2H2O(l) △H1
CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H2
则△H1
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) △H1
2H2(g)+O2(g )=2H2O(l) △H2
2C2H2(g)+5O2(g )=4CO2(g)+2H2O(1) △H3
则2C(s,石墨)+H2(g)=C2H2(g)反应的△H的表达式为:△H=
(4)已知热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=﹣25kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=﹣48kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+18kJ/mol
写出FeO(s)被CO(g)还原成Fe(g)和CO2(g)的热化学方程式
(5)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H-H | N-H | N N N |
| 键能/kJ•mol﹣1 | 436 | 391 | 946 |
 2NH3(g)△H=a kJ/mol。试根据表中所列键能数据计算a为
2NH3(g)△H=a kJ/mol。试根据表中所列键能数据计算a为(6)已知:①Al2O3(s)+3C(s)===2Al(s)+3CO(g) ΔH1=+1 344.1 kJ·mol-1
②2AlCl3(g)===2Al(s)+3Cl2(g) ΔH2=+1 169.2 kJ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)已知拆开 键、
键、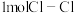 键、
键、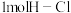 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、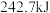 、
、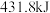 。则由
。则由 和
和 反应生成1molHCl需要
反应生成1molHCl需要_______  填“放出”或“吸收”
填“放出”或“吸收”
_________  的热量。
的热量。
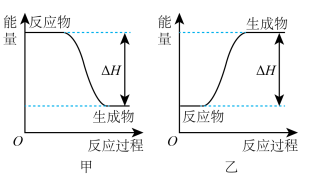
(2)H2可以在 中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图
中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____  填“甲”或“乙”
填“甲”或“乙” 。
。
 键、
键、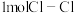 键、
键、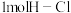 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、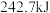 、
、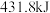 。则由
。则由 和
和 反应生成1molHCl需要
反应生成1molHCl需要 填“放出”或“吸收”
填“放出”或“吸收”
 的热量。
的热量。(2)H2可以在
 中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图
中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图 填“甲”或“乙”
填“甲”或“乙” 。
。
您最近一年使用:0次
【推荐2】汽车尾气主要含有二氧化碳、一氧化碳、二氧化硫、一氧化氮等物质,是造成城市空气污染的主要因素之一。请回答下列问题。
(1)汽车尾气中的一氧化碳来自_____ ,一氧化氮来自_____ 。汽车尾气对环境的危害主要有_____ (至少填两种)。
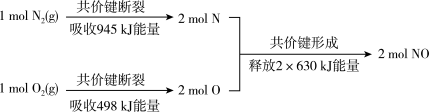
(2)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应_____ (填“释放”或“吸收”)____ kJ能量。
(1)汽车尾气中的一氧化碳来自
(2)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应

您最近一年使用:0次
【推荐3】Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
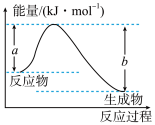
(1)如图表示某反应的能量变化关系,则此反应为___________ (填“吸收”或“放出”) ___________ kJ能量(用含有a、b的关系式表示)。
(2)反应H2(g)+ O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=___________ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为___________ 。
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
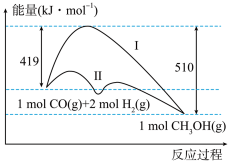
(4)计算当反应生成1.5molCH3OH(g)时,能量变化值是___________ kJ。
(5)推测反应CH3OH(g)⇌CO(g)+2H2(g)是___________ (填“吸热”或“放热”)反应。
Ⅲ.化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示:现提供以下化学键的键能(kJ·mol-1):P-P:198;P-O:360;O=O:498。
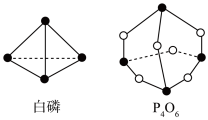
(6)则发生P4(白磷)+3O2(g)=P4O6(s)的反应,其中,生成1 mol P4O6需要___________ (“吸收或放出”)能量为___________ kJ
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |

(1)如图表示某反应的能量变化关系,则此反应为
(2)反应H2(g)+
 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
(4)计算当反应生成1.5molCH3OH(g)时,能量变化值是
(5)推测反应CH3OH(g)⇌CO(g)+2H2(g)是
Ⅲ.化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示:现提供以下化学键的键能(kJ·mol-1):P-P:198;P-O:360;O=O:498。

(6)则发生P4(白磷)+3O2(g)=P4O6(s)的反应,其中,生成1 mol P4O6需要
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】氨在工农业生产中应用广泛。在压强为30MPa时,不同温度时合成氨平衡混合气体中NH3的体积分数如下:
请回答:
(1)根据图中所示,合成氨的热化学方程式为___ 。
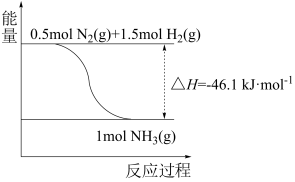
(2)将1molN2(g)和3molH2(g)通入一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量___ 92.2kJ(填“大于”“等于”或“小于”),原因是___ ;若加入催化剂,ΔH___ (填“变大”“变小”或“不变”)。
(3)已知破坏1molN≡N键、1molH—H键需要吸收的能量分别为946kJ、436kJ,则破坏1molN—H键需要吸收的能量为___ kJ。
(4)N2H4可视为NH3分子中的一个H被—NH2取代的产物。发射卫星用N2H4(g)为燃料,以NO2为氧化剂发生反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1。
则1molN2H4与NO2完全反应的热化学方程式为___ 。
| 温度/℃ | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
(1)根据图中所示,合成氨的热化学方程式为

(2)将1molN2(g)和3molH2(g)通入一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量
(3)已知破坏1molN≡N键、1molH—H键需要吸收的能量分别为946kJ、436kJ,则破坏1molN—H键需要吸收的能量为
(4)N2H4可视为NH3分子中的一个H被—NH2取代的产物。发射卫星用N2H4(g)为燃料,以NO2为氧化剂发生反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1。
则1molN2H4与NO2完全反应的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)据报道,我国在南海进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+H2O(g) CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③
则反应①自发进行的条件是___ (填“低温”或“高温”),ΔH3=__ kJ·mol-1。
(2)根据部分键能数据,以及热化学方程式CH4(g)+4F2(g)=CF4(g)+4HF(g) ΔH=-1940kJ·mol-1,计算H—F键的键能为__ kJ·mol-1。
(3)0.1mol的氯气和焦炭、TiO2固体完全反应,生成TiCl4液体和CO气体,放出热量4.28kJ,写出该反应的热化学方程式___ 。
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③则反应①自发进行的条件是
(2)根据部分键能数据,以及热化学方程式CH4(g)+4F2(g)=CF4(g)+4HF(g) ΔH=-1940kJ·mol-1,计算H—F键的键能为
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ·mol-1) | 414 | 489 | ? | 155 |
(3)0.1mol的氯气和焦炭、TiO2固体完全反应,生成TiCl4液体和CO气体,放出热量4.28kJ,写出该反应的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】已知下列热化学方程式:①2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
②C3H8(g)+5O2(g)=3CO2(g) +4H2O(g) △H=-2044.0kJ·mol-1
(1)氢气的燃烧热是__________
(2)已知:H2O(l)=H2O(g) △H=+44.0kJ·mol-1,写出丙烷(C3H8)燃烧生成二氧化碳和液态水的热化学方程式:__________
(3)实验测得H2和C3H8的混合气体共3mol,完全燃烧生成液态水时放热2791.6kJ,计算混合气体中H2和C3H8的体积比是_____
(4)恒温恒容条件下,硫可以发生如下反应,其反应过程和能量关系如图所示,已知2SO2(g)+O2(g)=2SO3(g) △H=-196.6kJ·mol-1
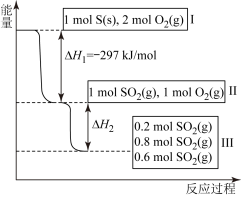
①写出能表示硫的燃烧热的热化学方程式:__________
②△H2=__________ kJ·mol-1
②C3H8(g)+5O2(g)=3CO2(g) +4H2O(g) △H=-2044.0kJ·mol-1
(1)氢气的燃烧热是
(2)已知:H2O(l)=H2O(g) △H=+44.0kJ·mol-1,写出丙烷(C3H8)燃烧生成二氧化碳和液态水的热化学方程式:
(3)实验测得H2和C3H8的混合气体共3mol,完全燃烧生成液态水时放热2791.6kJ,计算混合气体中H2和C3H8的体积比是
(4)恒温恒容条件下,硫可以发生如下反应,其反应过程和能量关系如图所示,已知2SO2(g)+O2(g)=2SO3(g) △H=-196.6kJ·mol-1

①写出能表示硫的燃烧热的热化学方程式:
②△H2=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】通常人们把拆开1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(△H),已知:
则下列热化学方程式不正确 的是___ (把正确的一个选项填在横线上)
a. H2(g)+
H2(g)+ Cl2(g)═HCl(g) △H=﹣91.5kJ•mol﹣1
Cl2(g)═HCl(g) △H=﹣91.5kJ•mol﹣1
b.H2(g)+Cl2(g)═2HCl(g) △H=﹣183kJ•mol﹣1
c.2HCl(g)═H2(g)+Cl2(g) △H=+183kJ•mol﹣1
d. H2(g)+
H2(g)+ Cl2(g)═HCl(g) △H=+91.5kJ•mol﹣1
Cl2(g)═HCl(g) △H=+91.5kJ•mol﹣1
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
则下列热化学方程式
a.
 H2(g)+
H2(g)+ Cl2(g)═HCl(g) △H=﹣91.5kJ•mol﹣1
Cl2(g)═HCl(g) △H=﹣91.5kJ•mol﹣1b.H2(g)+Cl2(g)═2HCl(g) △H=﹣183kJ•mol﹣1
c.2HCl(g)═H2(g)+Cl2(g) △H=+183kJ•mol﹣1
d.
 H2(g)+
H2(g)+ Cl2(g)═HCl(g) △H=+91.5kJ•mol﹣1
Cl2(g)═HCl(g) △H=+91.5kJ•mol﹣1
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是____________ 。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为___ mol,放出的热量为_______ kJ(用含有a和b的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1①
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=__________ 。
(4)已知:N2、O2分子中化学键的键能分别是946kJ·mol−1、497kJ·mol−1。N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol−1。NO分子中化学键的键能为______ 。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1①
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=
(4)已知:N2、O2分子中化学键的键能分别是946kJ·mol−1、497kJ·mol−1。N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol−1。NO分子中化学键的键能为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)已知C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1则0.5 mol丙烷完全燃烧释放的热量为___________ kJ。
(2)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1,2C(s)+O2(g)= 2CO(g) ΔH=-221 kJ·mol-1,写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:___________
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似,化学性质比较活泼。已知断裂1 mol N—N键吸收193 kJ热量,断裂1mol N≡N键吸收941 kJ热量,断裂1 mol N—H键吸收391 kJ热量,断裂1 mol H—H键吸收436 kJ热量,则:
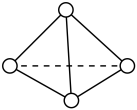
①1 mol N4气体转化为2 mol N2时要放出___________ kJ能量。
②写出N4与H2反应生成NH3的热化学方程式:___________ 。
(4)已知:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。下列反应中能放出57.3 kJ热量的是__________ 。
a.1 L 1 mol·L-1的稀H2SO4与足量NaOH溶液反应
b.稀盐酸与氨水反应生成1 mol H2O
c.稀盐酸与稀Ba(OH)2溶液反应生成1 mol 水
d.稀NaOH与95%浓硫酸反应生成1 mol 水
(2)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1,2C(s)+O2(g)= 2CO(g) ΔH=-221 kJ·mol-1,写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似,化学性质比较活泼。已知断裂1 mol N—N键吸收193 kJ热量,断裂1mol N≡N键吸收941 kJ热量,断裂1 mol N—H键吸收391 kJ热量,断裂1 mol H—H键吸收436 kJ热量,则:

①1 mol N4气体转化为2 mol N2时要放出
②写出N4与H2反应生成NH3的热化学方程式:
(4)已知:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。下列反应中能放出57.3 kJ热量的是
a.1 L 1 mol·L-1的稀H2SO4与足量NaOH溶液反应
b.稀盐酸与氨水反应生成1 mol H2O
c.稀盐酸与稀Ba(OH)2溶液反应生成1 mol 水
d.稀NaOH与95%浓硫酸反应生成1 mol 水
您最近一年使用:0次



