山东“十四五”规划提出“推动绿色发展,绘就绿水青山齐鲁画卷”。CO2加氢可缓解CO2带来的环境压力,同时带来巨大的经济效益。CO2加氢过程,主要发生的三个竞争反应为:
反应Ⅰ:
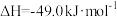
反应Ⅱ: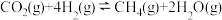

反应Ⅲ:

回答下列问题:
(1)①由CO、H2合成甲醇的热化学方程式为_______ 。
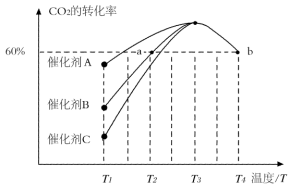
②相同时间内,在不同催化剂下用CO2和H2合成甲醇(其他条件均相同),CO2的转化率随温度变化如图所示,其中活化能最低的反应所用的催化剂是催化剂_______ (填“A”、“B”或“C”)。
③在 催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在
催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在 催化剂表面用“·”标注,
催化剂表面用“·”标注, 表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会
表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会_______ (填“放出热量”或“吸收热量”),反应历程中最小能垒(活化能)步骤的化学方程式为_______ 。

(2)我国科学家研究了不同反应温度对含碳产物组成的影响。在反应器中按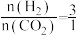 通入
通入 和
和 ,分别在
,分别在 和
和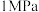 下进行反应。实验中温度对平衡组成体系的(
下进行反应。实验中温度对平衡组成体系的( 、
、 、
、 )三种物质分析,其
)三种物质分析,其 和
和 的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应Ⅰ”,只考虑反应Ⅱ和反应Ⅲ)。
的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应Ⅰ”,只考虑反应Ⅱ和反应Ⅲ)。

①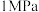 时,表示
时,表示 和
和 平衡组成随温度变化关系的曲线分别是
平衡组成随温度变化关系的曲线分别是_______ 、_______ 。 点平衡组成含量高于
点平衡组成含量高于 点的原因是
点的原因是_______ 。
②当 和
和 平衡组成均为
平衡组成均为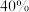 时,该温度下反应Ⅲ的平衡常数
时,该温度下反应Ⅲ的平衡常数 为
为_______ 。
(3) 超干重整
超干重整 得到的
得到的 经偶联反应可制得
经偶联反应可制得 (草酸)。在水溶液中
(草酸)。在水溶液中 、
、 和
和 物质的量分数与
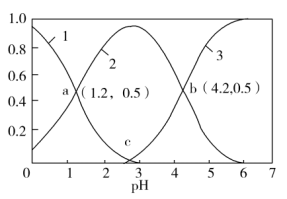
物质的量分数与 关系如图所示,则c点溶液
关系如图所示,则c点溶液
_______ 。
反应Ⅰ:

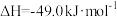
反应Ⅱ:
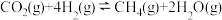

反应Ⅲ:


回答下列问题:
(1)①由CO、H2合成甲醇的热化学方程式为
②相同时间内,在不同催化剂下用CO2和H2合成甲醇(其他条件均相同),CO2的转化率随温度变化如图所示,其中活化能最低的反应所用的催化剂是催化剂

③在
 催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在
催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在 催化剂表面用“·”标注,
催化剂表面用“·”标注, 表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会
表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会
(2)我国科学家研究了不同反应温度对含碳产物组成的影响。在反应器中按
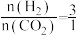 通入
通入 和
和 ,分别在
,分别在 和
和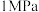 下进行反应。实验中温度对平衡组成体系的(
下进行反应。实验中温度对平衡组成体系的( 、
、 、
、 )三种物质分析,其
)三种物质分析,其 和
和 的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应Ⅰ”,只考虑反应Ⅱ和反应Ⅲ)。
的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应Ⅰ”,只考虑反应Ⅱ和反应Ⅲ)。
①
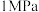 时,表示
时,表示 和
和 平衡组成随温度变化关系的曲线分别是
平衡组成随温度变化关系的曲线分别是 点平衡组成含量高于
点平衡组成含量高于 点的原因是
点的原因是②当
 和
和 平衡组成均为
平衡组成均为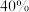 时,该温度下反应Ⅲ的平衡常数
时,该温度下反应Ⅲ的平衡常数 为
为(3)
 超干重整
超干重整 得到的
得到的 经偶联反应可制得
经偶联反应可制得 (草酸)。在水溶液中
(草酸)。在水溶液中 、
、 和
和 物质的量分数与
物质的量分数与 关系如图所示,则c点溶液
关系如图所示,则c点溶液

21-22高三上·山东济宁·期末 查看更多[3]
更新时间:2021-01-07 18:57:00
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】硫酸厂尾气中含有一定量的 SO2,回收并综合利用 SO2对环境保护有重要意义。
(1)利用氨水吸收烟气中的 SO2可转化为(NH4)2SO4。相关反应热化学方程式如下:
SO2(g)+NH3•H2O(aq)=NH4HSO3(aq) ΔH1=akJ•mol-1
NH3•H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l) ΔH2=bkJ•mol-1
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) ΔH3=ckJ•mol-1
①反应 2SO2(g)+4NH3•H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的ΔH3=_______ kJ•mol-1
②空气氧化(NH4)2SO3的速率随温度的变化如图 1 所示,当温度超过 60℃时,(NH4)2SO3氧化速率下降的原因可能是_____ 。研究发现,在 500℃下硫酸铵分解过程中得到 4 种产物,其含氮物质随时间变化关系如图 2 所示。写出该条件下硫酸铵分解的化学方程式: _______ 。

(2)工业上利用 SO2尾气可制备亚硫酰氯(SOCl2)。SOCl2是一种发烟液体,易水解,可用于农药、医药、染料、电池等生产,其制备原理为:S(s)+2Cl2(g)+SO2(g)⇌2SOCl2(g)。
①该反应的平衡常数表达式为____________ 。
②用 SOCl2与 A1Cl3•6H2O 混合共热,可得到无水 A1Cl3,原因是____________ 。
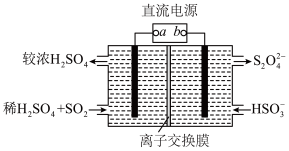
(3)用电解法处理含有 SO2尾气的装置如图所示(电极材料均为惰性电极)。阴极的电极反应式为_________________ 。
(1)利用氨水吸收烟气中的 SO2可转化为(NH4)2SO4。相关反应热化学方程式如下:
SO2(g)+NH3•H2O(aq)=NH4HSO3(aq) ΔH1=akJ•mol-1
NH3•H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l) ΔH2=bkJ•mol-1
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) ΔH3=ckJ•mol-1
①反应 2SO2(g)+4NH3•H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的ΔH3=
②空气氧化(NH4)2SO3的速率随温度的变化如图 1 所示,当温度超过 60℃时,(NH4)2SO3氧化速率下降的原因可能是

(2)工业上利用 SO2尾气可制备亚硫酰氯(SOCl2)。SOCl2是一种发烟液体,易水解,可用于农药、医药、染料、电池等生产,其制备原理为:S(s)+2Cl2(g)+SO2(g)⇌2SOCl2(g)。
①该反应的平衡常数表达式为
②用 SOCl2与 A1Cl3•6H2O 混合共热,可得到无水 A1Cl3,原因是
(3)用电解法处理含有 SO2尾气的装置如图所示(电极材料均为惰性电极)。阴极的电极反应式为

您最近一年使用:0次
【推荐2】Cu2O广泛用作颜料、光敏材料、能源行业催化剂。
(1)已知还原法制备Cu2O的原理为:
N2H4(l)+O2(g) N2(g)+2H2O(l) ΔH=−a kJ· mol−1
N2(g)+2H2O(l) ΔH=−a kJ· mol−1
Cu(OH)2(s) CuO(s)+ H2O(l) ΔH=+b kJ· mol−1
CuO(s)+ H2O(l) ΔH=+b kJ· mol−1
4CuO(s) 2Cu2O (s) +O2(g) ΔH=+c kJ· mol−1
2Cu2O (s) +O2(g) ΔH=+c kJ· mol−1
则由N2H4和Cu(OH)2反应制备Cu2O的热化学方程式为_______________ 。
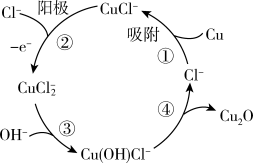
(2)用铜作阳极,钛片作阴极,电解一定浓度的NaCl和NaOH的混合溶液可得到Cu2O,阳极及溶液中物质的有关转化如图所示,阳极的电极反应式为________________ ,每生成14.4 g Cu2O转移电子________ mol。
(3)将CuCl水解再热分解也可得到纳米Cu2O,CuCl水解的反应为CuCl(s)+H2O(l) CuOH(s)+ Cl−(aq)+H+(aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为
CuOH(s)+ Cl−(aq)+H+(aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为________ 。
(4)我国科学家围绕Cu2O材料进行水相CO2光电还原反应合成甲醇,从而探究缓解能源危机和环境污染的方法,其模拟装置原理如图所示:

①在Cu/Cu2O/CuO电极薄膜表面进行CO2还原反应生成CH3OH的总反应是________ 。
②下图是Cu/Cu2O/CuO复合电极在0.1 mol·L−1 NaHCO3溶液中不同电压下的光电催化还原CO2生成甲醇的装置图,下图是产物甲醇的分析。
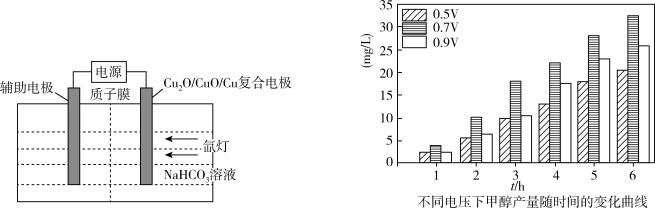
装置中CuO/CuO/Cu复合电极是________ (填“阴极”或“阳极”),光电催化还原CO2生成甲醇最佳电压是________ ,电压增大甲醇含量的降低的原因是________ 。
(1)已知还原法制备Cu2O的原理为:
N2H4(l)+O2(g)
 N2(g)+2H2O(l) ΔH=−a kJ· mol−1
N2(g)+2H2O(l) ΔH=−a kJ· mol−1Cu(OH)2(s)
 CuO(s)+ H2O(l) ΔH=+b kJ· mol−1
CuO(s)+ H2O(l) ΔH=+b kJ· mol−14CuO(s)
 2Cu2O (s) +O2(g) ΔH=+c kJ· mol−1
2Cu2O (s) +O2(g) ΔH=+c kJ· mol−1则由N2H4和Cu(OH)2反应制备Cu2O的热化学方程式为
(2)用铜作阳极,钛片作阴极,电解一定浓度的NaCl和NaOH的混合溶液可得到Cu2O,阳极及溶液中物质的有关转化如图所示,阳极的电极反应式为

(3)将CuCl水解再热分解也可得到纳米Cu2O,CuCl水解的反应为CuCl(s)+H2O(l)
 CuOH(s)+ Cl−(aq)+H+(aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为
CuOH(s)+ Cl−(aq)+H+(aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为(4)我国科学家围绕Cu2O材料进行水相CO2光电还原反应合成甲醇,从而探究缓解能源危机和环境污染的方法,其模拟装置原理如图所示:

①在Cu/Cu2O/CuO电极薄膜表面进行CO2还原反应生成CH3OH的总反应是
②下图是Cu/Cu2O/CuO复合电极在0.1 mol·L−1 NaHCO3溶液中不同电压下的光电催化还原CO2生成甲醇的装置图,下图是产物甲醇的分析。

装置中CuO/CuO/Cu复合电极是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下;
①BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2 kJ·mol-1
②BaS(s)=Ba(s)+S(s)ΔH=+460 kJ·mol-1
已知:③2C(s)+O2(g)=2CO(g)ΔH=-221kJ·mol-1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH =________________ 。
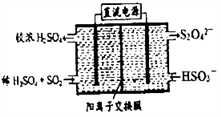
(2)利用下图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。
①阳极的电极反应式为__________________ 。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成。该反应中氧化剂与还原剂的物质的量之比为________________ 。
Ⅱ.乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产。哈斯特研究得出当甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图所示。
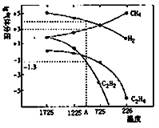
(3)T2℃时,向1L恒容密闭容器中充入0.3molCH4只发生反应2CH4(g) C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH
C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH____ 0(填“>”或“<”),CH4的平衡转化率为_________ 。上述平衡状态某一时刻,若改变温度至T℃,CH4以0.01mol/(L·s)的平均速率增多,经ts后再次达到平衡,平衡时2c(C2H4) = c(CH4),则t=________ s。
(4)计算反应2CH4(g) =C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=_________ (用平衡分压代替平衡浓度计算:lg ≈-1.3)
≈-1.3)
(1)重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下;
①BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2 kJ·mol-1
②BaS(s)=Ba(s)+S(s)ΔH=+460 kJ·mol-1
已知:③2C(s)+O2(g)=2CO(g)ΔH=-221kJ·mol-1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH =
(2)利用下图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。
①阳极的电极反应式为
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成。该反应中氧化剂与还原剂的物质的量之比为

Ⅱ.乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产。哈斯特研究得出当甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图所示。

(3)T2℃时,向1L恒容密闭容器中充入0.3molCH4只发生反应2CH4(g)
 C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH
C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH(4)计算反应2CH4(g) =C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=
 ≈-1.3)
≈-1.3)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】肼( )及其衍生物的合成与利用具有重要意义。
)及其衍生物的合成与利用具有重要意义。
(1)“肼合成酶”以其中的 “配合物为催化中心,可将
“配合物为催化中心,可将 与
与 转化为肼,其反应历程如图所示。
转化为肼,其反应历程如图所示。
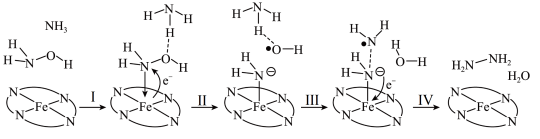
①上图所示的反应步骤Ⅱ、Ⅳ中Fe元素化合价的变化可分别描述为___________ 。
②将 替换为
替换为 ,反应所得产物的化学式为
,反应所得产物的化学式为___________ 。
(2)在碱性条件下,水合肼( )在催化剂Rh(铑)g-
)在催化剂Rh(铑)g- 作用下发生如下分解反应:
作用下发生如下分解反应:
反应Ⅰ: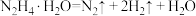
反应Ⅱ: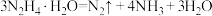
转化频率(TOF)能反映催化剂的性能。
 (t为反应时间)
(t为反应时间)
保持温度不变,相同时间内反应中不同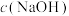 对应的TOF如图所示。
对应的TOF如图所示。
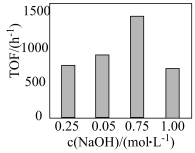
①催化剂载体g- 可由三聚氰胺(
可由三聚氰胺(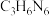 )在空气中焙烧得到。已知
)在空气中焙烧得到。已知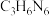 具有六元环结构,其结构简式可表示为
具有六元环结构,其结构简式可表示为___________ 。
②TOF随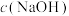 变化的原因是
变化的原因是___________ 。
(3)相同条件下,测得 诱导肼、甲肼(
诱导肼、甲肼(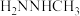 )和偏二甲肼[
)和偏二甲肼[ ]低温反应(均为吸热反应)产物与反应物能量差
]低温反应(均为吸热反应)产物与反应物能量差 、反应速率常数k值(k越大,反应越快)如下表。
、反应速率常数k值(k越大,反应越快)如下表。
①请补充上表所缺反应产物的结构简式___________ 。
②相较甲肼而言,肼、偏二甲肼与 的反应效果不佳的原因分别是
的反应效果不佳的原因分别是___________ 。
 )及其衍生物的合成与利用具有重要意义。
)及其衍生物的合成与利用具有重要意义。(1)“肼合成酶”以其中的
 “配合物为催化中心,可将
“配合物为催化中心,可将 与
与 转化为肼,其反应历程如图所示。
转化为肼,其反应历程如图所示。
①上图所示的反应步骤Ⅱ、Ⅳ中Fe元素化合价的变化可分别描述为
②将
 替换为
替换为 ,反应所得产物的化学式为
,反应所得产物的化学式为(2)在碱性条件下,水合肼(
 )在催化剂Rh(铑)g-
)在催化剂Rh(铑)g- 作用下发生如下分解反应:
作用下发生如下分解反应:反应Ⅰ:
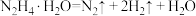
反应Ⅱ:
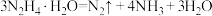
转化频率(TOF)能反映催化剂的性能。
 (t为反应时间)
(t为反应时间)保持温度不变,相同时间内反应中不同
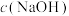 对应的TOF如图所示。
对应的TOF如图所示。
①催化剂载体g-
 可由三聚氰胺(
可由三聚氰胺(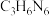 )在空气中焙烧得到。已知
)在空气中焙烧得到。已知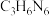 具有六元环结构,其结构简式可表示为
具有六元环结构,其结构简式可表示为②TOF随
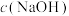 变化的原因是
变化的原因是(3)相同条件下,测得
 诱导肼、甲肼(
诱导肼、甲肼(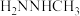 )和偏二甲肼[
)和偏二甲肼[ ]低温反应(均为吸热反应)产物与反应物能量差
]低温反应(均为吸热反应)产物与反应物能量差 、反应速率常数k值(k越大,反应越快)如下表。
、反应速率常数k值(k越大,反应越快)如下表。| 燃料 | 反应产物 |  | k值 |
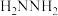 | 5.73 | 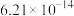 | |
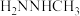 |  | 14.15 | 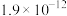 |
 |  | 47.81 | - |
②相较甲肼而言,肼、偏二甲肼与
 的反应效果不佳的原因分别是
的反应效果不佳的原因分别是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】合成氨反应N2(g)+3H2(g) 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。
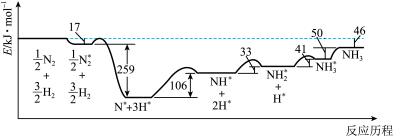
该历程中反应速率最慢的步骤的方程式为________ 。
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:

①以下叙述不能 说明该条件下反应达到平衡状态的是_________ (填字母)。
a.氨气的体积分数保持不变
b.容器中 保持不变
保持不变
c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=________ MPa•min-1,该反应的Kp=_______ MPa-2(保留小数点后两位)。(Kp为以分压表示的平衡常数)
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中_________ 点(填“d”“e”“f”或“g”)。
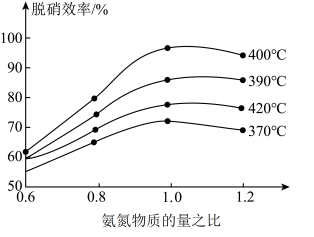
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)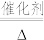 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因_________ 。
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=________ 。
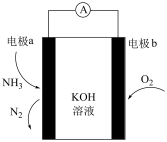
(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:________ 。
 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。

该历程中反应速率最慢的步骤的方程式为
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入
 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:
①以下叙述
a.氨气的体积分数保持不变
b.容器中
 保持不变
保持不变c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)
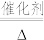 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH
 HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】醋酸是一种重要的基本有机化工原料,主要制取醋酸乙烯单体、VCM、醋酸纤维、聚乙烯醇等。
(1)据文献报道:铑阳离子配合物催化甲醇羰基化反应过程如下图所示。
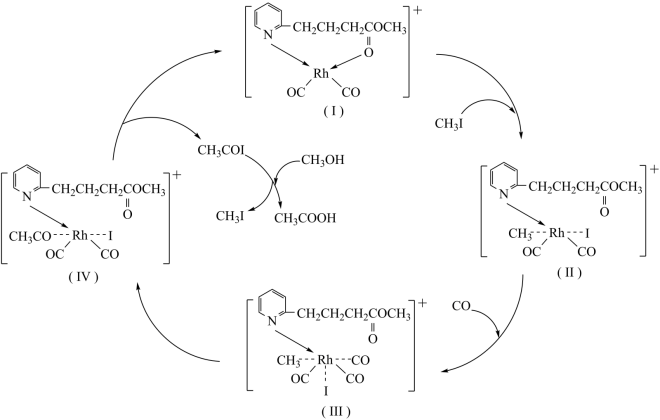
①甲醇羰基化总反应方程式为______ 。
②化合物I转化为II,存在二步机理反应,在不同催化剂a和b催化下各驻点相对能量(kJ·mol-1)如下:
可知化合物I转化为II的∆H______ 0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=______ kJ·mol-1,该条件下更好的催化剂是______ (填“催化剂a”或“催化剂b”),理由为______ 。
(2)140℃时,甲醇羰基化反应除了生成醋酸外,还有醋酸甲酯生成。某密闭容器充入反应物各0.5mol,以甲醇、醋酸甲酯、醋酸三者物质的量分数为纵坐标,其与时间的关系如下图所示。
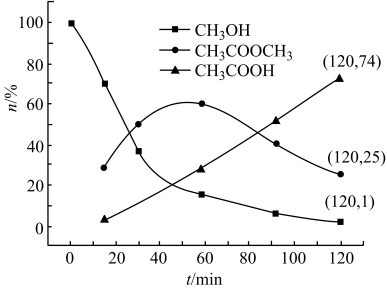
①反应在120min时,醋酸甲酯的物质的量为______ mol。
②反应的选择性,是指发生该反应的甲醇转化率与甲醇总转化率的比率,60min时生成产品醋酸的选择性______ 醋酸甲酯的选择性(填“>”“<”或“=”)。
③如果反应在120min时达到平衡,则CH3COOH(g)+CH3OH(g)⇌CH3COOCH3(g)+H2O(g)平衡常数为______ (保留一位小数)。
(1)据文献报道:铑阳离子配合物催化甲醇羰基化反应过程如下图所示。

①甲醇羰基化总反应方程式为
②化合物I转化为II,存在二步机理反应,在不同催化剂a和b催化下各驻点相对能量(kJ·mol-1)如下:
| 反应物 | 过渡态1 | 1步生成物 | 过渡态2 | 2步生成物 | |
| 催化剂a | 0.00 | 27.53 | 27.35 | 195.09 | 92.63 |
| 催化剂b | 0.00 | 63.93 | 61.86 | 191.88 | 101.04 |
可知化合物I转化为II的∆H
(2)140℃时,甲醇羰基化反应除了生成醋酸外,还有醋酸甲酯生成。某密闭容器充入反应物各0.5mol,以甲醇、醋酸甲酯、醋酸三者物质的量分数为纵坐标,其与时间的关系如下图所示。

①反应在120min时,醋酸甲酯的物质的量为
②反应的选择性,是指发生该反应的甲醇转化率与甲醇总转化率的比率,60min时生成产品醋酸的选择性
③如果反应在120min时达到平衡,则CH3COOH(g)+CH3OH(g)⇌CH3COOCH3(g)+H2O(g)平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】CH4—CO2重整技术是实现碳中和的一种CO2利用技术,具有广阔的市场前景、经济效应和社会意义。该过程中涉及的反应如下:
主反应:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H1=+247.4kJ·mol-1
2CO(g)+2H2(g) △H1=+247.4kJ·mol-1
副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
回答下列问题:
(1)已知:CH4(g)、CO(g)和H2(g)的燃烧热(△H)分别为-890.3kJ·mol-1、-283.0kJ·mol-1、-285.8kJ·mol-1,H2O(l)=H2O(g) △H=+44kJ·mol-1。该副反应的△H2=___ kJ·mol-1。
(2)___ (填标号)有利于提高主反应中CO2的平衡转化率。
A.高温低压 B.低温高压 C.低温低压
(3)800℃,在容积为10L的恒容密闭容器中充入1molCO2和1molCH4发生上述反应,4min后,反应达到平衡,此时测得反应前后总压强之比为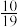 ,H2的物质的量为1.75mol。
,H2的物质的量为1.75mol。
①反应达到平衡时:v(CO2)=___ mol·L-1·min-1,CH4的平衡转化率为___ %,c(CO)=___ mol·L-1。
②副反应的平衡常数K=___ (保留三位有效数字)。
③下列说法正确的是___ (填标号)。
A.当混合气体的密度不再随时间变化时,上述反应达到平衡
B.上述反应达到平衡后,保持其他条件不变,向该容器中充入少量稀有气体,主、副反应的反应速率均不改变
C.当H2O(g)的物质的量浓度不再随时间变化时,上述反应达到平衡
主反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H1=+247.4kJ·mol-1
2CO(g)+2H2(g) △H1=+247.4kJ·mol-1副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2回答下列问题:
(1)已知:CH4(g)、CO(g)和H2(g)的燃烧热(△H)分别为-890.3kJ·mol-1、-283.0kJ·mol-1、-285.8kJ·mol-1,H2O(l)=H2O(g) △H=+44kJ·mol-1。该副反应的△H2=
(2)
A.高温低压 B.低温高压 C.低温低压
(3)800℃,在容积为10L的恒容密闭容器中充入1molCO2和1molCH4发生上述反应,4min后,反应达到平衡,此时测得反应前后总压强之比为
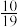 ,H2的物质的量为1.75mol。
,H2的物质的量为1.75mol。①反应达到平衡时:v(CO2)=
②副反应的平衡常数K=
③下列说法正确的是
A.当混合气体的密度不再随时间变化时,上述反应达到平衡
B.上述反应达到平衡后,保持其他条件不变,向该容器中充入少量稀有气体,主、副反应的反应速率均不改变
C.当H2O(g)的物质的量浓度不再随时间变化时,上述反应达到平衡
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。用CO2生产甲醇、乙醇
(1)已知:H2的燃烧热为—285.8kJ/mol,CH3OH(l)的燃烧热为—725.8kJ/mol,CH3OH(g)=CH3OH(l)△H=﹣37.3kJ/mol,则CO2(g)+3H2(g)=CH3OH(g)+H2O(l)△H=_______ kJ/mol。
(2)为探究用CO2生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1molCO2和3.25molH2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
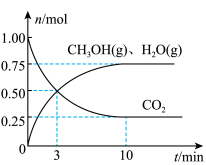
①从反应开始到平衡,氢气的平均反应速率v(H2)=_______ 。
②下列措施能使CO2的平衡转化率增大的是_______ (填序号)。
A.在原容器中再充入1molCO2
B.在原容器中再充入1molH2
C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
F.将水蒸气从体系中分离
(3)CO2也可通过催化加氢合成乙醇,其反应原理为2CO2(g)+6H2(g)=C2H5OH(g)+3H2O(g) △H<0。设m为起始时的投料比,即m= 。通过实验得到如图所示图象:
。通过实验得到如图所示图象:
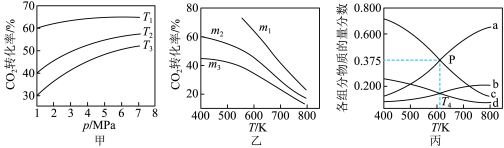
①图甲中投料比相同,温度从高到低的顺序为_______ 。
②图乙中m1、m2、m3从大到小的顺序为_______ 。
③图丙表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系,T4温度时,该反应压强平衡常数Kp的计算式为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,代入数据,不用计算)。
(1)已知:H2的燃烧热为—285.8kJ/mol,CH3OH(l)的燃烧热为—725.8kJ/mol,CH3OH(g)=CH3OH(l)△H=﹣37.3kJ/mol,则CO2(g)+3H2(g)=CH3OH(g)+H2O(l)△H=
(2)为探究用CO2生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1molCO2和3.25molH2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②下列措施能使CO2的平衡转化率增大的是
A.在原容器中再充入1molCO2
B.在原容器中再充入1molH2
C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
F.将水蒸气从体系中分离
(3)CO2也可通过催化加氢合成乙醇,其反应原理为2CO2(g)+6H2(g)=C2H5OH(g)+3H2O(g) △H<0。设m为起始时的投料比,即m=
 。通过实验得到如图所示图象:
。通过实验得到如图所示图象:
①图甲中投料比相同,温度从高到低的顺序为
②图乙中m1、m2、m3从大到小的顺序为
③图丙表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系,T4温度时,该反应压强平衡常数Kp的计算式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气,反应为:C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3kJ·mol-1.,能使该化学反应速率加快的措施有
CO(g)+H2(g) ΔH=+131.3kJ·mol-1.,能使该化学反应速率加快的措施有_______ (填序号)。
①增加C的物质的量 ②升高反应温度 ③增大压强 ④密闭定容容器中充入Ar
(2)将不同物质的量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,得到如下数据:
CO2(g)+H2(g) ΔH<0,得到如下数据:
①以v(CO2)表示的化学反应速率为_______ ,该温度下反应平衡常数K=_______ 。(用分数表示)
②升高体系的温度,则此时的化学反应速率:v(正)_______ v(逆)(填“>”、“=”或“<”)。
(3)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g) CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系如图所示:
CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系如图所示:
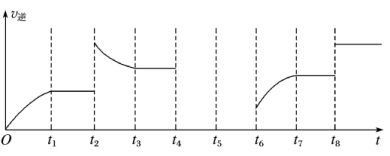
由图可知反应在t1、t3、t7时都达到了平衡,而在t2、t8时都改变了条件,试判断t8时改变的条件可能是_______ 。
(1)将水蒸气通过红热的炭即可产生水煤气,反应为:C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131.3kJ·mol-1.,能使该化学反应速率加快的措施有
CO(g)+H2(g) ΔH=+131.3kJ·mol-1.,能使该化学反应速率加快的措施有①增加C的物质的量 ②升高反应温度 ③增大压强 ④密闭定容容器中充入Ar
(2)将不同物质的量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH<0,得到如下数据:
CO2(g)+H2(g) ΔH<0,得到如下数据:| 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |
| 2 | 4 | 1.6 | 2.4 | 5 |
①以v(CO2)表示的化学反应速率为
②升高体系的温度,则此时的化学反应速率:v(正)
(3)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g)
 CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系如图所示:
CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系如图所示:
由图可知反应在t1、t3、t7时都达到了平衡,而在t2、t8时都改变了条件,试判断t8时改变的条件可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+ CO2(g)=2CO(g)+2H2(g)△H=+247kJ/mol;
①有利于提高CH4平衡转化率的条件是____
A.高温低压B.低温高压C.高温高压D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______ mol2·L−2。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
①由上表判断,催化剂X____ Y(填“优于”或“劣于”),理由是_________________ 。在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是________
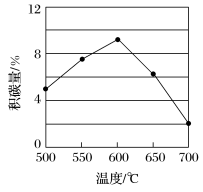
A.K积、K消均增加
B.v积减小,v消增加
C.K积减小,K消增加
D.v消增加的倍数比v积增加的倍数‘
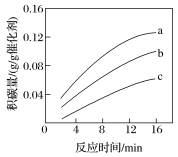
②在一定温度下,测得某催化剂上沉积碳的生成速率方v=k·p(CH4)·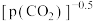 (k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为
(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为________________ 。
(1)CH4-CO2催化重整反应为:CH4(g)+ CO2(g)=2CO(g)+2H2(g)△H=+247kJ/mol;
①有利于提高CH4平衡转化率的条件是
A.高温低压B.低温高压C.高温高压D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
| 积碳反应CH4(g)= C(s)+2H2(g) | 消碳反应CO2(g)+ C(s)= 2CO(g) | ||
| ΔH/(kJ·mol−1) | 75 | 172 | |
| 活化能/(kJ·mol−1) | 催化剂X | 33 | 91 |
| 催化剂Y | 43 | 72 | |
①由上表判断,催化剂X

A.K积、K消均增加
B.v积减小,v消增加
C.K积减小,K消增加
D.v消增加的倍数比v积增加的倍数‘
②在一定温度下,测得某催化剂上沉积碳的生成速率方v=k·p(CH4)·
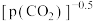 (k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为
(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】(一)醇烃化新技术是近几年合成氨工业净化精炼原料气,除去少量CO一种新方法,其原理可分为甲醇化与甲烷化两个部分。
甲醇化:CO(g)+2H2(g)⇌CH3OH(g))△H1<﹣116kJ•mol﹣1
甲烷化:CO(g)+3H2(g)⇌CH4(g)+H2O(g)△H2<﹣203kJ•mol﹣1
(1)下列措施有利于提高醇烃化过程CO转化率的是_____ 。
A.及时分离出CH3OH B.适当升高反应温度
C.使用高效的催化剂 D.适当增大压强
(2)甲醇化平衡常数 表示,α为平衡组分中各物质的物质的量分数。若CO与H2混合原料气中CO的体积分数为1%,经甲醇化后CO的平衡转化率为w,则Kα=
表示,α为平衡组分中各物质的物质的量分数。若CO与H2混合原料气中CO的体积分数为1%,经甲醇化后CO的平衡转化率为w,则Kα=_____ (用含w的表达式来表示)
(3)测试a、b两种催化剂在不同压强与温度条件下,甲醇化过程中催化效率如图:
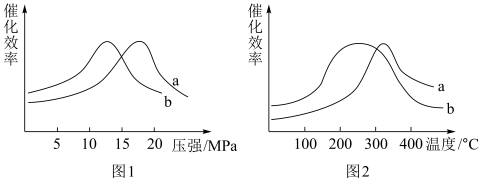
从上图可知选择哪种催化剂较好_____ (填a或b),理由是_____ 。
(4)下列关于醇烃化过程说法正确的是_____ 。
A.甲醇化与甲烷化过程在任何条件下均为自发反应
B.选择不同的催化剂可以控制醇烃化过程中生成甲醇与甲烷的百分含量
C.当温度与反应容器体积一定时,在原料气中加入少量的悄性气体,有利于提高平衡转化率与甲醇的产率
D.适当增大混合气体中H2的百分含量,有利于提高醇烃化过程CO平衡转化率
(二)“五水共治“是浙江治水的成功典范,其中含氮废水处理是污水治理的一个重要课题,图3是高含氰(CN﹣)废水处理方案:
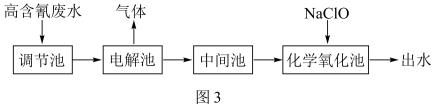
(5)高含氰废水可以通过电解法进行处理,阳极反应分两个阶段,第一阶段电极反应式:CN﹣+2OH﹣﹣2e﹣=CNO﹣+H2O,请写出第二阶段的电极反应式_____ 。
(6)电解后低含氰废水通过化学氧化方法处理:在碱性条件下加入NaClO,将CN﹣氧化为碳酸盐与对环境友好气体。请写出相关离子反应方程式_____ 。
甲醇化:CO(g)+2H2(g)⇌CH3OH(g))△H1<﹣116kJ•mol﹣1
甲烷化:CO(g)+3H2(g)⇌CH4(g)+H2O(g)△H2<﹣203kJ•mol﹣1
(1)下列措施有利于提高醇烃化过程CO转化率的是
A.及时分离出CH3OH B.适当升高反应温度
C.使用高效的催化剂 D.适当增大压强
(2)甲醇化平衡常数
 表示,α为平衡组分中各物质的物质的量分数。若CO与H2混合原料气中CO的体积分数为1%,经甲醇化后CO的平衡转化率为w,则Kα=
表示,α为平衡组分中各物质的物质的量分数。若CO与H2混合原料气中CO的体积分数为1%,经甲醇化后CO的平衡转化率为w,则Kα=(3)测试a、b两种催化剂在不同压强与温度条件下,甲醇化过程中催化效率如图:

从上图可知选择哪种催化剂较好
(4)下列关于醇烃化过程说法正确的是
A.甲醇化与甲烷化过程在任何条件下均为自发反应
B.选择不同的催化剂可以控制醇烃化过程中生成甲醇与甲烷的百分含量
C.当温度与反应容器体积一定时,在原料气中加入少量的悄性气体,有利于提高平衡转化率与甲醇的产率
D.适当增大混合气体中H2的百分含量,有利于提高醇烃化过程CO平衡转化率
(二)“五水共治“是浙江治水的成功典范,其中含氮废水处理是污水治理的一个重要课题,图3是高含氰(CN﹣)废水处理方案:

(5)高含氰废水可以通过电解法进行处理,阳极反应分两个阶段,第一阶段电极反应式:CN﹣+2OH﹣﹣2e﹣=CNO﹣+H2O,请写出第二阶段的电极反应式
(6)电解后低含氰废水通过化学氧化方法处理:在碱性条件下加入NaClO,将CN﹣氧化为碳酸盐与对环境友好气体。请写出相关离子反应方程式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】 经催化加氢可以生成低碳有机物,实现
经催化加氢可以生成低碳有机物,实现 的综合利用和“碳达峰、碳中和”的目标。
的综合利用和“碳达峰、碳中和”的目标。 合成甲醇涉及以下三个反应:
合成甲醇涉及以下三个反应:
①

②

③

已知:反应①、③是低温条件的自发反应。回答下列问题:
(1)上述三个反应的平衡常数 与温度关系如图1所示。图1中c线表示的反应是
与温度关系如图1所示。图1中c线表示的反应是___________ (填“①”、“②”或“③”),
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。 加氢制甲醇反应机理如图2所示。
加氢制甲醇反应机理如图2所示。___________ (填字母)。
A.羧基物种 和甲酸盐物种
和甲酸盐物种 为两种中间体
为两种中间体
B.该反应使用的催化剂既加快了反应速率,又提高了 的平衡转化率
的平衡转化率
C.反应过程中有极性键和非极性键的断裂和形成
(3)某温度下,向一恒容密闭容器中充入等物质的量的 和
和 ,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是
,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是___________ (填字母)。 和
和 )
)
(4)在密闭容器中,充入 和
和 合成
合成 ,发生反应①和②。不同温度下达到平衡时
,发生反应①和②。不同温度下达到平衡时 、
、 及
及 的体积分数如图3所示。
的体积分数如图3所示。 ,则曲线a代表
,则曲线a代表___________ 。
② 时,
时, 的平衡转化率为
的平衡转化率为___________ (保留两位有效数字,下同),此温度下反应②的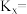
___________ (用平衡物质的量分数代替平衡浓度计算)。
 经催化加氢可以生成低碳有机物,实现
经催化加氢可以生成低碳有机物,实现 的综合利用和“碳达峰、碳中和”的目标。
的综合利用和“碳达峰、碳中和”的目标。 合成甲醇涉及以下三个反应:
合成甲醇涉及以下三个反应:①


②


③


已知:反应①、③是低温条件的自发反应。回答下列问题:
(1)上述三个反应的平衡常数
 与温度关系如图1所示。图1中c线表示的反应是
与温度关系如图1所示。图1中c线表示的反应是
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。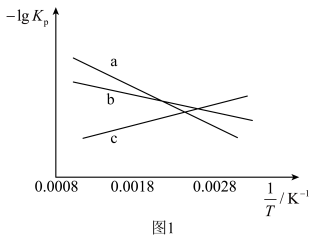
 加氢制甲醇反应机理如图2所示。
加氢制甲醇反应机理如图2所示。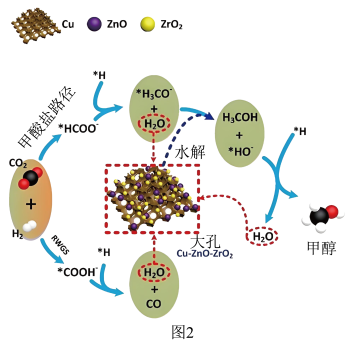
A.羧基物种
 和甲酸盐物种
和甲酸盐物种 为两种中间体
为两种中间体B.该反应使用的催化剂既加快了反应速率,又提高了
 的平衡转化率
的平衡转化率C.反应过程中有极性键和非极性键的断裂和形成
(3)某温度下,向一恒容密闭容器中充入等物质的量的
 和
和 ,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是
,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是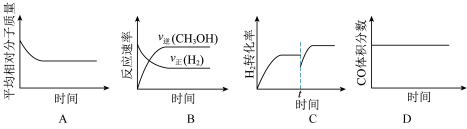
 和
和 )
)(4)在密闭容器中,充入
 和
和 合成
合成 ,发生反应①和②。不同温度下达到平衡时
,发生反应①和②。不同温度下达到平衡时 、
、 及
及 的体积分数如图3所示。
的体积分数如图3所示。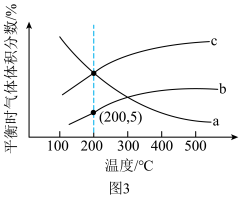
 ,则曲线a代表
,则曲线a代表②
 时,
时, 的平衡转化率为
的平衡转化率为
您最近一年使用:0次



