一定条件下,分别在甲、乙、丙三个恒容密闭容器中加入A和B,发生反应:3A(g)+B(g)⇌2C(g) ∆H>0,448 K时该反应的化学平衡常数K=1,反应体系中各物质的物质的量浓度的相关数据如下:
下列说法不正确 的是
容器 | 温度/K | 起始时物质的浓度/(mol·L−1) | 10分钟时物质的浓度/(mol·L−1) | |
c(A) | c(B) | c(C) | ||
甲 | 448 | 3 | 1 | 0.5 |
乙 | T1 | 3 | 1 | 0.4 |
丙 | 448 | 3 | 2 | a |
| A.甲中,10分钟内A的化学反应速率:υ(A)=0.075 mol·L−1·min−1 |
| B.甲中,10分钟时反应已达到化学平衡状态 |
| C.乙中,T1<448 K、K乙<K甲 |
| D.丙中,达到化学平衡状态时A的转化率大于25% |
21-22高三上·北京西城·期末 查看更多[18]
北京市第一六六中学2023-2024学年高二上学期期中考试化学试卷北京市育才学校2023-2024学年高一上学期化学期中试题北京市和平街第一中学2023-2024学年高二上学期期中考试化学试题北京市顺义区第一中学2023-2024学年高二上学期期中考试化学试题 北京市东直门中学2022-2023学年高二上学期期中考试化学试题北京市第十二中学2022-2023学年高二下学期3月练习化学试题北京市北京师范大学附属中学2022-2023学年高二上学期期中考试化学试题浙江省杭州市源清中学2021-2022学年高二上学期期末考试化学试题(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)辽宁省葫芦岛市普通高中2021-2022学年高三上学期期末学业质量监测化学试题北京市第十五中学2021-2022学年高二上学期期中考试化学试题北京师范大学附属中学2021-2022学年高三上学期期中考试化学试题北京市第四中学2021-2022学年高三上学期期中考试化学试题(已下线)2021年秋季高三化学开学摸底考试卷02(浙江专用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)浙江省金华市义乌市2021届高三适应性考试化学试题天津市第八中学2020-2021学年高三下学期第一次统练化学试题北京市西城区2021届高三上学期期末考试化学试题
更新时间:2021-01-23 22:58:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】 和
和 分别为A、B在两个恒容容器中平衡体系A(g)
分别为A、B在两个恒容容器中平衡体系A(g) 2B(g)和2A(g)
2B(g)和2A(g) B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是
B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是
 和
和 分别为A、B在两个恒容容器中平衡体系A(g)
分别为A、B在两个恒容容器中平衡体系A(g) 2B(g)和2A(g)
2B(g)和2A(g) B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是
B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是A. 、 、 均减小 均减小 | B. 、 、 均增大 均增大 |
C. 减小, 减小, 增大 增大 | D. 增大, 增大, 减小 减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一密闭容器中,反应mA(g) nB(g)+pC(s)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
nB(g)+pC(s)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
 nB(g)+pC(s)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
nB(g)+pC(s)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则| A.m<n+p | B.物质A的转化率减小 |
| C.物质B的质量分数减小 | D.平衡向正反应方向移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在373K时,把0.5 mol N2O4气体通入体积为5 L的恒容密闭容器中,立即出现红棕色。反应进行到2秒时,NO2的浓度为0.02 mol/L。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
| A.v(N2O4)正=2v(NO2)逆时,体系的密度不再发生变化,可判断其处于平衡状态 |
| B.在2秒时体系内的压强为开始时的1.2倍 |
| C.在平衡时体系内含N2O4 0.2 mol |
| D.平衡时,如果再充入一定量N2O4,则可提高N2O4的转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】二甲醚(CH3OCH3)是一种极具发展潜力的有机化工产品和洁净燃料。CO2加氢制二甲醚的反应体系中,主要发生的热化学方程式为反应Ⅰ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH=41.2kJ•mol-1,反应Ⅱ:CO2(g)+3H2(g)
CO(g)+H2O(g) ΔH=41.2kJ•mol-1,反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.5kJ•mol-1,反应Ⅲ:2CH3OH(g)
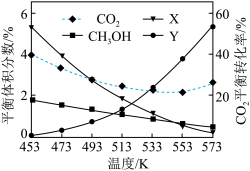
CH3OH(g)+H2O(g) ΔH=-49.5kJ•mol-1,反应Ⅲ:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-23.5kJ•mol-1,在2MPa,起始投料n(H2):n(CO2)=3时,CO2的平衡转化率及CO、CH3OCH3、CH3OH的平衡体积分数随温度变化如图所示。下列有关说法不正确的是
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ•mol-1,在2MPa,起始投料n(H2):n(CO2)=3时,CO2的平衡转化率及CO、CH3OCH3、CH3OH的平衡体积分数随温度变化如图所示。下列有关说法不正确的是
 CO(g)+H2O(g) ΔH=41.2kJ•mol-1,反应Ⅱ:CO2(g)+3H2(g)
CO(g)+H2O(g) ΔH=41.2kJ•mol-1,反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.5kJ•mol-1,反应Ⅲ:2CH3OH(g)
CH3OH(g)+H2O(g) ΔH=-49.5kJ•mol-1,反应Ⅲ:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-23.5kJ•mol-1,在2MPa,起始投料n(H2):n(CO2)=3时,CO2的平衡转化率及CO、CH3OCH3、CH3OH的平衡体积分数随温度变化如图所示。下列有关说法不正确的是
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ•mol-1,在2MPa,起始投料n(H2):n(CO2)=3时,CO2的平衡转化率及CO、CH3OCH3、CH3OH的平衡体积分数随温度变化如图所示。下列有关说法不正确的是
| A.图中X表示CH3OCH3 |
| B.反应Ⅲ中反应物所含化学键的键能之和大于生成物所含化学键的键能之和 |
| C.温度从553K上升至573K时,反应Ⅰ消耗的CO2多于反应Ⅱ生成的CO2 |
| D.其他条件不变,将压强增大到3MPa,可提高平衡时CH3OCH3的体积分数 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】向某密闭容器中充入一定量NO2,发生反应2NO2(g) N2O4(g)。其它条件相同时,不同温度下平衡体系中NO2的物质的量分数如下表,下列说法正确的是
N2O4(g)。其它条件相同时,不同温度下平衡体系中NO2的物质的量分数如下表,下列说法正确的是
 N2O4(g)。其它条件相同时,不同温度下平衡体系中NO2的物质的量分数如下表,下列说法正确的是
N2O4(g)。其它条件相同时,不同温度下平衡体系中NO2的物质的量分数如下表,下列说法正确的是| 温度/℃ | 27 | 35 |
| NO2的物质的量分数% | 20 | 25 |
| A.平衡后,升高温度,正反应速率增大的倍数小于逆反应速率增大的倍数 |
| B.在盛有一定量NO2的注射器中,向外拉活塞,其中气体的颜色会变深 |
| C.27℃平衡时,NO2 和N2O4的物质的量之比为2∶1 |
D.35℃时,NO2的平衡转化率为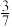 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以下图像对应的叙述正确的是


| A.图甲:A的平衡转化率为50% |
| B.图乙:t1时刻改变的条件只能是加入催化剂 |
| C.图丙:对图中反应升高温度,该反应平衡常数减小 |
| D.图丁:该正向反应在任何温度下都能自发进行 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向甲、乙、丙三个体积均为0.5L的密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:
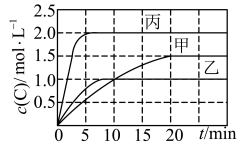
下列说法正确的是( )
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:| 容器 | 甲 | 乙 | 丙 |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5mol A 0.5mol B | 1.5mol A 0.5mol B | 3.0mol A 1.0mol B |

下列说法正确的是( )
| A.10min内甲容器中反应的平均速率v(A)=0.1mol·L-1·min-1 |
| B.x=1 |
| C.由图可知:T1<T2,且该反应为吸热反应 |
| D.T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25% |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度(mol·L-1) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol·L-1) | 0.05 | 0.05 | 0.1 |
| A.反应达平衡时,X的转化率为50% |
B.反应可表示为:X+3Y 2Z,其平衡常数为1 600 2Z,其平衡常数为1 600 |
| C.改变压强可以改变此反应的平衡常数 |
| D.改变温度可以改变此反应的平衡常数 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】利用CH4消除NO2污染,反应原理为CH4(g)+2NO2(g)⇌N2(g)+CO(g)+2H2O(g)。在10L密闭容器中,分别加入0.50molCH4和1.20molNO2,测得控制不同温度,n(CH4)(单位:mol)随时间变化的有关实验数据如表所示,下列说法正确的是
| 组别 | 温度/K | 时间/min 物质的量/mol | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
| A.该反应在高温下才能自发进行 |
| B.T2温度下,若容器内的密度不变则该反应处于平衡状态 |
| C.可以利用40min时的数据,计算T2温度下的平衡常数K |
| D.高温下CH4消除NO2速率较快,所以温度越高越有利于消除NO2 |
您最近半年使用:0次

 2HI,达到平衡时,生成HI 0.8 mol,若其它条件不变,开始充入的H2为2 mol,则达到平衡时生成的HI可能是下列中的
2HI,达到平衡时,生成HI 0.8 mol,若其它条件不变,开始充入的H2为2 mol,则达到平衡时生成的HI可能是下列中的 ,主要用于电子工业及制造塑料中间体,也可用作催化剂。在0.3L的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
,主要用于电子工业及制造塑料中间体,也可用作催化剂。在0.3L的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应: ,已知该反应中CO的平衡转化率与温度的关系如图:下列说法错误的是。
,已知该反应中CO的平衡转化率与温度的关系如图:下列说法错误的是。
 的反应为放热反应
的反应为放热反应
 ,则
,则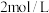
 ,
, 的平衡转化率
的平衡转化率 与体系总压强(p)的关系如图所示。下列说法不正确的是
与体系总压强(p)的关系如图所示。下列说法不正确的是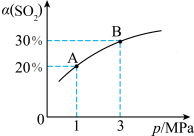
 和
和 置于密闭容器中发生反应,放出的热量小于
置于密闭容器中发生反应,放出的热量小于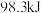
 到
到 时,平衡常数
时,平衡常数
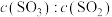 的比值将减小
的比值将减小

