下列关于催化剂和活化能的理解错误的是
| A.催化剂均不参与化学反应 |
| B.催化剂能加快反应速率,但不改变平衡转化率 |
C.溶液中 和 和 的反应瞬间完成,因为其活化能接近零 的反应瞬间完成,因为其活化能接近零 |
| D.岩石在自然界风化的速度很慢,因为该反应在自然条件下活化能较高 |
更新时间:2021-02-01 19:35:22
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】 可催化
可催化 分解,机理,Ⅰ:
分解,机理,Ⅰ: ;Ⅱ:
;Ⅱ: 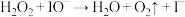 。反应过程中能量变化如图所示,下列判断正确的是
。反应过程中能量变化如图所示,下列判断正确的是
 可催化
可催化 分解,机理,Ⅰ:
分解,机理,Ⅰ: ;Ⅱ:
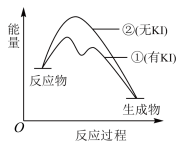
;Ⅱ: 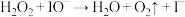 。反应过程中能量变化如图所示,下列判断正确的是
。反应过程中能量变化如图所示,下列判断正确的是
A. 是放热反应 是放热反应 | B. 分解反应的速率由机理Ⅰ决定 分解反应的速率由机理Ⅰ决定 |
C.KI能改变总反应的 | D. 不改变 不改变 分解反应的途径 分解反应的途径 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】科学家研究发现,在催化剂作用下,合成氨及氨的催化氧化反应的转化过程如下图所示:
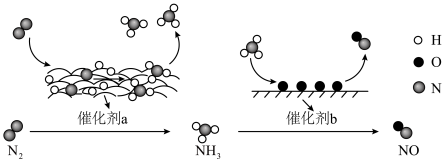
下列说法正确的是

下列说法正确的是
| A.催化剂a能提高合成氨反应的反应速率和平衡转化率 |
| B.催化剂a表面氮的吸附分解所需活化能高,是控制反应速率的关键步骤 |
| C.催化剂b表面反应生成NO时没有电子转移 |
| D.两个反应的原子利用率均为100% |
您最近一年使用:0次
【推荐3】SO2(g)+O2(g)→SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述正确的是


| A.该反应的逆反应为吸热反应,SO2的能量一定高于SO3的能量 |
| B.该反应中,反应物的总键能小于生成物的总键能 |
| C.ΔH=E2-E1,使用催化剂改变活化能,但不改变反应热 |
D.500℃、101kPa下,将1mol SO2(g)和0.5mol O2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g) 2SO3(g) ΔH=-2akJ·mol-1 2SO3(g) ΔH=-2akJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】汽车尾气包括CO、碳氢化合物、NOx(氮氧化合物)等,三元催化器中净化原理如图所示。下列说法正确的是
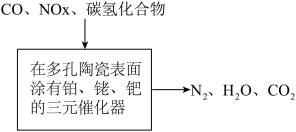

| A.铂、铑、钯属于主族元素 |
| B.三元催化器中的催化剂可降低该反应的活化能 |
| C.三元催化器中的多孔陶瓷可提高平衡时反应物的转化率 |
| D.在反应NO+CO→N2+CO2中,每生成1molN2时转移2mol电子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】某种含二价铜微粒[CuII(OH)(NH3)]+的催化剂可用于汽车尾气脱硝,催化机理如图所示,下列说法正确的是
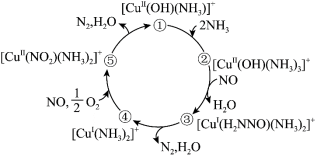

| A.[CuII(OH)(NH3)]+可降低该反应的活化能 |
| B.状态②到状态③的过程中N元素被还原 |
| C.状态③到状态④的过程中有O-H键的断裂 |
D.该脱硝过程的总反应方程式为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列实验操作和现象与结论关系不正确 的是
| 操作和现象 | 结论 | |
| A | 将铝片放入盐酸中,产生气泡的速率开始时较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
| B | 将大小相同的K和Na放入等体积的水中,钾比钠反应剧烈 | 钾元素的金属性比钠元素强 |
| C | 漂白粉与浓HCl混合产生的气体能使湿润蓝色石蕊试纸先变红后褪色 | 漂白粉和浓HCl反应生成Cl2 |
| D | 向盛有H2O2溶液的试管中,加入少量FeCl3溶液,产生气泡的速率比不加FeCl3溶液的快 | FeCl3可以加快H2O2分解的速率,起了催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列事实,不能用勒夏特列原理解释的是
|
|
|
|
| A.气体在热水中比在冷水中颜色深 | B.平衡体系加压后颜色变深 | C.加压后气体颜色先变深后变浅 | D.用浓氨水和NaOH固体制取氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列事实不能用化学平衡移动原理解释的是
| A.用饱和食盐水除去氯气中混有的氯化氢气体 |
| B.合成三氧化硫时用五氧化二钒提高生产效率 |
| C.用浓氨水和生石灰固体快速制取氨气 |
| D.在酯化反应中,为了提高乙酸的转化率,常采用过量的乙醇 |
您最近一年使用:0次





 H2(g)+I2(g),增大压强(缩小容积)可使颜色变深
H2(g)+I2(g),增大压强(缩小容积)可使颜色变深

