某恒温密闭容器中,可逆反应A(s)⇌B+C(g)该反应为放热反应达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
| A.产物B的状态只能为固态或液态 |
| B.平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 |
| C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 |
| D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q |
更新时间:2021-02-04 10:29:32
|
相似题推荐
多选题
|
较易
(0.85)
【推荐1】下列说法错误的是
| A.化学平衡常数改变,化学平衡一定发生移动 |
B.恒温恒容条件下,反应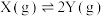 达平衡后再充入 达平衡后再充入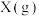 ,平衡向正反应方向移动 ,平衡向正反应方向移动 |
C.25℃时某容器中发生: ,当各组分物质的量不再变化时,达到化学平衡状态 ,当各组分物质的量不再变化时,达到化学平衡状态 |
D.实际生产中,反应 的条件为400~500℃、常压、合适的催化剂 的条件为400~500℃、常压、合适的催化剂 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐2】 ,在容积不变的密闭容器中发生反应:
,在容积不变的密闭容器中发生反应: ,实验测得
,实验测得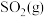 的物质的量浓度
的物质的量浓度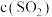 (单位:
(单位: )随反应时间t(单位:
)随反应时间t(单位: )的关系如图所示。下列说法正确的是
)的关系如图所示。下列说法正确的是
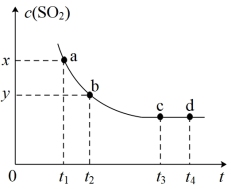
 ,在容积不变的密闭容器中发生反应:
,在容积不变的密闭容器中发生反应: ,实验测得
,实验测得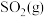 的物质的量浓度
的物质的量浓度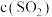 (单位:
(单位: )随反应时间t(单位:
)随反应时间t(单位: )的关系如图所示。下列说法正确的是
)的关系如图所示。下列说法正确的是
A. 时间内用 时间内用 表示的平均反应速率 表示的平均反应速率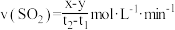 |
B. 点与 点与 点的正反应速率: 点的正反应速率: |
C. 点的反应速率: 点的反应速率: |
D. 点对应的容器中: 点对应的容器中: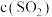 一定等于 一定等于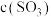 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
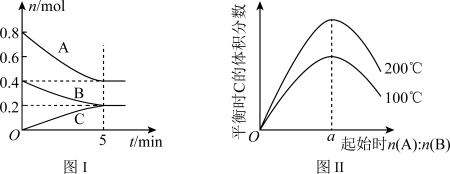
【推荐1】在体积为2L的恒容密闭容器中发生反应 ,图Ⅰ表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
,图Ⅰ表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
 ,图Ⅰ表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
,图Ⅰ表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率 |
B.图Ⅱ所知反应 的△H>0,且a=2 的△H>0,且a=2 |
| C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆) |
| D.200℃时,向容器中充入2molA和1molB,达到平衡时,A的体积分数小于0.5 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐2】在密闭容器中的一定量混合气体发生反应:xA(g)+ yB(g) zC(g),平衡时测得 A 的浓度为 0.5mol/L,保持温度不变,将容器容积缩小到原来的一半,再达到平衡时,测得 A 的 浓度为 0.9 mol/L。下列有关判断不正确的是( )
zC(g),平衡时测得 A 的浓度为 0.5mol/L,保持温度不变,将容器容积缩小到原来的一半,再达到平衡时,测得 A 的 浓度为 0.9 mol/L。下列有关判断不正确的是( )
 zC(g),平衡时测得 A 的浓度为 0.5mol/L,保持温度不变,将容器容积缩小到原来的一半,再达到平衡时,测得 A 的 浓度为 0.9 mol/L。下列有关判断不正确的是( )
zC(g),平衡时测得 A 的浓度为 0.5mol/L,保持温度不变,将容器容积缩小到原来的一半,再达到平衡时,测得 A 的 浓度为 0.9 mol/L。下列有关判断不正确的是( )| A.x+ y < z | B.平衡向正反应方向移动 |
| C.A 的转化率降低 | D.C 的体积分数增大 |
您最近一年使用:0次
多选题
|
较易
(0.85)
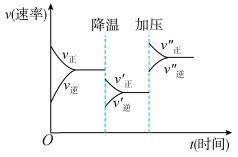
【推荐3】如图表示的是可逆反应A+2B 2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
 2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
| A.该反应的正反应是吸热反应 |
| B.若A,B是气体,则D一定是纯液体或固体 |
C.该反应的平衡常数始终没变 |
| D.A的转化率最终增大 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐1】如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在烧杯(1)中加入CaO,在烧杯(2)中不加其他物质,烧杯(3)中加入NH4Cl,发现烧瓶(1)中红棕色变深,烧瓶(3)中红棕色变浅。[已知反应2NO2(红棕色)⇌N2O4(无色)],下列叙述正确的是


| A.2NO2⇌N2O4是放热反应 |
| B.NH4Cl溶于水时放出热量 |
| C.烧瓶(1)中混合气体的平均相对分子质量减小 |
| D.烧瓶(3)中气体的压强增大 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】下列有关合成氨工业的叙述,可用勒夏特列原理来解释的是
A.使用铁触媒,使 和 和 混合气体有利于合成氨 混合气体有利于合成氨 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.700K左右比室温更有利于合成氨的反应 |
| D.合成氨时采用循环操作,可提高原料的利用率 |
您最近一年使用:0次



