将CO2转化成C2H4可以变废为宝、改善环境。以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
C2H6(g)=CH4(g)+H2(g)+C(s) △H=+9kJ•mol-1
C2H4(g)+H2(g)=C2H6(g) △H=-136kJ•mol-1
H2(g)+CO2(g)=H2O(g)+CO(g) △H=+41kJ•mol-1
(1)CO2、C2H6为原料合成C2H4的主要反应CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g)△H=__ ;任意写出两点加快该反应速率的方法:__ 、___ 。
(2)0.1MPa时向密闭容器中充入CO2和C2H6,发生反应CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g),温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示:
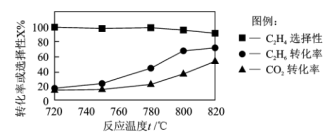
①工业生产综合各方面的因素,反应选择800℃的原因是___ 。
②C2H6的转化率随着温度的升高始终高于CO2的原因是___ 。
③800℃时,随着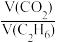 的比值增大,CO2转化率将
的比值增大,CO2转化率将__ (填“增大”或“减小”)。
(3)在800℃时,n(CO2):n(C2H6)=1:3,充入一定体积的密闭容器中,在有催化剂存在的条件下,发生反应CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g),初始压强为P0,一段时间达到平衡,产物的物质的量分数之和与剩余反应物的物质的量分数之和相等,该温度下反应的平衡常数Kp__ P0(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用最简分式表示)。
C2H6(g)=CH4(g)+H2(g)+C(s) △H=+9kJ•mol-1
C2H4(g)+H2(g)=C2H6(g) △H=-136kJ•mol-1
H2(g)+CO2(g)=H2O(g)+CO(g) △H=+41kJ•mol-1
(1)CO2、C2H6为原料合成C2H4的主要反应CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g)△H=
(2)0.1MPa时向密闭容器中充入CO2和C2H6,发生反应CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g),温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示:

①工业生产综合各方面的因素,反应选择800℃的原因是
②C2H6的转化率随着温度的升高始终高于CO2的原因是
③800℃时,随着
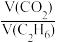 的比值增大,CO2转化率将
的比值增大,CO2转化率将(3)在800℃时,n(CO2):n(C2H6)=1:3,充入一定体积的密闭容器中,在有催化剂存在的条件下,发生反应CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g),初始压强为P0,一段时间达到平衡,产物的物质的量分数之和与剩余反应物的物质的量分数之和相等,该温度下反应的平衡常数Kp
更新时间:2021-03-17 18:43:50
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示(条件及物质未标出)。

(1)已知: 、CO、
、CO、 的标准燃烧热(ΔH)分别为
的标准燃烧热(ΔH)分别为 、
、 、
、 ,则上述流程中第一步反应
,则上述流程中第一步反应 的
的
___________ 。
(2)工业中 和
和 制备甲醇的方程式为
制备甲醇的方程式为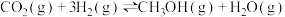 ,某温度下,将
,某温度下,将 和
和 充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下 的平衡转化率为
的平衡转化率为___________ 。
(3)某温度下,将 和
和 按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得
按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
___________  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4) 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: 。在0.1MPa时,按
。在0.1MPa时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
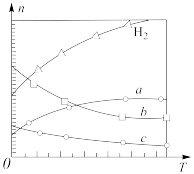
①该反应的ΔH___________ (填“>”或“<”)。
②曲线c表示的物质为___________ 。
③为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是___________ 。

(1)已知:
 、CO、
、CO、 的标准燃烧热(ΔH)分别为
的标准燃烧热(ΔH)分别为 、
、 、
、 ,则上述流程中第一步反应
,则上述流程中第一步反应 的
的
(2)工业中
 和
和 制备甲醇的方程式为
制备甲醇的方程式为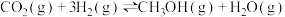 ,某温度下,将
,某温度下,将 和
和 充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下 的平衡转化率为
的平衡转化率为| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
 | 0.90 | 0.85 | 0.836 | 0.81 | 0.80 | 0.80 |
 和
和 按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得
按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)
 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: 。在0.1MPa时,按
。在0.1MPa时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
①该反应的ΔH
②曲线c表示的物质为
③为提高
 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】(12分)新型洁净能源能够解决环境污染、能源短缺等问题,真正把“绿水青山就是金山银山”落实到我国的各个角落。氢气作为清洁高效、可持续“零碳”能源被广泛研究,而水煤气变换反应(WGSR)是一个重要的制氢手段。
(1)WGSR的氧化还原机理和羧基机理如图所示。则热化学方程式CO(g)+H2O(g)=CO2(g)+H2(g) ΔH中,对ΔH表述错误的是________ (填字母)。

A.氧化还原机理途径:ΔH=ΔH1+ΔH2+ΔH5a+ΔH7
B.羧基机理途径:ΔH=ΔH1+ΔH4+ΔH5d+ΔH7
C.氧化还原机理途径:ΔH=ΔH1+ΔH3+ΔH5a+ΔH7
D.羧基机理途径:ΔH=ΔH1+ΔH4+ΔH5c+ΔH7
E.ΔH=ΔH1+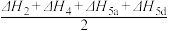 +ΔH7
+ΔH7
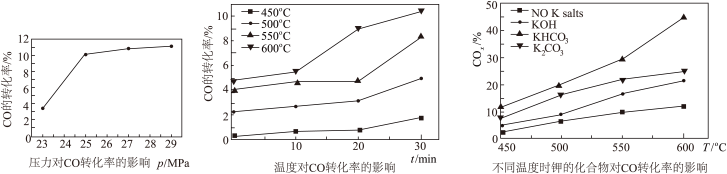
(2)水煤气变换反应在不同条件时CO的转化率不同,下图为压力、温度、不同温度时钾的化合物对CO的转化率的影响关系图,请认真观察图中信息,结合自己所学知识及生产实际,写出水煤气变换反应的条件:温度选择________ ℃;钾的化合物中_______ 催化效果最明显;压力选择______ Mpa,选用此压力的原因为________ 。
(3)如图是Au12Cu、Au12Pt、Au12Ni三种催化剂在合金团簇上WGSR最佳反应路径的基元反应能量图,反应能垒(活化能)最_______ (填“高”或“低”)的步骤,为整个反应的速控步骤;三种催化剂催化反应的速控步骤__________ (填“相同”或“不相同”);三种催化剂中,___________ 在合金团簇上的WGSR各基元反应能垒较小,对WGSR表现出较好的催化活性。

(4)已知某密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3,则K1、K2、K3由小到大的关系为
CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3,则K1、K2、K3由小到大的关系为____________ 。
(1)WGSR的氧化还原机理和羧基机理如图所示。则热化学方程式CO(g)+H2O(g)=CO2(g)+H2(g) ΔH中,对ΔH表述错误的是

A.氧化还原机理途径:ΔH=ΔH1+ΔH2+ΔH5a+ΔH7
B.羧基机理途径:ΔH=ΔH1+ΔH4+ΔH5d+ΔH7
C.氧化还原机理途径:ΔH=ΔH1+ΔH3+ΔH5a+ΔH7
D.羧基机理途径:ΔH=ΔH1+ΔH4+ΔH5c+ΔH7
E.ΔH=ΔH1+
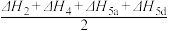 +ΔH7
+ΔH7(2)水煤气变换反应在不同条件时CO的转化率不同,下图为压力、温度、不同温度时钾的化合物对CO的转化率的影响关系图,请认真观察图中信息,结合自己所学知识及生产实际,写出水煤气变换反应的条件:温度选择

(3)如图是Au12Cu、Au12Pt、Au12Ni三种催化剂在合金团簇上WGSR最佳反应路径的基元反应能量图,反应能垒(活化能)最

(4)已知某密闭容器中存在下列平衡:CO(g)+H2O(g)
 CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3,则K1、K2、K3由小到大的关系为
CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3,则K1、K2、K3由小到大的关系为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求,依靠理论知识做基础。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:K=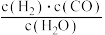 它所对应的化学反应为:
它所对应的化学反应为:___________ 。
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g) △H =-90.8 kJ/mol
CH3OH(g) △H =-90.8 kJ/mol
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol
CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol
③CO(g)+H2O(g) CO2(g)+H2(g) △H =-41.3 kJ/mol
CO2(g)+H2(g) △H =-41.3 kJ/mol
总反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g) 的△H =
CH3OCH3(g)+CO2(g) 的△H =___________ ;
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
该反应的正反应方向是___________ 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为 0.020 mol/L,在该条件下,CO的平衡转化率为:___________ 。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如 NO、NO2、N2O4等,对反应N2O4(g) 2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是
2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是___________ 。

A A、C 两点的反应速率:A>C
B A、C 两点气体的颜色:A 深,C浅
C A、C 两点的化学平衡常数:A>C
D 由状态 B 到状态 A,可以用加热的方法
(5)NO2可用氨水吸收生成NH4NO3,25℃时,将m mol NH4NO3溶于水,溶液显酸性,向该溶液滴加 n L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将___________ (填“正向”“不”或“逆向”)移动。
(6)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图乙所示,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触。

①A电极为原电池的___________ 极(填“正”或“负”);
②溶液中的H+移向极(用 A、B 表示)___________ ;
③B电极的电极反应式为___________ ;
④电池的总反应式为___________ 。
(1)已知某反应的平衡表达式为:K=
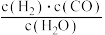 它所对应的化学反应为:
它所对应的化学反应为:(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)
 CH3OH(g) △H =-90.8 kJ/mol
CH3OH(g) △H =-90.8 kJ/mol②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol
CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol ③CO(g)+H2O(g)
 CO2(g)+H2(g) △H =-41.3 kJ/mol
CO2(g)+H2(g) △H =-41.3 kJ/mol 总反应:3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g) 的△H =
CH3OCH3(g)+CO2(g) 的△H =(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如 NO、NO2、N2O4等,对反应N2O4(g)
 2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是
2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是
A A、C 两点的反应速率:A>C
B A、C 两点气体的颜色:A 深,C浅
C A、C 两点的化学平衡常数:A>C
D 由状态 B 到状态 A,可以用加热的方法
(5)NO2可用氨水吸收生成NH4NO3,25℃时,将m mol NH4NO3溶于水,溶液显酸性,向该溶液滴加 n L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将
(6)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图乙所示,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触。

①A电极为原电池的
②溶液中的H+移向极(用 A、B 表示)
③B电极的电极反应式为
④电池的总反应式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】闪锌矿主要成分是 ZnS(含有 SiO2 和少量 FeS、CdS、PbS 杂质),以此为原料制备金属锌的流程如图所示:

相关金属离子[c0(Mn+)=0.1 mol·L -1]形成氢氧化物沉淀的 pH 范围如下:
回答下列问题:
(1)焙烧矿石时先粉碎的目的是_____ 焙烧过程中产生气体主要为_____ 。
(2)滤渣 1 的主要成分除 PbSO4 外还有_____ 。
(3)氧化除杂工序中 ZnO 的作用是_____ ,通入氧气的作用是_____ 。
(4)“溶浸”“氧化除杂”“还原除杂”有一共同操作名称是_____ 。
(5)用锌粉可除去溶液中的 Cd2+,还原除杂工序中反应的离子方程式为_____ 。

相关金属离子[c0(Mn+)=0.1 mol·L -1]形成氢氧化物沉淀的 pH 范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)焙烧矿石时先粉碎的目的是
(2)滤渣 1 的主要成分除 PbSO4 外还有
(3)氧化除杂工序中 ZnO 的作用是
(4)“溶浸”“氧化除杂”“还原除杂”有一共同操作名称是
(5)用锌粉可除去溶液中的 Cd2+,还原除杂工序中反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】甲烷不仅是一种燃料,还是用来生产氢气、乙炔、炭黑等物质的化工原料。回答下列问题:
(1)一种甲烷催化氧化的反应历程如图所示,*表示微粒吸附在催化剂表面。下列叙述错误的是___________(填字母)。

(2)向一恒容密闭容器中加入 和一定量的
和一定量的 ,发生反应:
,发生反应:
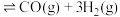 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比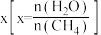 随温度的变化曲线如图所示。
随温度的变化曲线如图所示。

①
___________ (填“>”或“<”,下同) 。
。
②反应速率: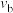 (正)
(正)___________ 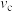 (正),理由是
(正),理由是___________ 。
③点 对应的平衡常数
对应的平衡常数 三者之间的大小关系是
三者之间的大小关系是___________ 。
(3)一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
I. ;
;
II. 。
。
恒定压强为 时,将
时,将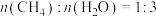 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。

①反应 在
在___________ 条件下能自发进行(填字母)。
A.低温 B.高温 C.任意温度
②图中表示CO的物质的量分数与温度的变化曲线是___________ (填“m”或“n”)。
③系统中q的含量在 左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
左右出现峰值,试从化学平衡的角度解释出现峰值的原因:___________ 。
④上述条件下, 时,
时, 的平衡转化率为
的平衡转化率为___________ (保留2位有效数字),反应Ⅰ的压强平衡常数的计算表达式为
___________  (Kp是以分压表示的平衡常数,分压=总压
(Kp是以分压表示的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
(1)一种甲烷催化氧化的反应历程如图所示,*表示微粒吸附在催化剂表面。下列叙述错误的是___________(填字母)。

| A.*CH3→*CH2的过程中C被氧化,放出热量 |
| B.产物从催化剂表面脱附的速率慢会降低总反应速率 |
| C.适当提高O2分压能加快O2(g)→2*O的反应速率 |
| D.CH4与O2反应生成CO、H2涉及极性键、非极性键的断裂和生成 |
(2)向一恒容密闭容器中加入
 和一定量的
和一定量的 ,发生反应:
,发生反应:
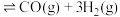 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比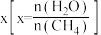 随温度的变化曲线如图所示。
随温度的变化曲线如图所示。
①

 。
。②反应速率:
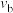 (正)
(正)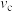 (正),理由是
(正),理由是③点
 对应的平衡常数
对应的平衡常数 三者之间的大小关系是
三者之间的大小关系是(3)一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
I.
 ;
;II.
 。
。恒定压强为
 时,将
时,将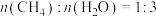 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
①反应
 在
在A.低温 B.高温 C.任意温度
②图中表示CO的物质的量分数与温度的变化曲线是
③系统中q的含量在
 左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
左右出现峰值,试从化学平衡的角度解释出现峰值的原因:④上述条件下,
 时,
时, 的平衡转化率为
的平衡转化率为
 (Kp是以分压表示的平衡常数,分压=总压
(Kp是以分压表示的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】请参考题中图表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根据要求回答问题:
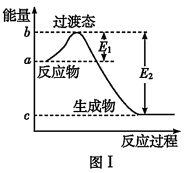
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________ (填“增大”、“减小”或“不变”,下同),ΔH的变化是________ 。请写出NO2和CO反应的热化学方程式:________________________________ 。
(2)如表所示是部分化学键的键能参数:
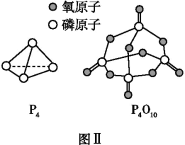
已知白磷的燃烧热为d kJ·mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x=________ kJ·mol-1(用含a、b、c、d的代表数式表示)。
(3)2012年伦敦奥运会火炬采用丙烷(C3H8)为燃料,已知丙烷在常温常压下为气态。试回答下列问题:
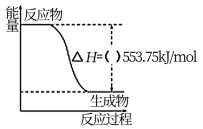
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”____ 。
②请说明使用丙烷作为火炬燃料的优点_____________________________________ 。
③写出表示丙烷燃烧热的热化学方程式:___________________________________ 。
④二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol二甲醚完全燃烧生成CO2和液态水放出1 455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1 645 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为________ 。


(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)如表所示是部分化学键的键能参数:
| 化学键 | P—P | P—O | O=O | P=O |
| 键能/kJ·mol-1 | a | b | c | x |
(3)2012年伦敦奥运会火炬采用丙烷(C3H8)为燃料,已知丙烷在常温常压下为气态。试回答下列问题:

①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”
②请说明使用丙烷作为火炬燃料的优点
③写出表示丙烷燃烧热的热化学方程式:
④二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol二甲醚完全燃烧生成CO2和液态水放出1 455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1 645 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】工业合成氨是人类科学技术的一项重大突破,我国目前氨的生产能力位居世界首位。合成氨反应为

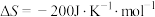 。回答下列问题:
。回答下列问题:
(1)已知 和
和 的燃烧热
的燃烧热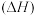 分别为
分别为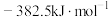 和
和 ,则合成氨反应的
,则合成氨反应的
______ ;合成氨反应的逆过程能自发进行的最低温度为______  。
。
(2)在合成氨过程中,需要不断分离出氨的原因为______ 。(填字母)。
A.有利于平衡正向移动 B.防止催化剂中毒 C.提高正反应速率
(3)某温度下,在容积为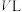 的恒容密闭容器中模拟工业合成氨,充入
的恒容密闭容器中模拟工业合成氨,充入 和
和 的总物质的量为
的总物质的量为 ,容器内起始压强为标准压强
,容器内起始压强为标准压强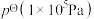 ,容器内各组分的物质的量分数与反应时间
,容器内各组分的物质的量分数与反应时间 的关系如图所示:
的关系如图所示: 表示
表示______ (填物质名称)的物质的量分数的变化情况。
②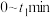 内,平均反应速率
内,平均反应速率
______  。
。
③达平衡时容器内压强为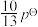 ,则标准平衡常数
,则标准平衡常数
______ [对于反应 ,标准平衡常数
,标准平衡常数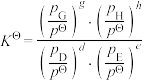 ,其中
,其中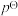 为标准压强,
为标准压强,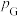 、
、 、
、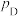 、
、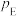 为各组分的平衡分压,分压
为各组分的平衡分压,分压 总压
总压 物质的量分数]。
物质的量分数]。
(4)利用热再生氨电池可实现 电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的
电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的 电镀废液,向甲室中加入足量氨气后电池开始工作。
电镀废液,向甲室中加入足量氨气后电池开始工作。

①乙室中铜极为______ (填“正极”或“负极”)。
②理论上每转移 电子,乙室中溶液的质量变化为
电子,乙室中溶液的质量变化为______  。
。


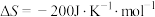 。回答下列问题:
。回答下列问题:(1)已知
 和
和 的燃烧热
的燃烧热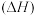 分别为
分别为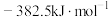 和
和 ,则合成氨反应的
,则合成氨反应的
 。
。(2)在合成氨过程中,需要不断分离出氨的原因为
A.有利于平衡正向移动 B.防止催化剂中毒 C.提高正反应速率
(3)某温度下,在容积为
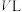 的恒容密闭容器中模拟工业合成氨,充入
的恒容密闭容器中模拟工业合成氨,充入 和
和 的总物质的量为
的总物质的量为 ,容器内起始压强为标准压强
,容器内起始压强为标准压强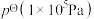 ,容器内各组分的物质的量分数与反应时间
,容器内各组分的物质的量分数与反应时间 的关系如图所示:
的关系如图所示:
 表示
表示②
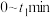 内,平均反应速率
内,平均反应速率
 。
。③达平衡时容器内压强为
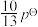 ,则标准平衡常数
,则标准平衡常数
 ,标准平衡常数
,标准平衡常数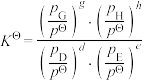 ,其中
,其中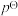 为标准压强,
为标准压强,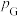 、
、 、
、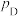 、
、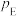 为各组分的平衡分压,分压
为各组分的平衡分压,分压 总压
总压 物质的量分数]。
物质的量分数]。(4)利用热再生氨电池可实现
 电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的
电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的 电镀废液,向甲室中加入足量氨气后电池开始工作。
电镀废液,向甲室中加入足量氨气后电池开始工作。
①乙室中铜极为
②理论上每转移
 电子,乙室中溶液的质量变化为
电子,乙室中溶液的质量变化为 。
。
您最近一年使用:0次
【推荐2】二氧化碳催化加氢是实现双碳达标的重要方式。
已知:I.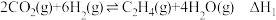
II.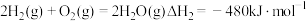
III.
(1)
_______  。
。
(2) 时,向一体积为2L的恒容密闭容器中通入2molCO2(g)和6molH2(g),只发生反应I,测得容器内总压强变化如图。
时,向一体积为2L的恒容密闭容器中通入2molCO2(g)和6molH2(g),只发生反应I,测得容器内总压强变化如图。
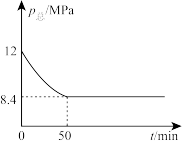
①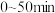 内,
内, 的平均速率为
的平均速率为_______ 。
②达到平衡时, 的转化率为
的转化率为_______ 。
③下列措施能提高 平衡转化率的是
平衡转化率的是_______ (填标号)。
A.使用合适的催化剂 B.充入氢气 C.升高温度 D.分离产物
(3)已知反应I的正反应速率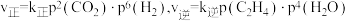 (
(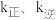 为正、逆反应速率常数,只与温度、催化剂有关,与浓度无关)。
为正、逆反应速率常数,只与温度、催化剂有关,与浓度无关)。
①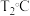 时,
时,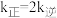 ,则该温度下压强平衡常数
,则该温度下压强平衡常数
_______ 。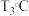 ,平衡时
,平衡时 ,则
,则
_______ (填“>”、“<”或“=”) 。
。
②下列说法正确的是_______ (填标号)。
A.升高温度,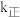 增大的倍数大于
增大的倍数大于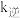 增大的倍数
增大的倍数
B.加入高效催化剂,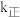 增大的倍数等于
增大的倍数等于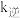 增大的倍数
增大的倍数
C.增大压强,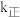 增大的倍数大于
增大的倍数大于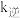 增大的倍数
增大的倍数
D.增大 浓度,
浓度,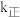 增大的倍数大于
增大的倍数大于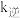 增大的倍数
增大的倍数
(4)工业上采用电催化法实现 还原制乙烯,除乙烯外还有副产物,装置如图所示。
还原制乙烯,除乙烯外还有副产物,装置如图所示。
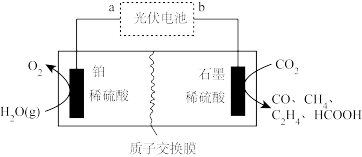
石墨电极上生成乙烯的电极反应式为_______ ;当生成了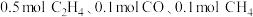 和
和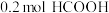 时,理论上有
时,理论上有_______ 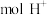 通过质子交换膜。
通过质子交换膜。
已知:I.
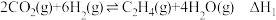
II.
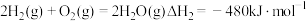
III.

(1)

 。
。(2)
 时,向一体积为2L的恒容密闭容器中通入2molCO2(g)和6molH2(g),只发生反应I,测得容器内总压强变化如图。
时,向一体积为2L的恒容密闭容器中通入2molCO2(g)和6molH2(g),只发生反应I,测得容器内总压强变化如图。
①
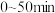 内,
内, 的平均速率为
的平均速率为②达到平衡时,
 的转化率为
的转化率为③下列措施能提高
 平衡转化率的是
平衡转化率的是A.使用合适的催化剂 B.充入氢气 C.升高温度 D.分离产物
(3)已知反应I的正反应速率
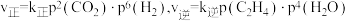 (
(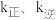 为正、逆反应速率常数,只与温度、催化剂有关,与浓度无关)。
为正、逆反应速率常数,只与温度、催化剂有关,与浓度无关)。①
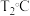 时,
时,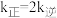 ,则该温度下压强平衡常数
,则该温度下压强平衡常数
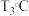 ,平衡时
,平衡时 ,则
,则
 。
。②下列说法正确的是
A.升高温度,
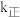 增大的倍数大于
增大的倍数大于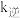 增大的倍数
增大的倍数B.加入高效催化剂,
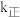 增大的倍数等于
增大的倍数等于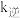 增大的倍数
增大的倍数C.增大压强,
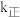 增大的倍数大于
增大的倍数大于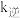 增大的倍数
增大的倍数D.增大
 浓度,
浓度,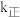 增大的倍数大于
增大的倍数大于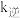 增大的倍数
增大的倍数(4)工业上采用电催化法实现
 还原制乙烯,除乙烯外还有副产物,装置如图所示。
还原制乙烯,除乙烯外还有副产物,装置如图所示。
石墨电极上生成乙烯的电极反应式为
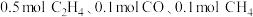 和
和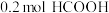 时,理论上有
时,理论上有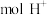 通过质子交换膜。
通过质子交换膜。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】苯硫酚( )是一种医药中间体,可做麻醉剂,其工业制备原理如下。
)是一种医药中间体,可做麻醉剂,其工业制备原理如下。
主反应I: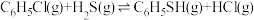
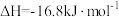
副反应Ⅱ: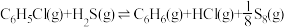

已知:① 的选择性
的选择性
②改变温度对热效应(吸收或释放)大的反应影响大
请回答下列问题:
(1)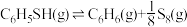 的活化能
的活化能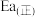
___________ 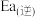 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
恒温恒容条件下,该分解反应达平衡时,减小反应物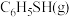 浓度,再次达平衡时,
浓度,再次达平衡时, 的转化率
的转化率___________ (填“增大”、“减小”或“不变”)。
(2)工业制备苯硫酚的反应常在高压容器内进行,该措施的优点有___________ (写出两点)
(3) 时向恒容密闭容器中充入等物质的量的
时向恒容密闭容器中充入等物质的量的 和
和 ,只发生上述主、副反应。反应达到平衡时
,只发生上述主、副反应。反应达到平衡时 的体积分数为m,
的体积分数为m, 的体积分数为n。
的体积分数为n。
①下列有关上述过程说法正确的是___________ 。
A.已知主反应 ,则该反应在高温下自发进行
,则该反应在高温下自发进行
B.平衡时 的选择性为
的选择性为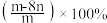
C.平衡时正反应速率: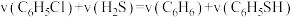
D.升高体系的温度,达新平衡后 比值变大
比值变大
② 时,主反应的压强平衡常数
时,主反应的压强平衡常数
___________ (用含m、n的代数式表示)
③上述条件下,实验测得 和
和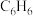 的产率在相同时间内随温度的变化如图所示。在温度高于
的产率在相同时间内随温度的变化如图所示。在温度高于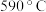 时两种产物的产率呈现图中变化趋势的原因是
时两种产物的产率呈现图中变化趋势的原因是___________ ;
由此可知主反应I和副反应Ⅱ的活化能大小为: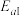
___________  (填写“>”、“<”或=)。
(填写“>”、“<”或=)。
 )是一种医药中间体,可做麻醉剂,其工业制备原理如下。
)是一种医药中间体,可做麻醉剂,其工业制备原理如下。主反应I:
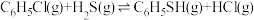
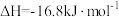
副反应Ⅱ:
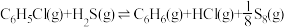

已知:①
 的选择性
的选择性
②改变温度对热效应(吸收或释放)大的反应影响大
请回答下列问题:
(1)
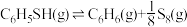 的活化能
的活化能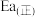
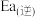 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。恒温恒容条件下,该分解反应达平衡时,减小反应物
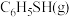 浓度,再次达平衡时,
浓度,再次达平衡时, 的转化率
的转化率(2)工业制备苯硫酚的反应常在高压容器内进行,该措施的优点有
(3)
 时向恒容密闭容器中充入等物质的量的
时向恒容密闭容器中充入等物质的量的 和
和 ,只发生上述主、副反应。反应达到平衡时
,只发生上述主、副反应。反应达到平衡时 的体积分数为m,
的体积分数为m, 的体积分数为n。
的体积分数为n。①下列有关上述过程说法正确的是
A.已知主反应
 ,则该反应在高温下自发进行
,则该反应在高温下自发进行B.平衡时
 的选择性为
的选择性为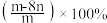
C.平衡时正反应速率:
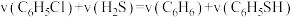
D.升高体系的温度,达新平衡后
 比值变大
比值变大②
 时,主反应的压强平衡常数
时,主反应的压强平衡常数
③上述条件下,实验测得
 和
和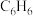 的产率在相同时间内随温度的变化如图所示。在温度高于
的产率在相同时间内随温度的变化如图所示。在温度高于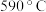 时两种产物的产率呈现图中变化趋势的原因是
时两种产物的产率呈现图中变化趋势的原因是由此可知主反应I和副反应Ⅱ的活化能大小为:
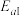
 (填写“>”、“<”或=)。
(填写“>”、“<”或=)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】 、
、 、CO、NO、
、CO、NO、 等物质不能直接排放到大气中,需要经过处理进行回收利用,从而达到减排的自的。请回答下列问题:
等物质不能直接排放到大气中,需要经过处理进行回收利用,从而达到减排的自的。请回答下列问题:
(1) 的分子空间构型是
的分子空间构型是_______ 。
(2)已知S(s)和CO(g)的燃烧热分别是296.0 kJ/mol、283.0 kJ/mol,则反应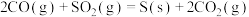 的
的
_______ 。
(3)向体积为20 L的恒容密闭容器中充入一定量的HCl和 ,发生反应:
,发生反应: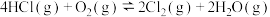
 。反应物的转化率与温度(T)的关系如图所示[已知起始时
。反应物的转化率与温度(T)的关系如图所示[已知起始时 ,a'和b'为平衡转化率]。
,a'和b'为平衡转化率]。
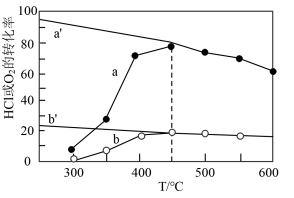
①该反应的
_______ (填“>”或“<”)0。
②下列关于该反应的说法正确的是_______ (填字母)。
A.曲线a表示HCl的转化率
B.温度越高化学平衡常数越大
C.容器中压强不再改变时反应达到最大限度
D.该反应只有高温下才能自发进行
③温度低于450℃时,温度升高,HCl和 的转化率增大的原因为
的转化率增大的原因为_______ 。
④若初始时向容器中充入的HCl和 均为1 mol,5 min时反应达到平衡,该温度下
均为1 mol,5 min时反应达到平衡,该温度下 的转化率为20%,则0~5 min内HCl的平均反应速率为
的转化率为20%,则0~5 min内HCl的平均反应速率为_______ ,该反应的平衡常数
_______ [已知:气体分压( )=气体总压(
)=气体总压( )×体积分数,
)×体积分数, 为以分压表示的平衡常数;平衡时容器内的总压为
为以分压表示的平衡常数;平衡时容器内的总压为 ]。
]。
 、
、 、CO、NO、
、CO、NO、 等物质不能直接排放到大气中,需要经过处理进行回收利用,从而达到减排的自的。请回答下列问题:
等物质不能直接排放到大气中,需要经过处理进行回收利用,从而达到减排的自的。请回答下列问题:(1)
 的分子空间构型是
的分子空间构型是(2)已知S(s)和CO(g)的燃烧热分别是296.0 kJ/mol、283.0 kJ/mol,则反应
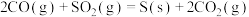 的
的
(3)向体积为20 L的恒容密闭容器中充入一定量的HCl和
 ,发生反应:
,发生反应: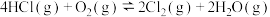
 。反应物的转化率与温度(T)的关系如图所示[已知起始时
。反应物的转化率与温度(T)的关系如图所示[已知起始时 ,a'和b'为平衡转化率]。
,a'和b'为平衡转化率]。
①该反应的

②下列关于该反应的说法正确的是
A.曲线a表示HCl的转化率
B.温度越高化学平衡常数越大
C.容器中压强不再改变时反应达到最大限度
D.该反应只有高温下才能自发进行
③温度低于450℃时,温度升高,HCl和
 的转化率增大的原因为
的转化率增大的原因为④若初始时向容器中充入的HCl和
 均为1 mol,5 min时反应达到平衡,该温度下
均为1 mol,5 min时反应达到平衡,该温度下 的转化率为20%,则0~5 min内HCl的平均反应速率为
的转化率为20%,则0~5 min内HCl的平均反应速率为
 )=气体总压(
)=气体总压( )×体积分数,
)×体积分数, 为以分压表示的平衡常数;平衡时容器内的总压为
为以分压表示的平衡常数;平衡时容器内的总压为 ]。
]。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】 和
和 在特殊条件下会出现某些特殊的性质。
在特殊条件下会出现某些特殊的性质。
(1)采用碱液吸收 并进行电化学氧化可得到硫单质。当
并进行电化学氧化可得到硫单质。当 浓度较低时常用纯碱溶液进行吸收。下表为
浓度较低时常用纯碱溶液进行吸收。下表为 、
、 的电离平衡常数。
的电离平衡常数。
纯碱溶液吸收少量 的离子方程式为
的离子方程式为___________ 。
(2)温度、压强分别超过临界温度(374.2℃)、临界压强(221MPa)的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此形成了超临界水氧化技术。一定实验条件下,运用超临界水氧化技术氧化乙醇的结果如图-1、图-2所示,其中x为以碳元素计的物质的量分数,t为反应时间。
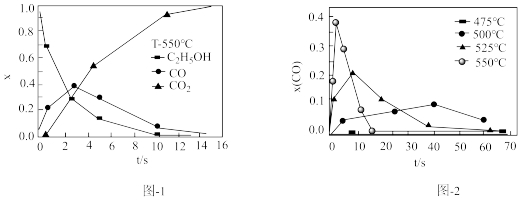
①由图-1,乙醇氧化过程中存在中间产物,该中间产物的化学式为_______ 。
②由图-2,随温度升高,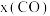 峰值出现的时间提前,且峰值更高,其可能的原因是
峰值出现的时间提前,且峰值更高,其可能的原因是_______ 。
(3)过氧化氢的电离方程式为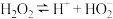 。研究表明,过氧化氢溶液中
。研究表明,过氧化氢溶液中 的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与
的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与 的关系如图-3所示。
的关系如图-3所示。
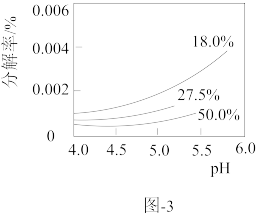
一定浓度的过氧化氢,随 增大分解率增大的原因是
增大分解率增大的原因是___________ 。
(4)研究表明, 对不同原子的结合能力具有差异性,
对不同原子的结合能力具有差异性, 在
在 表面电还原生成
表面电还原生成 的机理如下图:
的机理如下图:

用简洁的语言描述图-4中涉及的转化过程___________ 。
 和
和 在特殊条件下会出现某些特殊的性质。
在特殊条件下会出现某些特殊的性质。(1)采用碱液吸收
 并进行电化学氧化可得到硫单质。当
并进行电化学氧化可得到硫单质。当 浓度较低时常用纯碱溶液进行吸收。下表为
浓度较低时常用纯碱溶液进行吸收。下表为 、
、 的电离平衡常数。
的电离平衡常数。| 电离平衡常数 |  |  |
 |  | 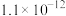 |
 | 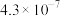 | 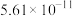 |
纯碱溶液吸收少量
 的离子方程式为
的离子方程式为(2)温度、压强分别超过临界温度(374.2℃)、临界压强(221MPa)的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此形成了超临界水氧化技术。一定实验条件下,运用超临界水氧化技术氧化乙醇的结果如图-1、图-2所示,其中x为以碳元素计的物质的量分数,t为反应时间。

①由图-1,乙醇氧化过程中存在中间产物,该中间产物的化学式为
②由图-2,随温度升高,
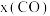 峰值出现的时间提前,且峰值更高,其可能的原因是
峰值出现的时间提前,且峰值更高,其可能的原因是(3)过氧化氢的电离方程式为
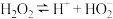 。研究表明,过氧化氢溶液中
。研究表明,过氧化氢溶液中 的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与
的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与 的关系如图-3所示。
的关系如图-3所示。
一定浓度的过氧化氢,随
 增大分解率增大的原因是
增大分解率增大的原因是(4)研究表明,
 对不同原子的结合能力具有差异性,
对不同原子的结合能力具有差异性, 在
在 表面电还原生成
表面电还原生成 的机理如下图:
的机理如下图:
用简洁的语言描述图-4中涉及的转化过程
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】燃煤烟气的脱硫脱硝是目前研究的热点。回答下列问题:
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物污染,涉及反应如下:
I.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ∆H=-574kJ/mol
II.CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ∆H=-1160kJ/mol
III.H2O(g)=H2O(l) ∆H=-44kJ/mol
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ∆H=_________ kJ/mol
(2)某科研小组研究臭氧氧化-碱吸收法同时脱除 SO2 和 NO工艺,氧化过程反应原理及反应热、活化能数据如表:
其他条件不变,每次向容积为2L的反应器中充入含1.0molNO、1.0molSO2 的混合气和 2.0molO3,改变温度,反应相同时间t 后,体系中NO 和 SO2 的转化率如图所示。
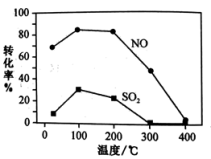
①由图可知相同温度下 NO 的转化率远高于 SO2,结合题中数据分析其可能原因:_______
②温度高于200℃后,NO和SO2的转化率随温度升高显著下降的可能原因是_______
③若其他条件不变,缩小反应器的容积,NO 和 SO2的平衡转化率_______ (填“增大”“减小”或“不变”)
(3)在一定条件下,焦炭催化还原SO2的化学方程式为:2C(s)+2SO2(g)⇌S2(g)+2CO2(g)
①该反应的逆反应速率表达式:v逆=k逆·c(S2)·c2(CO2),k逆为速率常数(仅与温度有关)。表为某温度下,测得的实验数据:
由表中数据可知,该温度下,上述反应的逆反应速率常数 k逆=_______ L2·mol-2·min-1
②一定压强下,向1L 密闭容器中加入足量的焦炭和 1molSO2 发生上述反应,反应 10min 时,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:
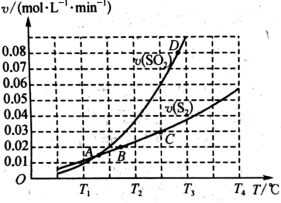
根据图象,判断反应2C(s)+2SO2(g)⇌S2(g)+2CO2(g)的∆H_______ (填“>”“<”“=”)0 A、B、C、D 四点对应的状态中,达到平衡状态的有_______ (填字母),该点对应的温度下的化学平衡常数K=_______
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物污染,涉及反应如下:
I.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ∆H=-574kJ/mol
II.CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ∆H=-1160kJ/mol
III.H2O(g)=H2O(l) ∆H=-44kJ/mol
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ∆H=
(2)某科研小组研究臭氧氧化-碱吸收法同时脱除 SO2 和 NO工艺,氧化过程反应原理及反应热、活化能数据如表:
| 反应 | 反应热(∆H1)/kJ mol-1 mol-1 | 活化能(Ea1)//kJ mol-1 mol-1 |
| NO(g)+O3(g)⇌NO2(g)+O2(g) | -200.9 | 3.2 |
SO2(g)+O3(g) SO3(g)+O2(g) SO3(g)+O2(g) | -241.6 | 58 |
| 臭氧分解:2O3(g)⇌3O2(g) |

①由图可知相同温度下 NO 的转化率远高于 SO2,结合题中数据分析其可能原因:
②温度高于200℃后,NO和SO2的转化率随温度升高显著下降的可能原因是
③若其他条件不变,缩小反应器的容积,NO 和 SO2的平衡转化率
(3)在一定条件下,焦炭催化还原SO2的化学方程式为:2C(s)+2SO2(g)⇌S2(g)+2CO2(g)
①该反应的逆反应速率表达式:v逆=k逆·c(S2)·c2(CO2),k逆为速率常数(仅与温度有关)。表为某温度下,测得的实验数据:
| S2的浓度/(mol/L) | CO2的浓度/(mol/L) | 逆反应速率/(mol L-1 L-1 min-1) min-1) |
| 0.1 | c1 | 9.6 |
| c2 | c1 | 19.2 |
| c2 | 0.3 | 64.8 |
②一定压强下,向1L 密闭容器中加入足量的焦炭和 1molSO2 发生上述反应,反应 10min 时,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:

根据图象,判断反应2C(s)+2SO2(g)⇌S2(g)+2CO2(g)的∆H
您最近一年使用:0次



