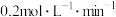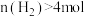N2O5是一种新型硝化剂,在一定温度下可以发生以下反应:2N2O5(g) 4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
下列说法中不正确的是
 4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:| 时间/s | 0 | 500 | 1 000 | 1 500 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A.500 s内,N2O5的分解速率为2.96×10-3 mol·L-1·s-1 |
| B.T1温度下的平衡常数K1=125,平衡时N2O5的转化率为50% |
| C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 |
D.T1时,4NO2(g)+O2(g) 2N2O5(g)的平衡常数为 2N2O5(g)的平衡常数为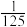 |
更新时间:2021-04-08 18:26:48
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】某化学反应2X(g) ⇌Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol·L -1)随反应时间(min)的变化情况如下表:
-1)随反应时间(min)的变化情况如下表:
化情况如下表:
下列说法不正确的是
 -1)随反应时间(min)的变化情况如下表:
-1)随反应时间(min)的变化情况如下表:化情况如下表:
| 实验序号 | 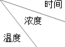 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A.c>1.0 |
| B.实验2可能使用了催化剂 |
| C.实验3比实验2先达到化学平衡状态 |
D.前10分钟,实验4的平均化学反应速率比实验 1的大 1的大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v1=k1c2(M),反应②的速率可表示为v2=k2c2(M) (k1、k2为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是


| A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1 |
| B.反应开始后,体系中Y和Z的浓度之比保持不变 |
| C.如果反应能进行到底,反应结束时62.5%的M转化为Z |
| D.反应①的活化能比反应②的活化能大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列实验过程可以达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A. | 比较碳酸和醋酸的酸性 | 常温下,用pH计测量等浓度醋酸钠和碳酸氢钠溶液的pH |
| B. | 探究浓度对反应速率的影响 | 向盛有4mL浓度分别为0.01mol/L和0.05mol/LKMnO4酸性溶液的两支试管中,同时加入4mL0.1mol/L的草酸溶液,记录褪色所需时间 |
| C. | 证明Ksp[Fe(OH)3]<Ksp[Al (OH)3] | 向1mL0.1 mol·L-1NaOH溶液中滴加2滴0.1 mol·L-1 AlCl3溶液,充分反应后再滴加2滴0.1 mol·L-1 FeCl3溶液,观察沉淀颜色变化 |
| D. | 探究温度对反应速率的影响 | 将2支盛有5 mL同浓度NaHSO3溶液的试管和两支盛有2 mL 5%H2O2溶液的试管分成两组,一组放入冷水中,另一组放入热水中,经过一段时间分别混合并搅拌,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】东南大学某课题组合成了一种新型具有平面分子结构的醌类聚合物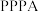 ,
,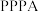 可作为有机锌离子电池的正极材料。下列叙述正确的是
可作为有机锌离子电池的正极材料。下列叙述正确的是

已知: 作该反应的催化剂,
作该反应的催化剂, 升华温度为178℃,
升华温度为178℃, 的熔点为801℃。
的熔点为801℃。
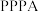 ,
,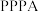 可作为有机锌离子电池的正极材料。下列叙述正确的是
可作为有机锌离子电池的正极材料。下列叙述正确的是
已知:
 作该反应的催化剂,
作该反应的催化剂, 升华温度为178℃,
升华温度为178℃, 的熔点为801℃。
的熔点为801℃。A.吩嗪和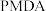 是 是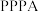 的链节 的链节 |
| B.为了提高反应速率,可将反应温度由150℃升至160℃ |
C.上述反应中,断裂了 键和 键和 键,也形成了 键,也形成了 键和 键和 键 键 |
D. 吩嗪和 吩嗪和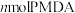 完全合成 完全合成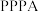 时,生成 时,生成 水 水 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】某同学模拟工业废水变废为宝,设计了用沉淀法回收各金属阳离子的实验方案:

已知:
①溶液中某离子浓度小于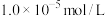 ,可认为该离子不存在;
,可认为该离子不存在;
②实验过程中,假设溶液体积、温度不变;
③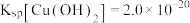 ;
;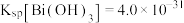 ;
;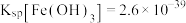 ;
; 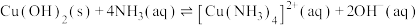

下列说法不正确的是

| 模拟工业废水的离子浓度(mol/l) |  |  |  |  |  |
| 0.10 | 0.010 | 0.0040 | 0.0010 | 0.141 |
①溶液中某离子浓度小于
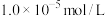 ,可认为该离子不存在;
,可认为该离子不存在;②实验过程中,假设溶液体积、温度不变;
③
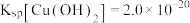 ;
;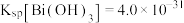 ;
;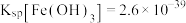 ;
; 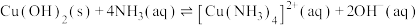

下列说法不正确的是
A.步骤I中加入的 |
B.步骤II得到的滤液N中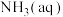 的浓度 的浓度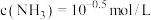 |
C.步骤III得到的沉淀Z为 |
D.反应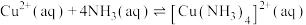 的平衡常数 的平衡常数 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:X2 (g)+3Y2(g) 2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
下列叙述不正确的是( )
 2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3 kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
下列叙述不正确的是( )
| A.容器①中达到平衡时,Y2的转化率为50% |
| B.Q="27.78" kJ |
| C.相同温度下;起始时向容器中充入1.0 X2mol 、3.0 mol Y2和2 mol XY3;反应达到平衡前v(正)>v(逆) |
D.容器①、②中反应的平衡常数相等,K= |
您最近半年使用:0次

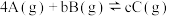
 。反应过程中的部分数据如下表所示:
。反应过程中的部分数据如下表所示: min时,该反应可能已达到平衡
min时,该反应可能已达到平衡
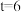 min时,反应放出的热量为0.6Q kJ
min时,反应放出的热量为0.6Q kJ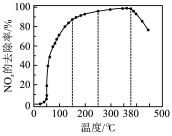

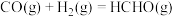

 的密闭装置中充入
的密闭装置中充入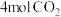 和
和 ,在t℃下反应,
,在t℃下反应, 后达平衡状态.测得容器内
后达平衡状态.测得容器内 ,
,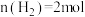 ,
,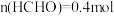 ,下列说法错误的是
,下列说法错误的是 表示的反应Ⅰ的平均反应速率为
表示的反应Ⅰ的平均反应速率为