铑的配合物Rh(PPh3)Cl可催化丙烯与氢气的加成,反应过程为:CH3CH=CH2+H2 CH3CH2CH3,回答下列问题:
CH3CH2CH3,回答下列问题:
(1)基态Rh原子的价电子排布式为4d85s1,铑在周期表的位置是_______ ,其原子中的未成对电子数为_______ 。
(2) 1mol丙烯(CH3CH=CH2)中σ键的数目为_______ ,其结构简式中打点的C原子与H原子间的σ键可称为sp2-sσ键,则丙烯分子中C原子之间的所有σ键可称为_______ 。
(3)第一电离能P_______ Cl (填“大于”或“小于”),PPh3是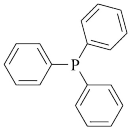 的缩写,该分子的立体构型是
的缩写,该分子的立体构型是_______ 。比较PPh3与PH3的沸点大小,并说明原因_______ 。
(4) RhCl3的晶胞结构中Rh3+的位置如图所示(Cl-未画出):
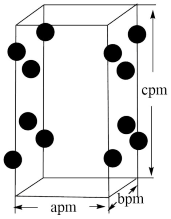
①晶胞中含有的Cl-数目为_______ ;
②若阿伏加德罗常数为NA,则晶体的密度为_______ g·cm-3.(列出计算式)
 CH3CH2CH3,回答下列问题:
CH3CH2CH3,回答下列问题:(1)基态Rh原子的价电子排布式为4d85s1,铑在周期表的位置是
(2) 1mol丙烯(CH3CH=CH2)中σ键的数目为
(3)第一电离能P
 的缩写,该分子的立体构型是
的缩写,该分子的立体构型是(4) RhCl3的晶胞结构中Rh3+的位置如图所示(Cl-未画出):

①晶胞中含有的Cl-数目为
②若阿伏加德罗常数为NA,则晶体的密度为
更新时间:2021-05-31 12:06:40
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】1100℃时,在体积为5L的密闭容器中,发生可逆反应:Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g)并达到平衡,请完成下列各题:
Na2S(s)+4H2O(g)并达到平衡,请完成下列各题:
(1)上述反应中涉及的非金属元素原子的半径从大到小的顺序为_____________ ,非金属性最强的元素原子的电子排布式_________________ ,其电子的自旋方向共有________ 种。
(2)该反应中O、S属于同主族元素,比较它们的单质的氧化性_____________________ (用化学方程式表示),写出Na2O的电子式______ ,比较Na2O和Na2S的熔点高低:Na2O___ Na2S。
(3)上述平衡的平衡常数表达式K=______________________ 。降低温度,K值减小,则正反应为_______ (填“吸热”或“放热”)反应。
(4)能判断反应达到平衡状态的依据是_____________ (填序号)。
A.混合气体的压强不变 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.各气体的浓度相等
(5)若初始时加入的Na2SO4为2.84g,10分钟后达到平衡时Na2SO4的转化率为45%,V(H2)=__________________ 。平衡后,向容器中充入1molH2,平衡向_________________ (填“正反应方向”、“逆反应方向”或“不移动”),重新达到平衡后,与原平衡相比,H2的体积百分含量_____________ (填“增大”、“减小”或“不变”)
 Na2S(s)+4H2O(g)并达到平衡,请完成下列各题:
Na2S(s)+4H2O(g)并达到平衡,请完成下列各题:(1)上述反应中涉及的非金属元素原子的半径从大到小的顺序为
(2)该反应中O、S属于同主族元素,比较它们的单质的氧化性
(3)上述平衡的平衡常数表达式K=
(4)能判断反应达到平衡状态的依据是
A.混合气体的压强不变 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.各气体的浓度相等
(5)若初始时加入的Na2SO4为2.84g,10分钟后达到平衡时Na2SO4的转化率为45%,V(H2)=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】随着科学技术的发展,过渡金属在高科技材料合成中得以广泛应用,以 、ZnO等半导体材料制作的传感器和芯片具有能耗低的特点,而以磷酸亚铁锂
、ZnO等半导体材料制作的传感器和芯片具有能耗低的特点,而以磷酸亚铁锂 为电极材料的锂离子电池具有充电快,比能量高等特点。请回答下列问题:
为电极材料的锂离子电池具有充电快,比能量高等特点。请回答下列问题:
(1)Cu元素位于周期表的_______ 区,基态Cu原子核外电子占据的最高能层符号是_______ 。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______ 。
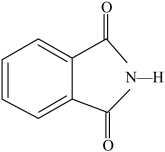
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。合成酞菁的原料之一邻苯二甲酰亚胺的结构如图,则N原子的孤电子对占据N原子的_______轨道。
(4)金属Zn能溶于氨水,生成配合物 ,提供孤电子对的原子是
,提供孤电子对的原子是_______ ,写出该配合物中配离子的结构式_______ (请标出配位键)。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是_______ 。
(6)磷酸亚铁锂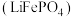 的一种制备方法如图。
的一种制备方法如图。
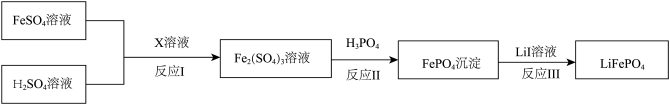
回答问题:
① 中,铁元素的化合价为
中,铁元素的化合价为_______ 。
②反应I中X试剂最好是_______ 。
③从反应II所得混合物中分离出 需要的玻璃仪器有玻璃棒、
需要的玻璃仪器有玻璃棒、_______ 、_______ 。
④反应III的离子方程式是_______ 。
 、ZnO等半导体材料制作的传感器和芯片具有能耗低的特点,而以磷酸亚铁锂
、ZnO等半导体材料制作的传感器和芯片具有能耗低的特点,而以磷酸亚铁锂 为电极材料的锂离子电池具有充电快,比能量高等特点。请回答下列问题:
为电极材料的锂离子电池具有充电快,比能量高等特点。请回答下列问题:(1)Cu元素位于周期表的
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。合成酞菁的原料之一邻苯二甲酰亚胺的结构如图,则N原子的孤电子对占据N原子的_______轨道。

| A.2s轨道 | B.2p轨道 | C. 杂化轨道 杂化轨道 | D. 杂化轨道 杂化轨道 |
 ,提供孤电子对的原子是
,提供孤电子对的原子是(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是
(6)磷酸亚铁锂
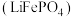 的一种制备方法如图。
的一种制备方法如图。
回答问题:
①
 中,铁元素的化合价为
中,铁元素的化合价为②反应I中X试剂最好是
③从反应II所得混合物中分离出
 需要的玻璃仪器有玻璃棒、
需要的玻璃仪器有玻璃棒、④反应III的离子方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】元素A、B、C、D、E、F、G的原子序数依次增大,A、F原子的最外层电子数等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同的能级,且每个能级上排布的电子数相等;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F;G原子最外层有一个单电子,且内层原子轨道均排满。
(1)与C单质分子互为等电子体的分子为_____ ,该分子的电子式为______________ 。
(2)B、C、D三种元素第一电离能从大到小的顺序:________ (填元素符号)
(3)光谱证实:单质F与强碱性溶液反应有[F(OH)4]-生成,则[F(OH)4]-中存在_________ 。
a、共价键 b、非极性键 c、配位键 d、σ键 e、π键
(4)B、C、D三种元素与A形成的最简单化合物的稳定性由强到弱的顺序:____ (填化学式)
(5)G位于元素周期表的____ 区,向含有G2+离子的溶液中通入A、C形成的最简单分子至过量所涉及的两个离子方程式_________________________________________________ 。
(1)与C单质分子互为等电子体的分子为
(2)B、C、D三种元素第一电离能从大到小的顺序:
(3)光谱证实:单质F与强碱性溶液反应有[F(OH)4]-生成,则[F(OH)4]-中存在
a、共价键 b、非极性键 c、配位键 d、σ键 e、π键
(4)B、C、D三种元素与A形成的最简单化合物的稳定性由强到弱的顺序:
(5)G位于元素周期表的
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铁和硒( :第四周期ⅥA)都是人体必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
:第四周期ⅥA)都是人体必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉是一种抗癌新药,其结构式如下:
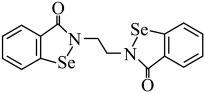
①基态Se原子的核外电子排布式为___________ 。
②比较键角大小:气态 分子
分子___________  离子(填“>”“<”或“=”),原因是:
离子(填“>”“<”或“=”),原因是:___________ 。
(2)富马酸亚铁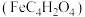 是一种补铁剂。富马酸分子的结构式如图所示:
是一种补铁剂。富马酸分子的结构式如图所示:
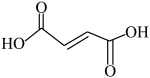
①富马酸分子中 键与
键与 键的数目比为
键的数目比为___________ 。
②富马酸亚铁中各元素的电负性由大到小的顺序为___________ 。
③请写出亚铁离子的价层电子轨道表示式___________ 。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化 ,将
,将 转化为
转化为 ,反应过程如图所示:
,反应过程如图所示:
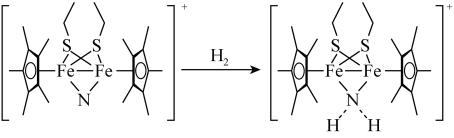
产物 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为___________ 。
 :第四周期ⅥA)都是人体必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
:第四周期ⅥA)都是人体必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:(1)乙烷硒啉是一种抗癌新药,其结构式如下:

①基态Se原子的核外电子排布式为
②比较键角大小:气态
 分子
分子 离子(填“>”“<”或“=”),原因是:
离子(填“>”“<”或“=”),原因是:(2)富马酸亚铁
 是一种补铁剂。富马酸分子的结构式如图所示:
是一种补铁剂。富马酸分子的结构式如图所示:
①富马酸分子中
 键与
键与 键的数目比为
键的数目比为②富马酸亚铁中各元素的电负性由大到小的顺序为
③请写出亚铁离子的价层电子轨道表示式
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化
 ,将
,将 转化为
转化为 ,反应过程如图所示:
,反应过程如图所示:
产物
 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】锌及其化合物在科学技术发展和人类生产生活中发挥着重要作用。
(1)明朝《天工开物》中就已经记载了我国古代的炼锌技术:以炉甘石(ZnCO3)和木炭为原料高温制取锌。请写出Zn2+的价电子排布轨道式_______ ,ZnCO3中C原子的杂化形式为_______ ,Zn、C、O的电负性由小到大的顺序是_______ 。
(2)“此物(“锌火”)无铜收伏,入火即成烟飞去”,意思是锌的沸点(907℃)较低,宜与铜熔合制成黄铜。已知Zn与Cu的能量变化如下所示:
Cu(g)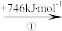 Cu+(g)
Cu+(g) Cu2+(g)
Cu2+(g)
Zn(g)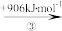 Zn+(g)
Zn+(g)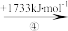 Zn2+(g)
Zn2+(g)
①试解释步骤②吸收能量大于步骤④的原因_______ 。
②金属锌采取如图1所示堆积方式:
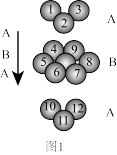
该堆积方式类型与金属铜的堆积方式_______ (填“相同”或“不相同”)。
(3)我国科学家最新研制成功了一种纳米半导体材料可以高效实现光化学转换,该种材料主要成分为硫化镉和硫化锌。Cd与Zn位于同一副族,且在Zn的下一周期。已知ZnS熔点为2830℃;CdS熔点为1750℃,ZnS熔点更高的原因为_______ 。
(4)独立的NH3分子中,H—N—H键键角为107°18',请解释[Zn(NH3)6]2+离子中H—N—H键角变为109.5°的原因是_______ 。根据VSEPR模型判断,下列微粒中所有原子都在同一平面上的一组是_______ 。
A. 和
和 B.
B. 和SO3 C.H3O+和
和SO3 C.H3O+和 D.
D. 和
和
(5)图2为ZnS晶胞,图3为晶胞沿z轴的1∶1投影平面图:
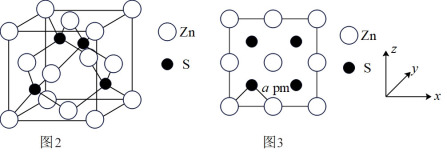
①晶胞中最近的两个S原子之间的距离为_______ pm(含字母a写计算表达式)。
②已知S2-半径为bpm,若晶胞中S2-、Zn2+相切,则Zn2+半径为_______ pm(写计算表达式)。(含字母a、b写计算表达式)。
(1)明朝《天工开物》中就已经记载了我国古代的炼锌技术:以炉甘石(ZnCO3)和木炭为原料高温制取锌。请写出Zn2+的价电子排布轨道式
(2)“此物(“锌火”)无铜收伏,入火即成烟飞去”,意思是锌的沸点(907℃)较低,宜与铜熔合制成黄铜。已知Zn与Cu的能量变化如下所示:
Cu(g)
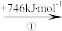 Cu+(g)
Cu+(g) Cu2+(g)
Cu2+(g)Zn(g)
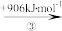 Zn+(g)
Zn+(g)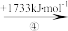 Zn2+(g)
Zn2+(g)①试解释步骤②吸收能量大于步骤④的原因
②金属锌采取如图1所示堆积方式:

该堆积方式类型与金属铜的堆积方式
(3)我国科学家最新研制成功了一种纳米半导体材料可以高效实现光化学转换,该种材料主要成分为硫化镉和硫化锌。Cd与Zn位于同一副族,且在Zn的下一周期。已知ZnS熔点为2830℃;CdS熔点为1750℃,ZnS熔点更高的原因为
(4)独立的NH3分子中,H—N—H键键角为107°18',请解释[Zn(NH3)6]2+离子中H—N—H键角变为109.5°的原因是
A.
 和
和 B.
B. 和SO3 C.H3O+和
和SO3 C.H3O+和 D.
D. 和
和
(5)图2为ZnS晶胞,图3为晶胞沿z轴的1∶1投影平面图:

①晶胞中最近的两个S原子之间的距离为
②已知S2-半径为bpm,若晶胞中S2-、Zn2+相切,则Zn2+半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】过渡金属元素铬(Cr)是不锈钢的重要成分。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是___________ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s轨道上电子能量比3d高,且总是在比3d轨道上电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是___________ ,中心离子的配位数为___________ 。
(3) 中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
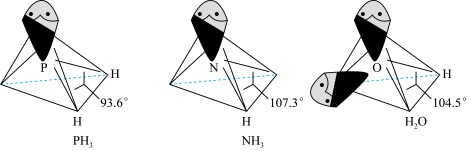
PH3中P的杂化类型是___________ 。NH3的沸点比PH3的___________ (填高,低或无法确定)
(1)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为

B.4s轨道上电子能量比3d高,且总是在比3d轨道上电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(3)
 中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
PH3中P的杂化类型是
您最近一年使用:0次
【推荐1】 、
、 是新型磁性材料的成分。依其中有关元素回答问题:
是新型磁性材料的成分。依其中有关元素回答问题:
(1)钕(Nd)属于镧系元素,则其在元素周期表中处于_______ 区,铁元素在元素周期表中的位置_______ 。
(2) 的立体构型为
的立体构型为_______ ;其中B原子的杂化方式为_______ 。
(3) 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为_______ 。
(4) 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
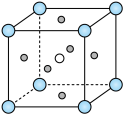
①K、Co、F的第一电离能由大到小的顺序为_______ 。
②该晶体密度为 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为_______ pm。
(5) 的制备:称取研细的
的制备:称取研细的 10.0 g和
10.0 g和 5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的
5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该的离子方程式为
溶液。写出该的离子方程式为_______ 。在制取的过程中可能还会有a.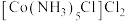 、b.
、b. 、c.
、c. 三种物质生成,物质的量相等的这三种物质分别与足量
三种物质生成,物质的量相等的这三种物质分别与足量 反应,生成AgCl的物质的量由大到小的顺序为
反应,生成AgCl的物质的量由大到小的顺序为_______ (填字母序号)。
(6)常温下,已知 电离平衡常数:
电离平衡常数: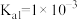 、
、 ,
, 、
、 。写出向0.1
。写出向0.1  的碳酸钠溶液中逐滴加入0.1
的碳酸钠溶液中逐滴加入0.1 
 溶液,生成沉淀的离子方程式
溶液,生成沉淀的离子方程式_______ 。
 、
、 是新型磁性材料的成分。依其中有关元素回答问题:
是新型磁性材料的成分。依其中有关元素回答问题:(1)钕(Nd)属于镧系元素,则其在元素周期表中处于
(2)
 的立体构型为
的立体构型为(3)
 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为(4)
 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
①K、Co、F的第一电离能由大到小的顺序为
②该晶体密度为
 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为(5)
 的制备:称取研细的
的制备:称取研细的 10.0 g和
10.0 g和 5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的
5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该的离子方程式为
溶液。写出该的离子方程式为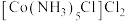 、b.
、b. 、c.
、c. 三种物质生成,物质的量相等的这三种物质分别与足量
三种物质生成,物质的量相等的这三种物质分别与足量 反应,生成AgCl的物质的量由大到小的顺序为
反应,生成AgCl的物质的量由大到小的顺序为(6)常温下,已知
 电离平衡常数:
电离平衡常数: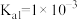 、
、 ,
, 、
、 。写出向0.1
。写出向0.1  的碳酸钠溶液中逐滴加入0.1
的碳酸钠溶液中逐滴加入0.1 
 溶液,生成沉淀的离子方程式
溶液,生成沉淀的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E、F为元素周期表中前四周期且原子序数依次增大的六种元素.其中A、B、C、D核电荷数之和为36,A、C原子的最外层电子数之和等于B原子 的次外层电子数,D原子质子数为B原子质子数的两倍,E元素所在主族均为金属,F的价电子数与C的核电荷数相等。
(1)下列关于上述几种元素的说法正确的是_________ 。
a.B、C、D的原子半径由大到小的顺序为:D >C >B
b.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F都位于周期表的3区
(2)B单质有两种同素异形体.其中在水中溶解度较大的是_______ (填化学式)。
(3)EA2和A2B熔点较高的是_______ (填化学式),原因是_________ 。
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是____ 。下列分子或离子中与DB3结构相似的是____________ 。
a. NH3 b. SO32- c.NO3- d.PCl3
(5)已知B、F能形成两种化合物,其晶胞如下图所示.则高温时甲易转化为乙的原因为___________ 。若乙晶体密度为pg/cm3,则乙晶胞的晶胞边长a =________ nm(用含P和NA的式子表示)

(1)下列关于上述几种元素的说法正确的是
a.B、C、D的原子半径由大到小的顺序为:D >C >B
b.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F都位于周期表的3区
(2)B单质有两种同素异形体.其中在水中溶解度较大的是
(3)EA2和A2B熔点较高的是
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是
a. NH3 b. SO32- c.NO3- d.PCl3
(5)已知B、F能形成两种化合物,其晶胞如下图所示.则高温时甲易转化为乙的原因为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为_________ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为_______ 。在四大晶体类型中,GaN属于_____ 晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有_________ 的原子或离子。
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:

① H、N、O三种元素的电负性由大到小的顺序是_______ 。
②SO2分子的空间构型为______ 。与SnCl4互为等电子体的一种离子的化学式为______
③乙二胺分子中氮原子轨道的杂化类型为______ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是________ 。
④⑶中所形成的配离子中含有的化学键类型有_________ 。
a.配位键 b.极性键 c.离子键 d.非极性键

⑤CuCl的晶胞结构如上图所示,其中Cl原子的配位数为_________ 。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:

① H、N、O三种元素的电负性由大到小的顺序是
②SO2分子的空间构型为
③乙二胺分子中氮原子轨道的杂化类型为
④⑶中所形成的配离子中含有的化学键类型有
a.配位键 b.极性键 c.离子键 d.非极性键

⑤CuCl的晶胞结构如上图所示,其中Cl原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】氮族元素由氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)和一种化学性质不明的合成元素镆(Mc)组成,它们的单质与化合物在工业与生活中发挥了重要作用。请回答下列问题。
(1)基态N原子的成对电子数与未成对电子数之比为___________ ,磷原子在成键时,能将一个3s电子激发到3d能级而参与成键,写出该激发态磷原子的核外电子排布式___________ 。
(2)氮、磷的简单气态氢化物的沸点的大小关系为___________ (填化学式)。
(3)咪唑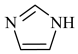 是一种五元芳杂环化合物,分子中所有原子共平面,其中氮原子的杂化方式为
是一种五元芳杂环化合物,分子中所有原子共平面,其中氮原子的杂化方式为___________ ,咪唑中所含元素电负性由大到小的顺序为___________ 。
(4)汽车产生的NO可用二氧化铈( )催化处理,
)催化处理, 能在
能在 和
和 之间改变氧化状态,将NO氧化为
之间改变氧化状态,将NO氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物 。铈氧化物晶胞发生的变化如下图所示,生成新的铈氧化物中x、y、z的最简整数比为
。铈氧化物晶胞发生的变化如下图所示,生成新的铈氧化物中x、y、z的最简整数比为___________ 。 族化合物半导体,是指元素周期表中的
族化合物半导体,是指元素周期表中的 A族与
A族与 A族元素相结合生成的化合物半导体。其中氮和硼可形成一种超硬、有优异的耐磨性能的立方氮化硼晶体,氮和镓可形成一种极稳定的六方氮化镓晶体。晶胞分别如下图所示。
A族元素相结合生成的化合物半导体。其中氮和硼可形成一种超硬、有优异的耐磨性能的立方氮化硼晶体,氮和镓可形成一种极稳定的六方氮化镓晶体。晶胞分别如下图所示。___________ 个。
②图2是纤锌矿型结构氮化镓晶胞模型图,若阿伏加德罗常数的值为 ,则纤锌矿型六方氮化镓晶体的密度
,则纤锌矿型六方氮化镓晶体的密度
___________ g⋅cm (用含a、c、
(用含a、c、 的代数式表示)。
的代数式表示)。
(1)基态N原子的成对电子数与未成对电子数之比为
(2)氮、磷的简单气态氢化物的沸点的大小关系为
(3)咪唑
 是一种五元芳杂环化合物,分子中所有原子共平面,其中氮原子的杂化方式为
是一种五元芳杂环化合物,分子中所有原子共平面,其中氮原子的杂化方式为(4)汽车产生的NO可用二氧化铈(
 )催化处理,
)催化处理, 能在
能在 和
和 之间改变氧化状态,将NO氧化为
之间改变氧化状态,将NO氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物 。铈氧化物晶胞发生的变化如下图所示,生成新的铈氧化物中x、y、z的最简整数比为
。铈氧化物晶胞发生的变化如下图所示,生成新的铈氧化物中x、y、z的最简整数比为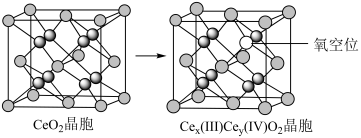
 族化合物半导体,是指元素周期表中的
族化合物半导体,是指元素周期表中的 A族与
A族与 A族元素相结合生成的化合物半导体。其中氮和硼可形成一种超硬、有优异的耐磨性能的立方氮化硼晶体,氮和镓可形成一种极稳定的六方氮化镓晶体。晶胞分别如下图所示。
A族元素相结合生成的化合物半导体。其中氮和硼可形成一种超硬、有优异的耐磨性能的立方氮化硼晶体,氮和镓可形成一种极稳定的六方氮化镓晶体。晶胞分别如下图所示。
②图2是纤锌矿型结构氮化镓晶胞模型图,若阿伏加德罗常数的值为
 ,则纤锌矿型六方氮化镓晶体的密度
,则纤锌矿型六方氮化镓晶体的密度
 (用含a、c、
(用含a、c、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮及其化合物在科学研究和化工生产等领域都有着广泛的应用。请回答下列问题:
(1)与氮元素同族的第四周期元素的基态原子价层电子轨道表达式为___________ 。
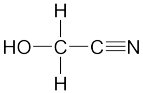
(2)HOCH2CN的结构简式如图,该分子中σ键与π键数目之比为___________ ,其分子中碳原子的杂化方式为___________ ,该物质中除氢以外的元素的第一电离能由大到小的顺序为______________________ 。
(3)[Cu(NH3)4]SO4是一种重要的配合物。与SO42-互为等电子体的分子的化学式为___________ (任写一种)。NH3的 VSEPR模型为___________ 。[Cu(NH3)4]2+的结构可用示意图表示为______________________ 。
(4)①已知:2UO2+5NH4HF2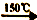 2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为
2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为___________ (填选项字母)。
A.共价键 B.配位键 C.金属键 D.离子键 E.氢键
②NH3和H2O的键角由大到小的顺序为______________________ (用分子式表示),原因是_______________________________________________________ 。
(5)Cu3N的晶胞结构如图所示,N3-的配位数为___________ ,Cu+半径为apm,N3-的半径为bpm,Cu3N晶胞的密度为___________ g/cm3(列出计算式即可,阿伏伽德罗常数的值用NA表示)。

(1)与氮元素同族的第四周期元素的基态原子价层电子轨道表达式为
(2)HOCH2CN的结构简式如图,该分子中σ键与π键数目之比为

(3)[Cu(NH3)4]SO4是一种重要的配合物。与SO42-互为等电子体的分子的化学式为
(4)①已知:2UO2+5NH4HF2
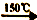 2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为
2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为A.共价键 B.配位键 C.金属键 D.离子键 E.氢键
②NH3和H2O的键角由大到小的顺序为
(5)Cu3N的晶胞结构如图所示,N3-的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】治疗疟疾的有效药物青蒿素是白色针状晶体,受热不稳定,易溶于乙醇和乙醚。按要求回答下列问题。
(1)青蒿素的提取:在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚(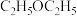 )提取,效果更好。
)提取,效果更好。
①乙醇的沸点高于乙醚,原因是___________ 。
②用乙醚提取效果更好,原因是___________ 。
(2)青蒿素的结构
①分子中C、H、O的原子半径最大的是___________ ,电负性最大的是___________ 。
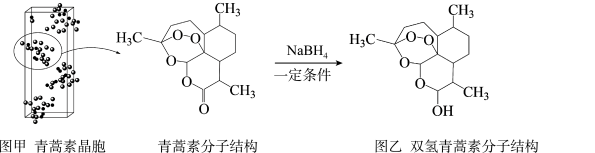
②测定晶体结构最常用的方法是___________ 、___________ ,经计算等过程得出其晶胞(长方体,棱长分别为a nm、b nm、c m,含4个青蒿素分子)及分子结构如下图甲所示。
③测定其分子的相对分子质量为282,其物理方法是___________ 。
④晶体的密度为___________  (阿伏加德罗常数的值设为
(阿伏加德罗常数的值设为 ;列出表达式)。
;列出表达式)。
(3)青蒿素结构的修饰:一定条件下,用 将青蒿素选择性反应,结构修饰为双氢青蒿素(如上图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如上图乙)。
①青蒿素结构修饰发生的反应类型为___________ ,其过程中杂化轨道发生变化的碳原子的杂化方式变为___________ 。
② 的空间结构名称为
的空间结构名称为___________ 。
③从结构与性质关系的角度推测双氢青蒿素比青蒿素的水溶性、疗效更好的原因:___________ 。
(1)青蒿素的提取:在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚(
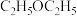 )提取,效果更好。
)提取,效果更好。①乙醇的沸点高于乙醚,原因是
②用乙醚提取效果更好,原因是
(2)青蒿素的结构
①分子中C、H、O的原子半径最大的是
②测定晶体结构最常用的方法是

③测定其分子的相对分子质量为282,其物理方法是
④晶体的密度为
 (阿伏加德罗常数的值设为
(阿伏加德罗常数的值设为 ;列出表达式)。
;列出表达式)。(3)青蒿素结构的修饰:一定条件下,用
 将青蒿素选择性反应,结构修饰为双氢青蒿素(如上图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如上图乙)。①青蒿素结构修饰发生的反应类型为
②
 的空间结构名称为
的空间结构名称为③从结构与性质关系的角度推测双氢青蒿素比青蒿素的水溶性、疗效更好的原因:
您最近一年使用:0次



