某密闭容器中有如下可逆反应:2SO2(g)+O2(g) 2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。
2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。
(1)升高温度,v(正)___ ,v(逆)___ ,SO2的转化率___ 。
(2)加正催化剂,v(正)___ ,v(逆)___ ,O2的物质的量___ 。
(3)缩小容器的体积,SO3的物质的量___ ,SO2的转化率___ 。
(4)该反应的平衡常数K值的表达式:K=___ ;升高温度,K值将___ 。
 2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。
2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。(1)升高温度,v(正)
(2)加正催化剂,v(正)
(3)缩小容器的体积,SO3的物质的量
(4)该反应的平衡常数K值的表达式:K=
20-21高二上·新疆乌鲁木齐·期中 查看更多[2]
更新时间:2021-06-16 15:58:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据在298K时,实验测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时的速率表,请与同学们交流研讨:
(1)补充表中的相应数据:
(2)找出化学反应速率与H2O2浓度、HI浓度之间的关系,并尝试写出相应的数学表达式____ 。
(1)补充表中的相应数据:
| 试验编号 | 1 | 2 | 3 | 4 | 5 |
| c(HI)/(mol/L) | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
| c(H2O2)/(mol/L) | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
| v/(mol·L-1·s-1) |
(2)找出化学反应速率与H2O2浓度、HI浓度之间的关系,并尝试写出相应的数学表达式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)在某一容积为2 L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:
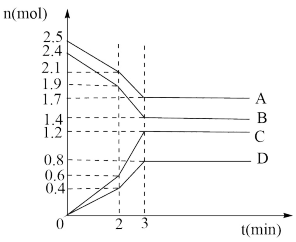
回答下列问题:
①该反应的化学方程式为______ ;
②前2 min用A的浓度变化表示的化学反应速率为____ ,在2 min时,图象发生改变的原因是_______ (填字母)。
A 增大压强 B 降低温度 C 加入催化剂 D 增加A的物质的量
(2)在100 ℃时,将0.01 mol的四氧化二氮气体充入0.1 L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:
①该反应的化学方程式_______ ,达到平衡时四氧化二氮的转化率为____ ;
②反应速率最大的时间段为____ (指0~20s、20~40s、40~60s、60~80s、80~100 s),其原因是_____________

回答下列问题:
①该反应的化学方程式为
②前2 min用A的浓度变化表示的化学反应速率为
A 增大压强 B 降低温度 C 加入催化剂 D 增加A的物质的量
(2)在100 ℃时,将0.01 mol的四氧化二氮气体充入0.1 L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
时间/s 浓度/mol·L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L-1 | 0.100 | 0.070 | 0.050 | c3 | a | b |
| c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
①该反应的化学方程式
②反应速率最大的时间段为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在下列事实中,影响反应速率的外界条件分别为:
(1)夏天的食品易霉变,放置在冰箱中不易发生该现象,影响反应速率的外界条件_________ ;
(2)在5%的H2O2溶液中加入1滴~2滴1 mol/L FeCl3溶液,很快产生气体,影响反应速率的外界条件______________________________________ ;
(3)工业合成氨通常采用200~500个大气压下进行。影响反应速率的外部条件____________ ;
(4)铁丝在纯氧中剧烈燃烧,火星四溅,影响反应速率的外界条件______________________ 。
(1)夏天的食品易霉变,放置在冰箱中不易发生该现象,影响反应速率的外界条件
(2)在5%的H2O2溶液中加入1滴~2滴1 mol/L FeCl3溶液,很快产生气体,影响反应速率的外界条件
(3)工业合成氨通常采用200~500个大气压下进行。影响反应速率的外部条件
(4)铁丝在纯氧中剧烈燃烧,火星四溅,影响反应速率的外界条件
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在200℃和a℃时,反应X(g) 4Y(g)+Z(g)中X的浓度随时间变化的关系如图所示。
4Y(g)+Z(g)中X的浓度随时间变化的关系如图所示。
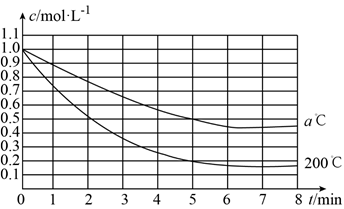
(1)200℃时5min内用Y表示的平均反应速率为__________ 。
(2)200℃、8min时,Z的浓度为__________ 。
(3)200℃时,在__________ 时,反应达到平衡状态。
(4)200℃、7min时,v正__________ v逆(填“>”、“<”或“=”)。
(5)从图中可以看出,a__________ 200(填“>”、“<”或“=”)。
 4Y(g)+Z(g)中X的浓度随时间变化的关系如图所示。
4Y(g)+Z(g)中X的浓度随时间变化的关系如图所示。
(1)200℃时5min内用Y表示的平均反应速率为
(2)200℃、8min时,Z的浓度为
(3)200℃时,在
(4)200℃、7min时,v正
(5)从图中可以看出,a
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】CrO 和Cr2O
和Cr2O 在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O
在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O )随c(H+)的变化如图所示。
)随c(H+)的变化如图所示。
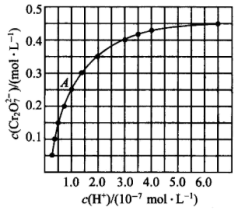
(1)向黄色的K2CrO4溶液中滴加稀硫酸,溶液变为橙色,用离子方程式表示该转化反应:_____ 。
(2)下列可判断转化反应达到平衡的是_____ (填标号)。
a.溶液的pH不再变化 b.v(H+)=2v(Cr2O )
)
c.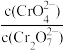 不再变化 d.c(CrO
不再变化 d.c(CrO )=0.45mol/L
)=0.45mol/L
(3)由图可知,溶液酸性增强,CrO 的平衡转化率
的平衡转化率_____ (填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为_____ 。
(4)升高温度,溶液中CrO 的平衡转化率减小,则该反应的△H
的平衡转化率减小,则该反应的△H____ 0(填“>”“<”或“=”)。
 和Cr2O
和Cr2O 在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O
在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O )随c(H+)的变化如图所示。
)随c(H+)的变化如图所示。
(1)向黄色的K2CrO4溶液中滴加稀硫酸,溶液变为橙色,用离子方程式表示该转化反应:
(2)下列可判断转化反应达到平衡的是
a.溶液的pH不再变化 b.v(H+)=2v(Cr2O
 )
)c.
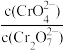 不再变化 d.c(CrO
不再变化 d.c(CrO )=0.45mol/L
)=0.45mol/L(3)由图可知,溶液酸性增强,CrO
 的平衡转化率
的平衡转化率(4)升高温度,溶液中CrO
 的平衡转化率减小,则该反应的△H
的平衡转化率减小,则该反应的△H
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】溶液中存在各种平衡体系。
(1)氨水溶液中存在电离平衡,NH3·H2O的电离方程式是___ 。升高温度时,NH3·H2O的电离程度___ (填“增大”、“减小”或“不变”。下同)。稀释时,NH3·H2O的电离程度___ 。
(2)向黄色的FeCl3溶液加入无色的KSCN溶液,溶液变成血红色,建立了如下平衡:Fe3++3SCN- Fe(SCN)3。
Fe(SCN)3。
①若向溶液中加入少量KSCN固体,实验现象是___ ,用化学平衡原理解释该现象产生的原因是___ 。
②若向溶液中加入几滴浓NaOH溶液,实验现象是___ 。
(1)氨水溶液中存在电离平衡,NH3·H2O的电离方程式是
(2)向黄色的FeCl3溶液加入无色的KSCN溶液,溶液变成血红色,建立了如下平衡:Fe3++3SCN-
 Fe(SCN)3。
Fe(SCN)3。①若向溶液中加入少量KSCN固体,实验现象是
②若向溶液中加入几滴浓NaOH溶液,实验现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在2L密闭容器内,800℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)写出该反应的平衡常数表达式:K=__________ 。
(2)0~2 s内该反应的平均速率v(NO)=__________ , v(O2)=__________ 。
(3)能说明该反应已达到平衡状态的是__________ 。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是__________ 。
a.及时分离出NO2气体 b.增大O2的浓度
c.扩大容器体积 d.选择高效催化剂
 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=
(2)0~2 s内该反应的平均速率v(NO)=
(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.增大O2的浓度
c.扩大容器体积 d.选择高效催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在一密闭容器中发生反应N2(g)+3H2(g) 2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是_________ 。
A.增大压强 B.降低温度 C.使用催化剂 D.增大反应物的浓度
(2)上述反应达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
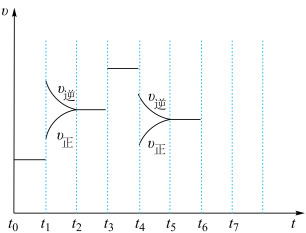
t1、t3、t4时刻分别改变了反应的一个条件,其中t1时刻改变的条件是________ ;某时刻改变的条件是保持压强不变,向容器中冲入氩气,这个时刻是________ 。
(3)下列时间段中,混合气体中氮气百分含量最高的是________ ,氢气浓度最大的是________
A.t0~t1 B.t2~t3 C.t4~t5 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为________ 。
(5)合成氨及其相关工业中,部分物质间的转化关系如下:
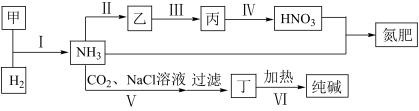
下列说法不正确的是( )
A.甲、乙、丙三种物质都含有氮元素
B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用
D.丁为NaHCO3
E. V过程中先通入CO2 ,再通入NH3
 2NH3(g) ΔH<0
2NH3(g) ΔH<0(1)改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是
A.增大压强 B.降低温度 C.使用催化剂 D.增大反应物的浓度
(2)上述反应达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。

t1、t3、t4时刻分别改变了反应的一个条件,其中t1时刻改变的条件是
(3)下列时间段中,混合气体中氮气百分含量最高的是
A.t0~t1 B.t2~t3 C.t4~t5 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为
(5)合成氨及其相关工业中,部分物质间的转化关系如下:

下列说法不正确的是
A.甲、乙、丙三种物质都含有氮元素
B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用
D.丁为NaHCO3
E. V过程中先通入CO2 ,再通入NH3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】水蒸气通过炙热的碳层发生反应:C(s)+H2O(g) CO(g)+H2(g) △H。
CO(g)+H2(g) △H。
(1)已知:K(300℃)<K(350℃),则该反应是__ (吸或放)热反应。
(2)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图所示,填出对应的编号。
①缩小容器体积__ ;②降低温度__ 。

(3)已知反应①CO(g)+CuO(g) CO2(g)+Cu(s);②H2(g)+CuO(g)
CO2(g)+Cu(s);②H2(g)+CuO(g) Cu(s)+H2O(g);在相同的某温度下的平衡常数分别为K1和K2,该温度下反应CO (g)+H2O (g)
Cu(s)+H2O(g);在相同的某温度下的平衡常数分别为K1和K2,该温度下反应CO (g)+H2O (g) CO2(g)+H2(g)的平衡常数K=
CO2(g)+H2(g)的平衡常数K=__ (用K1和K2表示)。
 CO(g)+H2(g) △H。
CO(g)+H2(g) △H。(1)已知:K(300℃)<K(350℃),则该反应是
(2)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图所示,填出对应的编号。
①缩小容器体积

(3)已知反应①CO(g)+CuO(g)
 CO2(g)+Cu(s);②H2(g)+CuO(g)
CO2(g)+Cu(s);②H2(g)+CuO(g) Cu(s)+H2O(g);在相同的某温度下的平衡常数分别为K1和K2,该温度下反应CO (g)+H2O (g)
Cu(s)+H2O(g);在相同的某温度下的平衡常数分别为K1和K2,该温度下反应CO (g)+H2O (g) CO2(g)+H2(g)的平衡常数K=
CO2(g)+H2(g)的平衡常数K=
您最近一年使用:0次



