在四个恒容密闭容器中按下表相应量充入气体,发生反应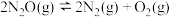 ,容器I、II、III中
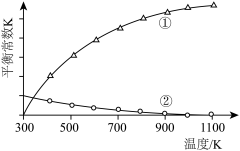
,容器I、II、III中 的平衡转化率如图所示,下列说法正确的是
的平衡转化率如图所示,下列说法正确的是
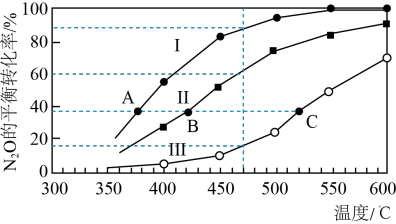
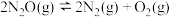 ,容器I、II、III中
,容器I、II、III中 的平衡转化率如图所示,下列说法正确的是
的平衡转化率如图所示,下列说法正确的是
| 容器 | 容积/L | 起始物质的量/mol | ||
 |  |  | ||
| I | V1 | 0.1 | 0 | 0 |
| II | 1.0 | 0.1 | 0 | 0 |
| III | V2 | 0.1 | 0 | 0 |
| IV | 1.0 | 0.06 | 0.06 | 0.04 |
| A.该反应的正反应放热 |
B.相同温度下反应达到平衡时,平均反应速率: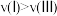 |
C.图中A、B、C三点处容器内总压强: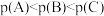 |
D.容器IV在470℃进行反应时,起始速率: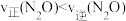 |
17-18高二下·湖南长沙·开学考试 查看更多[8]
2.3.3化学平衡中的图像问题 课后河南省濮阳市第一高级中学2022-2023学年高三年级上学期期中考试化学试题黑龙江省哈尔滨市第九中学2022届高三上学期10月月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)湖南省岳阳县一中2022届高三年级入学考试化学试题选择性必修1 专题2 第三单元 突破3 化学平衡图像分析重庆市重点中学2021届高三下学期开学考试(新高考)化学试题湖南省长沙市长郡中学2017-2018学年高二下学期开学考试化学试题
更新时间:2021-08-07 18:44:00
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】汽车尾气处理存在反应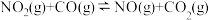 ,该反应过程及能量变化如图所示。下列说法错误的是
,该反应过程及能量变化如图所示。下列说法错误的是
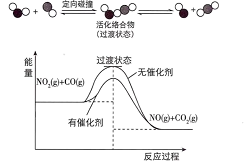
 ,该反应过程及能量变化如图所示。下列说法错误的是
,该反应过程及能量变化如图所示。下列说法错误的是
| A.升高温度,平衡逆向移动 |
| B.反应物转化为活化络合物需要吸收能量 |
C.该反应生成了具有非极性共价键的 |
| D.使用催化剂可以降低活化能,加快反应速率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图所示,在密闭容器中发生反应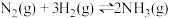
 ,达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
,达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
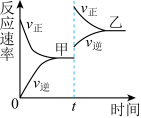
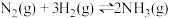
 ,达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
,达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
| A.加入适当催化剂 | B.升高温度 |
| C.增大反应物的浓度 | D.增大压强 |
您最近半年使用:0次
单选题
|
适中
(0.65)
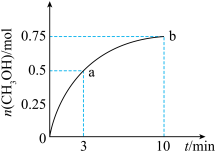
【推荐3】某温度下,在容积为1L的密闭容器中充入1molCO2和3.25molH2,发生CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,测得CH3OH的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数K=2.25)下列说法正确的是
CH3OH(g)+H2O(g) △H<0,测得CH3OH的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数K=2.25)下列说法正确的是
 CH3OH(g)+H2O(g) △H<0,测得CH3OH的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数K=2.25)下列说法正确的是
CH3OH(g)+H2O(g) △H<0,测得CH3OH的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数K=2.25)下列说法正确的是
| A.0-10min,v(H2)=0.075 mol/(L·min) |
| B.点 b 所对应的状态没有达到化学平衡状态 |
| C.CH3OH 的生成速率,点 a 大于点 b |
D.欲增大平衡状态时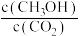 ,可保持其他条件不变,升高温度 ,可保持其他条件不变,升高温度 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:[Cu(NH3)2]++CO+NH3 [Cu(NH3)3CO]+ △H<0。下列说法正确的是
[Cu(NH3)3CO]+ △H<0。下列说法正确的是
 [Cu(NH3)3CO]+ △H<0。下列说法正确的是
[Cu(NH3)3CO]+ △H<0。下列说法正确的是| A.原料气在进入合成塔前进行处理,可防止催化剂中毒 |
| B.铜氨液吸收CO适宜的生产条件是高温低压 |
| C.该反应可自发进行,熵增 |
| D.吸收CO后铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用,铜氨液再生适宜的生产条件是低温高压 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在某刚性容器中发生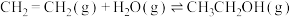
 ,下列说法正确的是
,下列说法正确的是
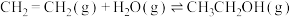
 ,下列说法正确的是
,下列说法正确的是A.恒温恒容条件下,增大 的物质的量,则 的物质的量,则 的平衡转化率增大 的平衡转化率增大 |
| B.恒温恒压条件下达到平衡状态,再通入适量氮气,平衡逆向移动,平衡常数减小 |
C.恒温恒容条件下达到平衡状态,升高温度,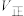 增大, 增大,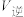 增大,平衡向逆反应方向移动 增大,平衡向逆反应方向移动 |
D.加入催化剂,能缩短达到平衡时间,并提高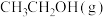 的平衡产率 的平衡产率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】关于化学平衡常数的叙述中正确的是
| A.温度一定,一个化学反应的平衡常数不是一个常数 |
| B.两种物质反应,不管如何书写化学方程式,平衡常数不变 |
| C.温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数 |
| D.某一时刻,当生成物浓度幂之积与反应物浓度幂之积的比值小于该温度下的平衡常数时,v正<v逆 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
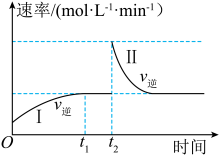
【推荐2】在某一恒温体积可变的密闭容器中发生反应:X(g)+Y(g) 2Z(g) ΔH<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程中逆反应速率变化如图所示。下列说法正确的是
2Z(g) ΔH<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程中逆反应速率变化如图所示。下列说法正确的是
 2Z(g) ΔH<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程中逆反应速率变化如图所示。下列说法正确的是
2Z(g) ΔH<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程中逆反应速率变化如图所示。下列说法正确的是
| A.O~t2时,v正>v逆 |
| B.t2时刻改变的条件是向密闭容器中加Z |
| C.t2时刻改变的条件是从密闭容器中抽出了Y |
| D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ |
您最近半年使用:0次
【推荐1】在一恒容的密闭容器中充入0.1mol/LCO2、0.1mol/LCH4,在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是( )
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是( )

 2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是( )
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是( )
| A.上述反应的ΔH>0 |
| B.压强:p4>p3>p2>p1 |
| C.1100℃时该反应平衡常数约为1.64 |
| D.压强为p4时,在y点:v(正)<v(逆) |
您最近半年使用:0次
单选题
|
适中
(0.65)
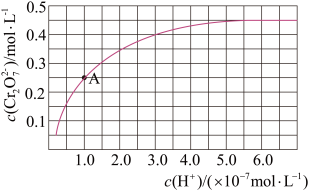
【推荐2】已知: 。25℃时,调节初始浓度为1.0 mol•L-1的Na2CrO4溶液的pH(忽略溶液体积变化),测定平衡时溶液中c(
。25℃时,调节初始浓度为1.0 mol•L-1的Na2CrO4溶液的pH(忽略溶液体积变化),测定平衡时溶液中c( )和c(H+),获得如图所示的曲线。下列说法不正确的是( )
)和c(H+),获得如图所示的曲线。下列说法不正确的是( )
 。25℃时,调节初始浓度为1.0 mol•L-1的Na2CrO4溶液的pH(忽略溶液体积变化),测定平衡时溶液中c(
。25℃时,调节初始浓度为1.0 mol•L-1的Na2CrO4溶液的pH(忽略溶液体积变化),测定平衡时溶液中c( )和c(H+),获得如图所示的曲线。下列说法不正确的是( )
)和c(H+),获得如图所示的曲线。下列说法不正确的是( )
A.平衡时,pH越小,c( )越大 )越大 |
B.A点 的平衡转化率为50% 的平衡转化率为50% |
C.A点 -转化为 -转化为 反应的平衡常数K=1014 反应的平衡常数K=1014 |
D.平衡时,若溶液中c( )=c( )=c( ),则c(H+)>2.0×10-7 mol·L-1 ),则c(H+)>2.0×10-7 mol·L-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定条件下,用 Fe2O3、 NiO 或 Cr2O3作催化剂对燃煤烟气进行回收,使 SO2转化生成为 S。催化剂不同,相同其他条件(浓度、温度、压强)情况下, 相同时间内 SO2的转化率随反应温度的变化如下图:下列说法不正确的是
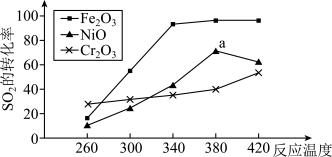

| A.不考虑催化剂价格因素,选择 Fe2O3作催化剂可以节约能源 |
| B.相同其他条件下,选择 Cr2O3作催化剂, SO2的平衡转化率最小 |
| C.a 点后 SO2的转化率减小的原因可能是温度升高催化剂活性降低了 |
| D.选择 Fe2O3作催化剂,最适宜温度为 340~380℃温度范围 |
您最近半年使用:0次

 的能量变化如图所示。下列说法错误的是
的能量变化如图所示。下列说法错误的是
 和
和 总键能小于
总键能小于 和
和 的总键能
的总键能
 的转化率增大
的转化率增大 的平衡常数为
的平衡常数为


