11. 温室气体的利用是当前环境和能源领域的研究热点。
I.CH
4与CO
2重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
反应①CH
4(g) + CO
2(g)
⇌2CO(g)+2H
2 (g) Δ
H1反应②CO
2 (g)+ H
2 (g)
⇌CO(g) + H
2O(g) Δ
H2= +41.2 kJ·mol
-1反应③CH
4 (g)+

O
2(g)
⇌CO(g) + 2H
2(g) Δ
H3 = -35.6 kJ·mol
-1(1)已知:

O
2(g)+H
2(g)= H
2O(g) Δ
H = -241.8 kJ·mol
-1,则Δ
H1 =
______ kJ·mol
-1。
(2)一定条件下,向体积为VL的密闭容器中通入CH
4、CO
2各1.0 mol及少量O
2,测得不同温度下反应平衡时各产物产量如图所示。
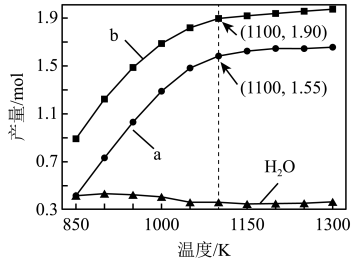
①图中a和b分别代表产物
______和
______,当温度高于900 K, H
2O的含量随温度升高而下降的主要原因是
______。
②1100 K时,CH
4与CO
2的转化率分别为95%和90%,反应①的平衡常数K=
______ ( 写出计算式)。
II.Ni-CeO
2催化CO
2加H
2形成CH
4的反应历程如图1所示(吸附在催化剂表面的物种用*标注),含碳产物中CH
4的物质的量百分数(Y)及CO
2的转化率随温度的变化如图2所示。

(3)下列对CO
2甲烷化反应体系的说法合理的有
______。
A.含碳副产物的产率均低于CH
4B.存在反应CO
2+4H
2⇌CH
4 + 2H
2O
C.存在副反应CO
2+ H
2⇌CO+ H
2O
D. CO
2 转化为CH
4的过程中发生了能量转化
E.温度高于260℃后,升高温度,甲烷产率几乎不变
(4) CO
2甲烷化的过程中,保持CO
2与H
2的体积比为1:4,反应气的总流量控制在40 mL·min
-1,320 ℃时测得CO
2转化率为80%,则CO
2反应速率为
______mL·min
-1。