化石燃料的燃烧会产生大量污染大气的二氧化硫和温室气体二氧化碳。而氢气和氨气都被认为是无碳无污染的清洁能源。
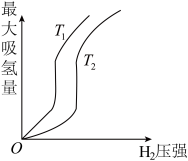
(1)某些合金可用于储存氢,金属储氢的原理可表示为:M+xH2⇌MH2x △H<0 (M 表示某种合金)。如图表示温度分别为T1、T2时,最大吸氢量与氢气压强的关系。则下列说法中,正确的是_______。
(2)以熔融碳酸盐为电解质,稀土金属材料为电极组成氢氧燃料电池(如下图装置甲所示),其中负极通入H2,正极通入O2和CO2的混合气体。乙装置中a、b为石墨,电解一段时间后,b电极附近滴入酚酞溶液变红,NaCl溶液的体积为100mL。
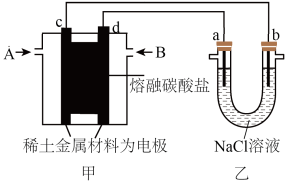
①工作过程中,甲装置中d电极的电极反应式为_______ ,乙装置中电极a为_______ 极(填电极名称)。
②若在a极产生112mL(标准状况)气体,25°C时乙装置中所得溶液pH=_______ 。(忽略电解前后溶液体积变化)
(3)氨在氧气中燃烧,生成水和一种空气组成成分的单质。
已知:N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ·mol-1
2H2(g) +O2(g) =2H2O(l) △H= -572 kJ·mol-1
试写出氨在氧气中燃烧生成液态水的热化学方程式:_______ 。
(4)在一定条件下,将1molN2和3molH2混合于一个10L的容积不变的密闭容器中发生反应:N2+3H2 2NH3△H<0,已知5分钟后达到平衡,平衡时氨的体积分数为25%。
2NH3△H<0,已知5分钟后达到平衡,平衡时氨的体积分数为25%。
①该反应的平衡常数表达式为_______ ;
②反应开始到平衡时N2的消耗速率v(N2)=_______ ;
③能判断该反应是否达到化学平衡状态的依据是_______ ;
a.容器中压强不变
b.混合气体的密度不变
c.3v正(H2)=2v逆(NH3)
d.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
④对于上述平衡状态,改变下列条件能使反应速率增大,且能使平衡向正反应方向移动的是_______ 。
a.选用更高效的催化剂
b.升高温度
c.及时分离出氨气
d.增加H2的依度
e.充入He,使体系总压强增大
(1)某些合金可用于储存氢,金属储氢的原理可表示为:M+xH2⇌MH2x △H<0 (M 表示某种合金)。如图表示温度分别为T1、T2时,最大吸氢量与氢气压强的关系。则下列说法中,正确的是_______。

| A.T1>T2 |
| B.增大氢气压强,加快氢气的吸收速率 |
| C.增大M的量,上述平衡向右移动 |
| D.上述反应可实现多次储存和释放氢气 |

①工作过程中,甲装置中d电极的电极反应式为
②若在a极产生112mL(标准状况)气体,25°C时乙装置中所得溶液pH=
(3)氨在氧气中燃烧,生成水和一种空气组成成分的单质。
已知:N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ·mol-1
2H2(g) +O2(g) =2H2O(l) △H= -572 kJ·mol-1
试写出氨在氧气中燃烧生成液态水的热化学方程式:
(4)在一定条件下,将1molN2和3molH2混合于一个10L的容积不变的密闭容器中发生反应:N2+3H2
 2NH3△H<0,已知5分钟后达到平衡,平衡时氨的体积分数为25%。
2NH3△H<0,已知5分钟后达到平衡,平衡时氨的体积分数为25%。①该反应的平衡常数表达式为
②反应开始到平衡时N2的消耗速率v(N2)=
③能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变
b.混合气体的密度不变
c.3v正(H2)=2v逆(NH3)
d.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
④对于上述平衡状态,改变下列条件能使反应速率增大,且能使平衡向正反应方向移动的是
a.选用更高效的催化剂
b.升高温度
c.及时分离出氨气
d.增加H2的依度
e.充入He,使体系总压强增大
更新时间:2021-08-13 09:20:54
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】研究二氧化碳的回收对我国2060年实现碳中和具有现实意义:
(1)以 与
与 为原料可合成尿素[
为原料可合成尿素[ ]回收
]回收 并为农业服务,
并为农业服务,
已知:反应I.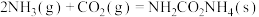
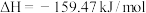
反应II.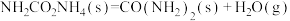
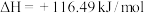
在相同条件下,反应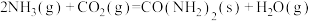 正反应的活化能
正反应的活化能 为8179kJ/mol,则逆反应的活化能
为8179kJ/mol,则逆反应的活化能 为
为_______ 。
(2)向一体积为1L的密闭容器中通入 和
和 发生反应:
发生反应:

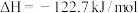 。
。 的平衡转化率与压强、温度及氢碳比m[
的平衡转化率与压强、温度及氢碳比m[ ]的关系分别如图a和图b所示。
]的关系分别如图a和图b所示。

图a中压强从大到小的顺序为_______ ,图b中氢碳比m从大到小的顺序为_______ 。
(3)工业上也可利用NaOH溶液捕获 。
。
①1L 1mol/L的NaOH溶液捕获标准状况下16.8L 所得溶液中,所有离子浓度由大到小的顺序为
所得溶液中,所有离子浓度由大到小的顺序为_______ 。
②若所得溶液中 ,溶液pH=
,溶液pH=_______ 。(室温下, 的
的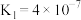 ;
;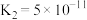 )
)
(4)工业上也可以用电解法捕获 ,如图,
,如图, 在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所示,则b电极上的电极反应为
在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所示,则b电极上的电极反应为_______ 。

(1)以
 与
与 为原料可合成尿素[
为原料可合成尿素[ ]回收
]回收 并为农业服务,
并为农业服务,已知:反应I.
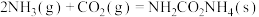
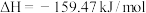
反应II.
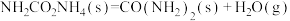
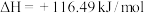
在相同条件下,反应
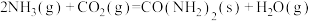 正反应的活化能
正反应的活化能 为8179kJ/mol,则逆反应的活化能
为8179kJ/mol,则逆反应的活化能 为
为(2)向一体积为1L的密闭容器中通入
 和
和 发生反应:
发生反应:

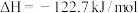 。
。 的平衡转化率与压强、温度及氢碳比m[
的平衡转化率与压强、温度及氢碳比m[ ]的关系分别如图a和图b所示。
]的关系分别如图a和图b所示。
图a中压强从大到小的顺序为
(3)工业上也可利用NaOH溶液捕获
 。
。①1L 1mol/L的NaOH溶液捕获标准状况下16.8L
 所得溶液中,所有离子浓度由大到小的顺序为
所得溶液中,所有离子浓度由大到小的顺序为②若所得溶液中
 ,溶液pH=
,溶液pH= 的
的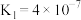 ;
;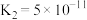 )
)(4)工业上也可以用电解法捕获
 ,如图,
,如图, 在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所示,则b电极上的电极反应为
在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所示,则b电极上的电极反应为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】火力发电厂释放出大量氮的氧化物(NOx)、二氧化硫等气体会造成环境污染,对燃煤废气进行脱除处理。可实现绿色环保、低碳减排、废物利用等目的。
(1)已知:N2(g) +O2(g) =2NO (g) △H=+180.5kJ·mol-1
C (s) +O2(g)=CO2(g) △H=-393.5 kJ·mol-1
2C (s) +O2(g) =2CO (g)△H=-221 kJ·mol-1
若某反应的平衡常数表达式为: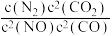 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式_________ 。
(2)脱硝
利用甲烷与NO2反应,生成无污染的物质,则该反应的化学方程式为:___________ 。
(3)脱碳
将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线(见如图1),则上述CO2转化为甲醇反应的△H3_____ 0(填“>”、“<”或“=”)。
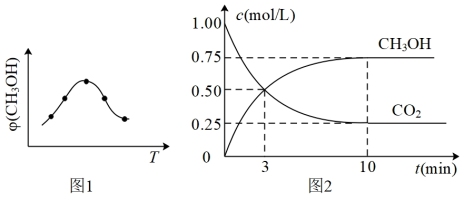
②在一恒温恒容密闭容器中充入0.5molCO2和1.5molH2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如上图2所示,请回答:第10min后,若升温,该反应的平衡常数将_____ (填“变大”、“变小”、“不变”);若向该容器中再充入1molCO2和3molH2再次达到平衡时,则CH3OH(g)的体积分数将___ (“变大”、“变小”、“不变”)。
(4)脱硫
某种脱硫工艺中将废气经处理后,与一定量的氨气、潮湿的空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥,设烟气中的SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为__________ 。若在0.1mol/L的硝酸铵溶液中加入等体积的0.09mol/L氨水,配制了pH=8.2的溶液,则该溶液中微粒浓度由大到小的顺序为______________ 。
(1)已知:N2(g) +O2(g) =2NO (g) △H=+180.5kJ·mol-1
C (s) +O2(g)=CO2(g) △H=-393.5 kJ·mol-1
2C (s) +O2(g) =2CO (g)△H=-221 kJ·mol-1
若某反应的平衡常数表达式为:
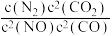 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(2)脱硝
利用甲烷与NO2反应,生成无污染的物质,则该反应的化学方程式为:
(3)脱碳
将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3①取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线(见如图1),则上述CO2转化为甲醇反应的△H3

②在一恒温恒容密闭容器中充入0.5molCO2和1.5molH2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如上图2所示,请回答:第10min后,若升温,该反应的平衡常数将
(4)脱硫
某种脱硫工艺中将废气经处理后,与一定量的氨气、潮湿的空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥,设烟气中的SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】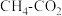 催化重整不仅可以得到CO和
催化重整不仅可以得到CO和 ,还对温室气体的减排具有重要意义。回答下列问题:
,还对温室气体的减排具有重要意义。回答下列问题:
(1)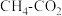 催化重整反应为:
催化重整反应为: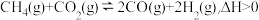
①有利于提高CH4平衡转化率的条件是___________ (填字母)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②在体积恒定的密闭容器中进行该反应并达到平衡状态,若此时改变条件使平衡常数K值变大,该反应___________ (填字母)。
A.一定向正反应方向移动 B.重新达到平衡后正反应速率增大
C.一定向逆反应方向移动 D.重新达到平衡后逆反应速率减小
③某温度下,在体积为2L的容器中加入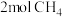 、
、 以及催化剂进行重整反应,达到平衡时
以及催化剂进行重整反应,达到平衡时 的转化率是50%,
的转化率是50%, 的体积分数为
的体积分数为___________ ,该温度下的平衡常数为___________ (可保留分数)。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
①由上表判断,催化剂X___________ Y(填“优于”或“劣于”),理由是___________ 。
②在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是___________ (填标号)。

A.K积、K消均增加 B.v积减小、v消增加
C.K积减小、K消增加 D.v消增加的倍数比v积增加的倍数大
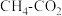 催化重整不仅可以得到CO和
催化重整不仅可以得到CO和 ,还对温室气体的减排具有重要意义。回答下列问题:
,还对温室气体的减排具有重要意义。回答下列问题:(1)
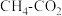 催化重整反应为:
催化重整反应为: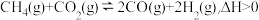
①有利于提高CH4平衡转化率的条件是
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②在体积恒定的密闭容器中进行该反应并达到平衡状态,若此时改变条件使平衡常数K值变大,该反应
A.一定向正反应方向移动 B.重新达到平衡后正反应速率增大
C.一定向逆反应方向移动 D.重新达到平衡后逆反应速率减小
③某温度下,在体积为2L的容器中加入
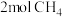 、
、 以及催化剂进行重整反应,达到平衡时
以及催化剂进行重整反应,达到平衡时 的转化率是50%,
的转化率是50%, 的体积分数为
的体积分数为(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
积碳反应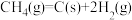 | 消碳反应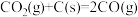 | ||
 /(kJ/mol) /(kJ/mol) | +75 | +172 | |
| 活化能(kJ/mo)l | 催化剂X | 33 | 91 |
| 催化剂Y | 43 | 72 | |
②在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是

A.K积、K消均增加 B.v积减小、v消增加
C.K积减小、K消增加 D.v消增加的倍数比v积增加的倍数大
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为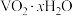 、
、 及少量的
及少量的 一种初步分离钒铬还原渣中钒铬并获得
一种初步分离钒铬还原渣中钒铬并获得 的工艺流程如图。
的工艺流程如图。

已知:①“酸浸”后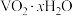 转化为
转化为 ;②
;② ;③
;③ 的
的 近似为
近似为 ;
;
④有关物质的溶解度(g/100g )如表所示:
)如表所示:
回答下列问题:
(1)写出“滤渣”的一种用途___________ ,“氧化”生成 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)若“含 净化液”中
净化液”中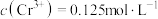 ,则“水解沉钒”调pH的范围是2.5~
,则“水解沉钒”调pH的范围是2.5~___________ 。(结果保留1位小数)
(3)“溶液1”中含 ,加入
,加入 后发生的化学反应方程式为
后发生的化学反应方程式为___________ 。
(4)“溶液2调pH”,所发生反应的离子方程式___________ 。
(5)“多步操作”包括蒸发浓缩、___________ 、冷却结晶、过滤、洗涤等步骤。
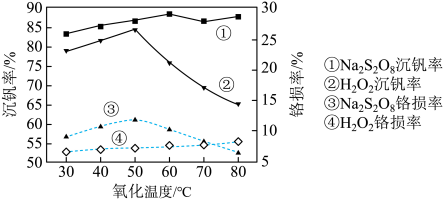
(6)研究温度对 与
与 的氧化-水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在80℃左右,降低温度能耗增加。由图可知,分别采用
的氧化-水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在80℃左右,降低温度能耗增加。由图可知,分别采用 、
、 进行“氧化”时,应选择的适宜温度是
进行“氧化”时,应选择的适宜温度是___________ 、___________ 。
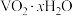 、
、 及少量的
及少量的 一种初步分离钒铬还原渣中钒铬并获得
一种初步分离钒铬还原渣中钒铬并获得 的工艺流程如图。
的工艺流程如图。
已知:①“酸浸”后
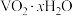 转化为
转化为 ;②
;② ;③
;③ 的
的 近似为
近似为 ;
;④有关物质的溶解度(g/100g
 )如表所示:
)如表所示:| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
 | 183.6 | 215.1 | 269.2 | 376.4 | 415.0 |
 | 19.5 | 48.8 | 45.3 | 43.7 | 42.5 |
(1)写出“滤渣”的一种用途
 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为(2)若“含
 净化液”中
净化液”中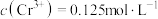 ,则“水解沉钒”调pH的范围是2.5~
,则“水解沉钒”调pH的范围是2.5~(3)“溶液1”中含
 ,加入
,加入 后发生的化学反应方程式为
后发生的化学反应方程式为(4)“溶液2调pH”,所发生反应的离子方程式
(5)“多步操作”包括蒸发浓缩、
(6)研究温度对
 与
与 的氧化-水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在80℃左右,降低温度能耗增加。由图可知,分别采用
的氧化-水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在80℃左右,降低温度能耗增加。由图可知,分别采用 、
、 进行“氧化”时,应选择的适宜温度是
进行“氧化”时,应选择的适宜温度是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】Ⅰ.某易溶于水的正盐X由3种元素组成,兴趣小组对化合物X开展探究实验。

①A和B均为纯净物,生成的A全部逸出,且可使品红溶液褪色。
②溶液C中的溶质只含一种阴离子,进行焰色反应,发现透过蓝色钴玻片,火焰呈紫色;
③用酸性: 标准溶液滴定用5.40gX配成的溶液,发生反应:
标准溶液滴定用5.40gX配成的溶液,发生反应: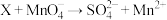 ,消耗0.032mol
,消耗0.032mol 。(注:忽略加入固体X后溶液的体积变化)。
。(注:忽略加入固体X后溶液的体积变化)。
请回答:
((1))组成X的3种元素是___________ (填元素符号),X的化学式是___________ 。
(2)若吸收气体A的KOH不足,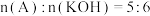 ,该反应的化学方程式是
,该反应的化学方程式是___________ 。
(3)固体X与稀盐酸发生反应的离子方程式是___________ 。
Ⅱ.(4)某研究小组为讨论 (aq)与
(aq)与 (aq)的反应原理,提出了两种可能:
(aq)的反应原理,提出了两种可能:
①发生双水解反应;
②___________ 。
(5)在探究前,先进行了一个实验,选择实验用品如下: 溶液、
溶液、 稀溶液、稀盐酸、试管、胶头滴管。从选择的药品分析,设计这个实验的目的是
稀溶液、稀盐酸、试管、胶头滴管。从选择的药品分析,设计这个实验的目的是___________ 。

①A和B均为纯净物,生成的A全部逸出,且可使品红溶液褪色。
②溶液C中的溶质只含一种阴离子,进行焰色反应,发现透过蓝色钴玻片,火焰呈紫色;
③用酸性:
 标准溶液滴定用5.40gX配成的溶液,发生反应:
标准溶液滴定用5.40gX配成的溶液,发生反应: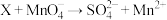 ,消耗0.032mol
,消耗0.032mol 。(注:忽略加入固体X后溶液的体积变化)。
。(注:忽略加入固体X后溶液的体积变化)。请回答:
((1))组成X的3种元素是
(2)若吸收气体A的KOH不足,
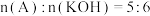 ,该反应的化学方程式是
,该反应的化学方程式是(3)固体X与稀盐酸发生反应的离子方程式是
Ⅱ.(4)某研究小组为讨论
 (aq)与
(aq)与 (aq)的反应原理,提出了两种可能:
(aq)的反应原理,提出了两种可能:①发生双水解反应;
②
(5)在探究前,先进行了一个实验,选择实验用品如下:
 溶液、
溶液、 稀溶液、稀盐酸、试管、胶头滴管。从选择的药品分析,设计这个实验的目的是
稀溶液、稀盐酸、试管、胶头滴管。从选择的药品分析,设计这个实验的目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】锂电池让移动智能生活成为可能。我省分布大量含锂云母的锂矿。锂云母主要成分为:KLi1.5Al1.5[AlSi3O10](FOH)2,还含有铷、铯等稀有金属及少量铁、镁等杂质。2019年,中国有色金属工业协会评估认为江西浩海锂能科技有限公司开发完成的“锂云母全组分利用绿色工艺及关键技术”达到了国际领先水平。以下是锂云母制备碳酸锂的一种工艺(部分流程步骤已省略):
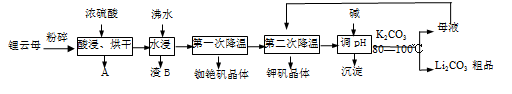
请回答下列问题:
(1)A可以用于刻蚀玻璃,则A的化学式为___________ 。25℃时,A的电离常数约为1 10-4,则1mol/LA溶液的pH=
10-4,则1mol/LA溶液的pH=___________ 。
(2)酸浸时,要使浓硫酸尽可能耗尽,其主要原因是___________ 。
(3)为了提高沸水浸出金属离子的效率,可以采取的措施有___________ 。
(4)B主要成分为___________ (填化学式),母液中用于循环利用的主要物质为___________ 。
(5)洗涤Li2CO3 粗品所选择的试剂为___
A.冰水 B.热水 C.乙醇
(6)写出生成Li2CO3 粗品的化学方程式___________ 。

请回答下列问题:
(1)A可以用于刻蚀玻璃,则A的化学式为
 10-4,则1mol/LA溶液的pH=
10-4,则1mol/LA溶液的pH=(2)酸浸时,要使浓硫酸尽可能耗尽,其主要原因是
(3)为了提高沸水浸出金属离子的效率,可以采取的措施有
(4)B主要成分为
(5)洗涤Li2CO3 粗品所选择的试剂为
A.冰水 B.热水 C.乙醇
(6)写出生成Li2CO3 粗品的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】氢能被视为21世纪最具发展潜力的清洁能源,其开发利用是科学家们研究的重要课题。试回答下列问题:
(1)与化石燃料相比,氢气作为燃料的优点是_________ (至少答出两点)。
(2)与氢气直接燃烧相比较,设计成镍氢电池可以大大提高能量的转换率,在镍氢电池充电过程中储氢合金(M)吸氢转化为MH2,总反应为:xNi(OH)2+M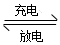 xNiOOH+MHx,试写出放电过程中负极
xNiOOH+MHx,试写出放电过程中负极
反应式____________ 。
(3)施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,已知NaBH4与水反应后所得溶液显碱性,溶液中各离子浓度大小关系为__________ ,用离子方程式表示出溶液显碱性的原因_______________ 。
(4)在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中,分别放入ag的储氢合金(M)和bmol氢气发生如下反应:2M(s)+xH2(g) 2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是
2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___________ ,当三个容器反应都达到化学平衡时,H2转化率最大的反应温度是______ 。

(5)储氢还可以借助有机物,如利用乙苯与苯乙烯之间的可逆反应来实现脱氢和加氢;
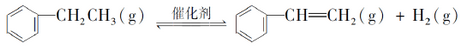
①在恒容密闭容器中,控制不同温度进行乙苯的脱氢实验。以乙苯起始浓度均为c mol/L测定乙苯的转化率,结果如图2所示。图中A为乙苯的平衡转化率与温度关系曲线,B曲线表示不同温度下反应经过相同时间且为达到化学平衡时乙苯的转化率。试说明随温度的升高,曲线B向曲线A逼近的原因__________ 。
②维持体系总压恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢。已知乙苯的平衡转换率为a,则在该温度下反应的平衡常数K=__________ (用a等符号表示)。
(1)与化石燃料相比,氢气作为燃料的优点是
(2)与氢气直接燃烧相比较,设计成镍氢电池可以大大提高能量的转换率,在镍氢电池充电过程中储氢合金(M)吸氢转化为MH2,总反应为:xNi(OH)2+M
 xNiOOH+MHx,试写出放电过程中负极
xNiOOH+MHx,试写出放电过程中负极反应式
(3)施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,已知NaBH4与水反应后所得溶液显碱性,溶液中各离子浓度大小关系为
(4)在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中,分别放入ag的储氢合金(M)和bmol氢气发生如下反应:2M(s)+xH2(g)
 2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是
2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是
(5)储氢还可以借助有机物,如利用乙苯与苯乙烯之间的可逆反应来实现脱氢和加氢;

①在恒容密闭容器中,控制不同温度进行乙苯的脱氢实验。以乙苯起始浓度均为c mol/L测定乙苯的转化率,结果如图2所示。图中A为乙苯的平衡转化率与温度关系曲线,B曲线表示不同温度下反应经过相同时间且为达到化学平衡时乙苯的转化率。试说明随温度的升高,曲线B向曲线A逼近的原因
②维持体系总压恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢。已知乙苯的平衡转换率为a,则在该温度下反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】 循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
(1) 催化加氢。在密闭容器中,向含有催化剂的
催化加氢。在密闭容器中,向含有催化剂的 溶液(
溶液( 与KOH溶液反应制得)中通入
与KOH溶液反应制得)中通入 生成
生成 。其他条件不变,
。其他条件不变, 转化为
转化为 的转化率随温度的变化如图所示。反应温度在。40℃~80℃范围内,
的转化率随温度的变化如图所示。反应温度在。40℃~80℃范围内, 催化加氢的转化率迅速上升,其原因可能是
催化加氢的转化率迅速上升,其原因可能是___________ 。

(2)HCOOH燃料电池。研究HCOOH燃料电池性能的装置如图所示,两电极区间用允许 、
、 通过的半透膜隔开。
通过的半透膜隔开。
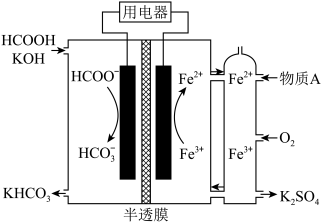
①电池负极电极反应式为___________ :过程中需补充的物质A为___________ (填化学式)。
②每得到1 mol ,理论消耗标准状况下
,理论消耗标准状况下 的体积为
的体积为___________ L。
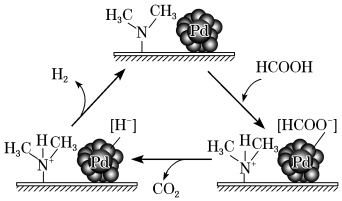
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成 和
和 可能的反应机理如图所示。根据机理,HCOOD催化释氢反应除生成
可能的反应机理如图所示。根据机理,HCOOD催化释氢反应除生成 外,还生成
外,还生成___________ (填化学式)。
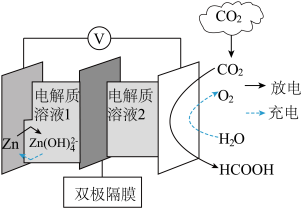
(4)科学家近年发明了一种新型 水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体
水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体 被转化为储氢物质甲酸等。为解决环境和能源问题提供了一种新途径。
被转化为储氢物质甲酸等。为解决环境和能源问题提供了一种新途径。
①放电时,负极溶液pH___________ 。(填“减小”“增大”或“不变”)
②充电时,电池总反应为___________ 。
 循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
循环在氢能的贮存/释放、燃料电池等方面具有重要应用。(1)
 催化加氢。在密闭容器中,向含有催化剂的
催化加氢。在密闭容器中,向含有催化剂的 溶液(
溶液( 与KOH溶液反应制得)中通入
与KOH溶液反应制得)中通入 生成
生成 。其他条件不变,
。其他条件不变, 转化为
转化为 的转化率随温度的变化如图所示。反应温度在。40℃~80℃范围内,
的转化率随温度的变化如图所示。反应温度在。40℃~80℃范围内, 催化加氢的转化率迅速上升,其原因可能是
催化加氢的转化率迅速上升,其原因可能是
(2)HCOOH燃料电池。研究HCOOH燃料电池性能的装置如图所示,两电极区间用允许
 、
、 通过的半透膜隔开。
通过的半透膜隔开。
①电池负极电极反应式为
②每得到1 mol
 ,理论消耗标准状况下
,理论消耗标准状况下 的体积为
的体积为(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成
 和
和 可能的反应机理如图所示。根据机理,HCOOD催化释氢反应除生成
可能的反应机理如图所示。根据机理,HCOOD催化释氢反应除生成 外,还生成
外,还生成
(4)科学家近年发明了一种新型
 水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体
水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体 被转化为储氢物质甲酸等。为解决环境和能源问题提供了一种新途径。
被转化为储氢物质甲酸等。为解决环境和能源问题提供了一种新途径。①放电时,负极溶液pH
②充电时,电池总反应为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】硫酸铅广泛应用于制造铅蓄电池、白色颜料以及精细化工产品3PbO·PbSO4·H2O(三盐)等。工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)制备PbSO4的工艺流程如下:
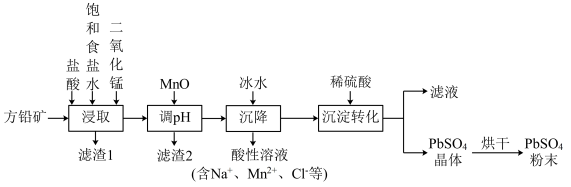
已知:①PbCl2难溶于冷水,易溶于热水。
②PbCl2(s)+2Cl-(aq) PbCl
PbCl (aq) △H>0
(aq) △H>0
③Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5
(1)“浸取”时需要加热,此时盐酸与MnO2、PbS以及NaCl发生反应生成Na2PbCl4、S等物质,反应的化学方程式为___________ ;该步骤中FeS2和MnO2颗粒可以组成两个原电池,如图所示:
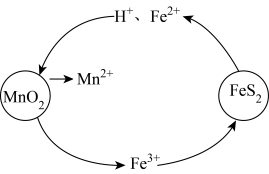
其中,MnO2原电池反应迅速,而FeS2原电池由于生成的硫覆盖在FeS2颗粒表面,溶解速率变慢。
①MnO2原电池中,每消耗3 mol MnO2,生成___________ mol Fe3+。
②FeS2原电池负极上的电极反应式为___________ 。
(2)“滤渣2”的主要成分是___________ 。
(3)“沉降”操作时加入冰水的目的是___________ 。
(4)上述流程中可循环利用的物质是___________ (填名称)。
(5)PbCl2经“沉淀转化”后得到PbSO4,若用1 L硫酸溶液转化10 mol的PbCl2,则硫酸溶液的最初浓度不得低于___________ 。
(6)用硫酸铅与氢氧化钠溶液在50℃-60℃反应可以制备三盐,该反应的离子方程式为___________ 。

已知:①PbCl2难溶于冷水,易溶于热水。
②PbCl2(s)+2Cl-(aq)
 PbCl
PbCl (aq) △H>0
(aq) △H>0③Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5
(1)“浸取”时需要加热,此时盐酸与MnO2、PbS以及NaCl发生反应生成Na2PbCl4、S等物质,反应的化学方程式为

其中,MnO2原电池反应迅速,而FeS2原电池由于生成的硫覆盖在FeS2颗粒表面,溶解速率变慢。
①MnO2原电池中,每消耗3 mol MnO2,生成
②FeS2原电池负极上的电极反应式为
(2)“滤渣2”的主要成分是
(3)“沉降”操作时加入冰水的目的是
(4)上述流程中可循环利用的物质是
(5)PbCl2经“沉淀转化”后得到PbSO4,若用1 L硫酸溶液转化10 mol的PbCl2,则硫酸溶液的最初浓度不得低于
(6)用硫酸铅与氢氧化钠溶液在50℃-60℃反应可以制备三盐,该反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】生命体中,各种物质的结构和功能都与基础化学密切相关。磷脂和蛋白质就是其中的重要代表。
(1)磷脂双层膜是由两亲性的磷脂分子以“尾部朝里,头朝外”的方式组成的双层膜结构,它起到对细胞进行包裹保护以及对物质进行选择性传递的作用。构成该双层膜结构的磷脂分子和磷脂双层膜结构的示意图以及其相关的脂质体如图所示。
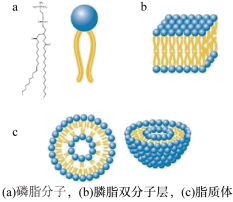
①依据磷脂双层膜结构的特征,解释为什么水溶液中的离子无法自由通过磷脂双层膜_____ 。
②细胞膜是由磷脂双层膜组成,由于细胞内外离子浓度分布的不均匀性,造成了膜两边形成了一定的电势差,被称为膜电位。由离子An+浓差形成的膜电位(定义细胞外的电势为零)可以通过如下方程计算:
神经元细胞内和细胞外的钠离子和钾离子浓度分别为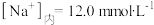 ,
,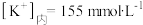 ,。
,。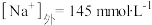 ,
, ,计算37.0°C下此种细胞的膜电位(注明正负)
,计算37.0°C下此种细胞的膜电位(注明正负)_____ 。
③在水溶液中,磷脂双层膜会自发卷曲成球形,该结构被称为脂质体,其结构如7-1中之图所示。通过测量脂质体在不同粘度溶液中自由扩散运动的扩散系数(D),可以计算得到其粒径。自由扩散运动符合布朗运动规律,遵循Stokes-Einstein方程,有d=kB77(3πηD),其中d为脂质体直径,η是溶液粘度(单位为cp, )。20.0℃下测得某脂质体在不同粘度溶液中的扩散系数如表所示,计算其直径(忽咯磷脂双层膜厚度)
)。20.0℃下测得某脂质体在不同粘度溶液中的扩散系数如表所示,计算其直径(忽咯磷脂双层膜厚度)_____ 。
某脂质体在不同粘度溶液中的扩散速率
④称取725.6mg磷脂分子(式盘786.1),制备成1.000mL脂质体水溶液。取10.00μL该溶液,测得其中含有1.12×10l4个脂质体颗粒。直径为100nm。假设所有磷脂分子都形成了脂质体,计算脂质体外表面磷脂分子的排布密度(单位:个·m-2)_____ 。
(2)某蛋白质可发生可逆的二聚化反应,2M(单体)=D(二聚体)。pH=7.5时,测得该二聚化反应在15°C,30°C,40°C下的平衡常数均为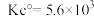 。假设二聚反应的焓变与熵变均与温度无关。
。假设二聚反应的焓变与熵变均与温度无关。
①计算在pH=7.5和体温37.0°C下二聚反应的标准摩尔焓变(单位:kJ·mo1-1)与熵变(单位:K·mol-1)_____ 。
②指明反应是焓驱动反应还是熵驱动反应,解释上述二聚反应熵变化的原因_____ 。
有机部分缩写:
Ac:乙酰基r。Bn:苄基(苯甲基):Bu:丁基;Cy:环已基;equiv:当量;Et:乙基;Me:甲基;OTf:三氟甲磺酰基;Ph:苯基;。R:烷基;TBS:tBuMeySi-;THF:四氢呋喃;TMS:三甲基硅基;Ts:对甲苯磺酰基。
(1)磷脂双层膜是由两亲性的磷脂分子以“尾部朝里,头朝外”的方式组成的双层膜结构,它起到对细胞进行包裹保护以及对物质进行选择性传递的作用。构成该双层膜结构的磷脂分子和磷脂双层膜结构的示意图以及其相关的脂质体如图所示。

①依据磷脂双层膜结构的特征,解释为什么水溶液中的离子无法自由通过磷脂双层膜
②细胞膜是由磷脂双层膜组成,由于细胞内外离子浓度分布的不均匀性,造成了膜两边形成了一定的电势差,被称为膜电位。由离子An+浓差形成的膜电位(定义细胞外的电势为零)可以通过如下方程计算:

神经元细胞内和细胞外的钠离子和钾离子浓度分别为
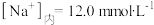 ,
,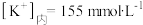 ,。
,。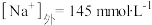 ,
, ,计算37.0°C下此种细胞的膜电位(注明正负)
,计算37.0°C下此种细胞的膜电位(注明正负)③在水溶液中,磷脂双层膜会自发卷曲成球形,该结构被称为脂质体,其结构如7-1中之图所示。通过测量脂质体在不同粘度溶液中自由扩散运动的扩散系数(D),可以计算得到其粒径。自由扩散运动符合布朗运动规律,遵循Stokes-Einstein方程,有d=kB77(3πηD),其中d为脂质体直径,η是溶液粘度(单位为cp,
 )。20.0℃下测得某脂质体在不同粘度溶液中的扩散系数如表所示,计算其直径(忽咯磷脂双层膜厚度)
)。20.0℃下测得某脂质体在不同粘度溶液中的扩散系数如表所示,计算其直径(忽咯磷脂双层膜厚度)某脂质体在不同粘度溶液中的扩散速率
| D(μm2·s-1) | η(cp) |
| 0.389 | 7.18 |
| 0.281 | 9.85 |
| 0.188 | 14.1 |
| 0.146 | 20.8 |
| 0.091 | 33.5 |
(2)某蛋白质可发生可逆的二聚化反应,2M(单体)=D(二聚体)。pH=7.5时,测得该二聚化反应在15°C,30°C,40°C下的平衡常数均为
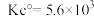 。假设二聚反应的焓变与熵变均与温度无关。
。假设二聚反应的焓变与熵变均与温度无关。①计算在pH=7.5和体温37.0°C下二聚反应的标准摩尔焓变(单位:kJ·mo1-1)与熵变(单位:K·mol-1)
②指明反应是焓驱动反应还是熵驱动反应,解释上述二聚反应熵变化的原因
有机部分缩写:
Ac:乙酰基r。Bn:苄基(苯甲基):Bu:丁基;Cy:环已基;equiv:当量;Et:乙基;Me:甲基;OTf:三氟甲磺酰基;Ph:苯基;。R:烷基;TBS:tBuMeySi-;THF:四氢呋喃;TMS:三甲基硅基;Ts:对甲苯磺酰基。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】(1)下列玻璃仪器的洗涤方法不涉及氧化还原反应的是_____
A.附有银镜的试管用稀硝酸清洗
B.附有油脂的烧杯用热纯碱溶液清洗
C.附有MnO2的烧瓶用热的浓盐酸清洗
D.附有硫的燃烧匙用热的烧碱溶液清洗
(2)室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
下列说法正确的是_____
A.试管I中浅棕色气体为NO2,由硝酸还原生成
B.等量的Cu完全溶解时,I中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管II中反应更剧烈
D.试管II中反应后溶液颜色与试管I中的不同,是由于溶有NO2
(3)溶液的导电性与溶液中的离子的种类和浓度有关,下列各组实验过程的被滴加溶液导电性变化与如图对应的是_____
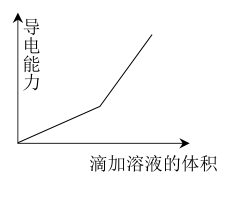
A.向Ba(OH)2溶液中滴加H2SO4溶液
B.向醋酸溶液中滴加NaOH溶液
C.向糖水中滴加NaCl溶液。
D.向盐酸中滴加氨水
(4)卤化钠(NaX)和四卤化钛(TiX4) 的熔点如图所示。下列判断不正确的是_____
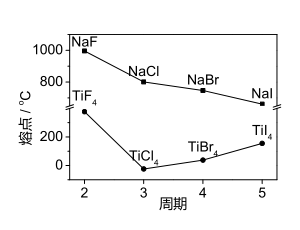
A. TiF4 的熔点反常升高是由于氢键的作用
B. NaX随X-半径增大,离子键减弱。
C. NaX均为离子化合物
D. TiCl4 为共价化合物
(5)如图所示,钠-氯化镍电池是以β-Al2O3(Al2O3· xNa2O)作为固体电解质构成的一种新型高能电池(2Na + NiCl2 Ni+2NaCl),下列关于该电池的叙述错误的是
Ni+2NaCl),下列关于该电池的叙述错误的是_____
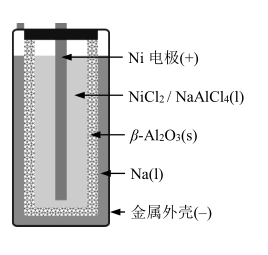
A.放电时NaCl在熔融电解质中生成
B.充电时阴极反应: Na++e-= Na 。
C.氯离子通过β-Al2O3 (s)在两电极间移动
D.如果电池过度放电,AlCl 可能被还原
可能被还原
(6)最近我国科学家预测并据此合成了新型碳材料: T-碳。可以看做金刚石结构中的一个碳原子被四个碳原子构成一个正四面体结构单元替代(如下图所示,所有小球都代表碳原子)。下列说法正确的是_____

A.T-碳与石墨、金刚石互为同素异形体
B.T-碳晶体与金刚石晶体类似,属于原子晶体。
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子都采取杂化方式不同
A.附有银镜的试管用稀硝酸清洗
B.附有油脂的烧杯用热纯碱溶液清洗
C.附有MnO2的烧瓶用热的浓盐酸清洗
D.附有硫的燃烧匙用热的烧碱溶液清洗
(2)室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
| 实验 | 现象 |
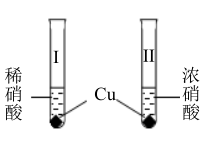 | 试管I中开始无明显现象,逐渐有微小气泡生成,越来越剧烈,液面上方出现浅棕色气体,溶液呈蓝色。 |
| 试管II中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色;之后向绿色溶液中持续通入N2,溶液变为蓝色。 |
下列说法正确的是
A.试管I中浅棕色气体为NO2,由硝酸还原生成
B.等量的Cu完全溶解时,I中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管II中反应更剧烈
D.试管II中反应后溶液颜色与试管I中的不同,是由于溶有NO2
(3)溶液的导电性与溶液中的离子的种类和浓度有关,下列各组实验过程的被滴加溶液导电性变化与如图对应的是

A.向Ba(OH)2溶液中滴加H2SO4溶液
B.向醋酸溶液中滴加NaOH溶液
C.向糖水中滴加NaCl溶液。
D.向盐酸中滴加氨水
(4)卤化钠(NaX)和四卤化钛(TiX4) 的熔点如图所示。下列判断不正确的是

A. TiF4 的熔点反常升高是由于氢键的作用
B. NaX随X-半径增大,离子键减弱。
C. NaX均为离子化合物
D. TiCl4 为共价化合物
(5)如图所示,钠-氯化镍电池是以β-Al2O3(Al2O3· xNa2O)作为固体电解质构成的一种新型高能电池(2Na + NiCl2
 Ni+2NaCl),下列关于该电池的叙述错误的是
Ni+2NaCl),下列关于该电池的叙述错误的是
A.放电时NaCl在熔融电解质中生成
B.充电时阴极反应: Na++e-= Na 。
C.氯离子通过β-Al2O3 (s)在两电极间移动
D.如果电池过度放电,AlCl
 可能被还原
可能被还原(6)最近我国科学家预测并据此合成了新型碳材料: T-碳。可以看做金刚石结构中的一个碳原子被四个碳原子构成一个正四面体结构单元替代(如下图所示,所有小球都代表碳原子)。下列说法正确的是

A.T-碳与石墨、金刚石互为同素异形体
B.T-碳晶体与金刚石晶体类似,属于原子晶体。
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子都采取杂化方式不同
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】太阳能发电和阳光分解水制氢,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面。下图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带(未充填电子的分子轨道构成的能级最低的能带)与价带(已充填价电子的分子轨道构成的能级最高的能带)之间的能量差△E(=Ec-Ev)称为带隙,图中的e-为电子、h+为空穴。
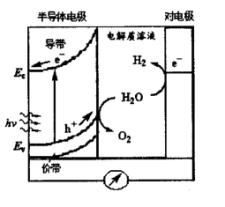
瑞士科学家最近发明了一种基于上图所示原理的廉价光电化学电池装置,其半导体电极由2个光系统串联而成。系统一由吸收蓝色光的WO3纳米晶薄膜构成;系统二吸收绿色和红色光,由染料敏化的TiO2纳米晶薄膜构成。在光照下,系统一的电子(e-)由价带跃迁到导带后,转移到系统二的价带,再跃迁到系统二的导带,然后流向对电极。所采用的光敏染料为配合物RuL2(SCN)2,其中中性配体L为4,4’-二羧基-2,2’-联吡啶。
(1)指出配合物RuL2(SCN)2中配体L的配位原子和中心金属原子的配位数_______ 、______ 。
(2)推测该配合物的分子结构________ ,并用 Z代表L(其中Z为配位原子),画出该配合物及其几何异构体的几何结构示意图
Z代表L(其中Z为配位原子),画出该配合物及其几何异构体的几何结构示意图_______ 。
(3)画出该配合物有旋光活性的键合异构体______ 。
(4)分别写出半导体电极表面和对电极表面发生的电极反应式以及总反应式___ 、___ 、___ 。
(5)已知太阳光能量密度最大的波长在560nm附近,说明半导体电极中TiO2纳米晶膜(白色)必须添加光敏剂的原因____ 。
(6)说明TiO2和配合物RuL2(SCN)2对可见光的吸收情况_____ ,推测该配合物的颜色______ 。
(7)该光电化学电池装置所得产物可用于环保型汽车发动机吗______ ?说明理由______ 。

瑞士科学家最近发明了一种基于上图所示原理的廉价光电化学电池装置,其半导体电极由2个光系统串联而成。系统一由吸收蓝色光的WO3纳米晶薄膜构成;系统二吸收绿色和红色光,由染料敏化的TiO2纳米晶薄膜构成。在光照下,系统一的电子(e-)由价带跃迁到导带后,转移到系统二的价带,再跃迁到系统二的导带,然后流向对电极。所采用的光敏染料为配合物RuL2(SCN)2,其中中性配体L为4,4’-二羧基-2,2’-联吡啶。
(1)指出配合物RuL2(SCN)2中配体L的配位原子和中心金属原子的配位数
(2)推测该配合物的分子结构
 Z代表L(其中Z为配位原子),画出该配合物及其几何异构体的几何结构示意图
Z代表L(其中Z为配位原子),画出该配合物及其几何异构体的几何结构示意图(3)画出该配合物有旋光活性的键合异构体
(4)分别写出半导体电极表面和对电极表面发生的电极反应式以及总反应式
(5)已知太阳光能量密度最大的波长在560nm附近,说明半导体电极中TiO2纳米晶膜(白色)必须添加光敏剂的原因
(6)说明TiO2和配合物RuL2(SCN)2对可见光的吸收情况
(7)该光电化学电池装置所得产物可用于环保型汽车发动机吗
您最近一年使用:0次



