光刻技术需要利用深紫激光,我国是唯一掌握通过非线性光学晶体变频来获得深紫外激光技术的国家。目前唯一实用化的晶体是氟代硼铍酸钾晶体KBBF(KBe2BO3F2),实验室可用 BeO、KBF4和B2O3在700 ℃左右灼烧获得氟代硼铍酸钾晶体(晶胞如图所示,其中 K原子已经给出,氧原子略去),并放出BF3气体。回答下列问题:
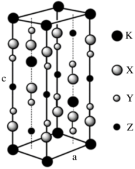
(1)基态钾原子的核外电子排布式为___________ ,能量最高的电子的电子云轮廓图形状为___________ 。
(2)BF3的空间构型为___________ ,与其互为等电子体的阴离子为___________ (填一种即可)。
(3)指出图中代表硼原子的字母为___________ ,该KBBF晶体的晶胞参数分别为a pm和c pm,α=β=γ=90°,则晶体密度为___________ g·cm-3(M代表 KBBF 的摩尔质量,NA表示阿伏加德罗常数的值,列出计算式)。

(1)基态钾原子的核外电子排布式为
(2)BF3的空间构型为
(3)指出图中代表硼原子的字母为
2021高三·全国·专题练习 查看更多[1]
(已下线)第十二章能力提升检测卷(精练)-2022年一轮复习讲练测
更新时间:2021-08-17 16:44:23
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Z、Q、R、T为前四周期元素,且原子序数依次增大。X和Q属同族元素,X和R可形成化合物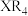 ;
; 为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;
为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;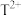 的3d轨道中有5个电子。请回答下列问题。
的3d轨道中有5个电子。请回答下列问题。
(1)Z基态原子的电子排布式是___________ ;
(2)利用价层电子对互斥模型判断 的空间结构是
的空间结构是___________ ;
(3)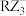 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为___________ 。
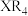 ;
; 为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;
为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;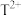 的3d轨道中有5个电子。请回答下列问题。
的3d轨道中有5个电子。请回答下列问题。(1)Z基态原子的电子排布式是
(2)利用价层电子对互斥模型判断
 的空间结构是
的空间结构是(3)
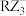 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为
您最近一年使用:0次
【推荐2】最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行(面心)立方最密堆积(ccp),它们的排列有序,没有相互代换的现象(即没有平均原子或统计原子),它们构成两种八面体空隙(由6个球体所围成的空隙。6个球体中心的连线连接成八面体形状),一种由镍原子构成,另一种由镍原子和镁原子一起构成,两种八面体的数量比是1︰3,碳原子只填充在镍原子构成的八面体空隙中。
(1)镍的外围电子排布式为________________ 。
(2)画出该新型超导材料的一个晶胞。(镁原子处于晶胞的顶点。碳原子用▲球,镍原子用○球表示)_______ 。

(3)写出该新型超导材料的化学式_____________ 。
(4)镍原子的配位数是_____________ 。
(5)原子坐标参数表示晶胞内部各原子的相对位置,用(0,0,0)表示镁原子的原子坐标,晶胞边长设为1,则碳原子的原子坐标参数为_____________ 。
(6)已知晶胞边长为a pm,则该化合物的密度为________ g·cm-3(只要求列出算式,阿伏伽德罗常数的数值为NA)。
(1)镍的外围电子排布式为
(2)画出该新型超导材料的一个晶胞。(镁原子处于晶胞的顶点。碳原子用▲球,镍原子用○球表示)

(3)写出该新型超导材料的化学式
(4)镍原子的配位数是
(5)原子坐标参数表示晶胞内部各原子的相对位置,用(0,0,0)表示镁原子的原子坐标,晶胞边长设为1,则碳原子的原子坐标参数为
(6)已知晶胞边长为a pm,则该化合物的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为_______ 。
(2)H2SeO3的中心原子杂化类型是:_______ ,  的立体构型是
的立体构型是_______ 。与 互为等电子体的分子有
互为等电子体的分子有_______ (写一种物质的化学式即可)。
(3)H2Se属于_______ (填“极性”或“非极性”)分子;比较H2Se与H2O沸点高低,并说明原因:_______ 。
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_______ ;若该晶胞密度为ρg·cm-3,硒化锌的摩尔质量为Mg·mol-1,NA代表阿伏加德罗常数的值,则晶胞参数a为_______ 。

(1)基态硒原子的价层电子排布式为
(2)H2SeO3的中心原子杂化类型是:
 的立体构型是
的立体构型是 互为等电子体的分子有
互为等电子体的分子有(3)H2Se属于
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】明代宋应星所著《天工开物》中已经记载了我国古代用炉甘石(主要成分ZnCO3)和煤冶锌工艺,锌的主要用途是制造锌合金和作为其他金属的保护层。回答下列问题:
(1)Zn原子基态核外电子排布式为_____________________________ 。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①与SO42-互为等电子体的阴离子化学式为________________ (写出一种)
②氨的热稳定性强于膦(PH3),原因是____________________________ 。
(3)黄铜是由铜和锌所组成的合金,元素铜与锌的第一电离能分别为ICu=746 kJ·mol-1,IZn=906 kJ·mol-1,ICu< IZn的原因是___________________ 。
(4)《本草纲目》中记载炉甘石(主要成分ZnCO3)可止血,消肿毒,生肌,明目……。Zn、C、O电负性由大至小的顺序是_________________ 。ZnCO3中阴离子的立体构型是_____________________ 。
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶胞结构如图所示,每个Zn原子周围最近的Zn原子数目为________________ 。晶胞边长为apm,阿伏伽德罗常数的值为NA,则ZnS晶体的密度为 __________ g·cm-3(列出计算式即可)。

(1)Zn原子基态核外电子排布式为
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①与SO42-互为等电子体的阴离子化学式为
②氨的热稳定性强于膦(PH3),原因是
(3)黄铜是由铜和锌所组成的合金,元素铜与锌的第一电离能分别为ICu=746 kJ·mol-1,IZn=906 kJ·mol-1,ICu< IZn的原因是
(4)《本草纲目》中记载炉甘石(主要成分ZnCO3)可止血,消肿毒,生肌,明目……。Zn、C、O电负性由大至小的顺序是
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶胞结构如图所示,每个Zn原子周围最近的Zn原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】原子结构与元素周期表、元素性质三者关系密切。
A、B、D、E、F为原子序数依次增大的前四周期元素,其中A的最外层电子数是其内层电子数的2倍,B、D、E为同周期元素,B原子的核外电子总数是其未成对电子数的5倍,E原子最外层有1个未成对电子,F原子核外有22种运动状态的电子。
请回答下列问题:
(1)F元素位于周期表_____________ 区,其价电子排布图为:_____________ 。
(2)B、D、E三种元素中,第一电离能最小的是_____________ (填元素符号);写出AD2的等电子体_____________ (分子和阴离子各写一种)。
(3)AO2和DO2熔点高的是_____________ ,原因是_____________ 。
A、B、D、E、F为原子序数依次增大的前四周期元素,其中A的最外层电子数是其内层电子数的2倍,B、D、E为同周期元素,B原子的核外电子总数是其未成对电子数的5倍,E原子最外层有1个未成对电子,F原子核外有22种运动状态的电子。
请回答下列问题:
(1)F元素位于周期表
(2)B、D、E三种元素中,第一电离能最小的是
(3)AO2和DO2熔点高的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】青蒿素(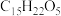 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
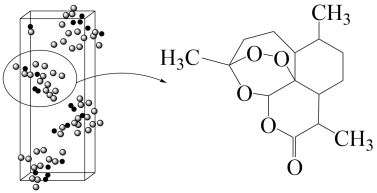
(1)提取青蒿素
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙谜( )提取,效果更好。
)提取,效果更好。
①乙醚沸点低于乙醇,原因是_______ 。
②用乙醚提取效果更好,原因是_______ 。
(2)确定结构
①比较青蒿素分子中C、H、O的电负性大小:_______ 。
②图中晶胞的棱长分别为 ,晶体的密度为
,晶体的密度为_______  。(用
。(用 表示阿伏加德罗常数;青蒿素的相对分子质量为282)
表示阿伏加德罗常数;青蒿素的相对分子质量为282)
③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是_______ 。
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
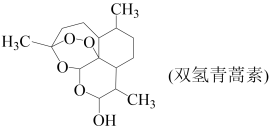
①双氢青蒿素分子中碳原子的杂化方式为_______ 。
② 的空间结构为
的空间结构为_______ 。
双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
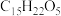 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
(1)提取青蒿素
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙谜(
 )提取,效果更好。
)提取,效果更好。①乙醚沸点低于乙醇,原因是
②用乙醚提取效果更好,原因是
(2)确定结构
①比较青蒿素分子中C、H、O的电负性大小:
②图中晶胞的棱长分别为
 ,晶体的密度为
,晶体的密度为 。(用
。(用 表示阿伏加德罗常数;青蒿素的相对分子质量为282)
表示阿伏加德罗常数;青蒿素的相对分子质量为282)③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用
 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
①双氢青蒿素分子中碳原子的杂化方式为
②
 的空间结构为
的空间结构为双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
您最近一年使用:0次
【推荐2】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题。
(1)X元素原子基态时的电子排布式为___________________ ,该元素的符号是_____ 。
(2)Y元素原子的价层电子的轨道表示式为_______________ ,该元素的名称是_____ 。
(3)X与Z可形成化合物XZ3,该化合物的空间构型为____________________ 。
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是______________________________________________________ 。
(5)碳正离子[例如,CH3+,CH5+,(CH3)3C+等]是有机反应中重要的中间体。欧拉(G.Olah)因在此领域研究中的卓越成就而荣获1994年诺贝尔化学奖。碳正离子CH5+可以通过CH4在“超强酸”中再获得一个H+而得到,而CH5+失去H2可得CH3+。
①CH3+ 是反应性很强的正离子,是缺电子的,其电子式是_________ 。
②CH3+ 中4个原子是共平面的,三个键角相等,键角应是_________ (填角度)。
③(CH3)2CH+在NaOH的水溶液中反应将得到电中性的有机分子,其结构简式是_________ 。
④(CH3)3C+ 去掉H+ 后将生成电中性的有机分子,其结构简式是_________ 。
(1)X元素原子基态时的电子排布式为
(2)Y元素原子的价层电子的轨道表示式为
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
(5)碳正离子[例如,CH3+,CH5+,(CH3)3C+等]是有机反应中重要的中间体。欧拉(G.Olah)因在此领域研究中的卓越成就而荣获1994年诺贝尔化学奖。碳正离子CH5+可以通过CH4在“超强酸”中再获得一个H+而得到,而CH5+失去H2可得CH3+。
①CH3+ 是反应性很强的正离子,是缺电子的,其电子式是
②CH3+ 中4个原子是共平面的,三个键角相等,键角应是
③(CH3)2CH+在NaOH的水溶液中反应将得到电中性的有机分子,其结构简式是
④(CH3)3C+ 去掉H+ 后将生成电中性的有机分子,其结构简式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】已知A、B、C、D、E都是周期表中前四周期的元素,它们的原子序数依次增大。其中A元素原子的核外p电子数比s电子数少1。C是电负性最大的元素。D原子次外层电子数是最外层电子数2倍,E是第Ⅷ族中原子序数最小的元素。
(1)写出基态C原子的电子排布式_________________ 。
(2)A、B、C三种元素的第一电离能由大到小的顺序为______________ (用元素符号表示),原因是___________________ 。
(3)已知DC4常温下为气体,则该物质的晶体类型是_________ ,组成微粒的中心原子的轨道杂化类型为____________ ,空间构型是___________ 。
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但AC3不易与Cu2+形成配离子,其原因是______________________ 。
(5)A、B两元素分别与D形成的共价键中,极性较强的是__________ 。A、B两元素间能形成多种二元化合物,其中与A3—互为等电子体的物质的化学式为__________ 。
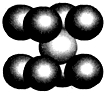
(6)已知E单质的晶胞如图所示,则晶体中E原子的配位数为__________ ,一个E的晶胞质量为___________ 。
(1)写出基态C原子的电子排布式
(2)A、B、C三种元素的第一电离能由大到小的顺序为
(3)已知DC4常温下为气体,则该物质的晶体类型是
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但AC3不易与Cu2+形成配离子,其原因是
(5)A、B两元素分别与D形成的共价键中,极性较强的是
(6)已知E单质的晶胞如图所示,则晶体中E原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】氮元素在农药生产及工业、制造业等领域用途非常广泛。请根据提示回答下列问题∶
(1)N原子的最外层电子排布式为___ ,在第二周期元素中,第一电离能大于N的元素有___ 种。
(2)NH3是重要的配体,如[Cu(NH3)4]2+,NH3分子的VSEPR模型为____ ,其中H—N—H的键角为107.3°,则[Cu(NH3)4]2+中H—N—H的键角___ 107.3°(填“大于”“小于”“等于”)。
(3)甲基胺离子(CH3NH )的电子式为
)的电子式为_____ ,其中存在的共价键类型为____ (填极性键、非极性键、配位键)。已知(CH3)2NH比NH3接收质子的能力强,可能的原因是____ 。
(4)2-甲基吡啶(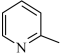 )是类似于苯的芳香化合物,分子中N原子的杂化类型为
)是类似于苯的芳香化合物,分子中N原子的杂化类型为___ 。1mol该物质中含有的σ键数目为____ 。
(5)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示

①晶胞的棱长为apm,则该晶体的密度为___ g/cm3(写出数学表达式,设NA为阿伏加德罗常数的值)。
②请画出该立方晶胞沿体对角线方向的投影图___ 。
(1)N原子的最外层电子排布式为
(2)NH3是重要的配体,如[Cu(NH3)4]2+,NH3分子的VSEPR模型为
(3)甲基胺离子(CH3NH
 )的电子式为
)的电子式为(4)2-甲基吡啶(
 )是类似于苯的芳香化合物,分子中N原子的杂化类型为
)是类似于苯的芳香化合物,分子中N原子的杂化类型为(5)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示

①晶胞的棱长为apm,则该晶体的密度为
②请画出该立方晶胞沿体对角线方向的投影图
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】原子模型塔(如图1所示)由9个大圆球组成,若每个圆球代表一个铁原子,则可以构成一个铁原子晶胞模型。


回答下列问题:
(1)基态Fe原子核外电子排布式为___________ ,核外电子占据的最高能层符号是___________ 。
(2)铁的化合物在生产生活及科学研究方面应用非常广泛。
①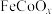 是一种新型光电催化剂,第四电离能大小关系是
是一种新型光电催化剂,第四电离能大小关系是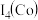
___________ 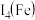 (填“>”或“<”),原因是
(填“>”或“<”),原因是___________ 。
②由环戊二烯负离子( )与Fe(Ⅱ)形成的二茂铁
)与Fe(Ⅱ)形成的二茂铁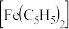 结构如图2所示。已知
结构如图2所示。已知 与苯结构相似,所有碳原子处于同一平面上。二茂铁中存在的作用力有
与苯结构相似,所有碳原子处于同一平面上。二茂铁中存在的作用力有___________ (填标号)
A.金属键 B.σ键 C.π键 D.氢键
③纳米氧化铁能催化火箭推进剂 的分解,
的分解, 的结构式为
的结构式为___________ (标出配位键),空间构型为___________ ;与 互为等电子体的粒子有
互为等电子体的粒子有___________ (任写一种)。
(3)铁的一种晶胞如图3所示,其堆积方式为___________ ,铁原子的配位数为___________ ,若铁原子的半径为a pm,则该铁晶体的密度=___________  (用
(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。



回答下列问题:
(1)基态Fe原子核外电子排布式为
(2)铁的化合物在生产生活及科学研究方面应用非常广泛。
①
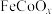 是一种新型光电催化剂,第四电离能大小关系是
是一种新型光电催化剂,第四电离能大小关系是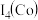
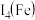 (填“>”或“<”),原因是
(填“>”或“<”),原因是②由环戊二烯负离子(
 )与Fe(Ⅱ)形成的二茂铁
)与Fe(Ⅱ)形成的二茂铁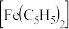 结构如图2所示。已知
结构如图2所示。已知 与苯结构相似,所有碳原子处于同一平面上。二茂铁中存在的作用力有
与苯结构相似,所有碳原子处于同一平面上。二茂铁中存在的作用力有A.金属键 B.σ键 C.π键 D.氢键
③纳米氧化铁能催化火箭推进剂
 的分解,
的分解, 的结构式为
的结构式为 互为等电子体的粒子有
互为等电子体的粒子有(3)铁的一种晶胞如图3所示,其堆积方式为
 (用
(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】人们发现,纸张会发生酸性腐蚀而变脆、破损,这严重威胁纸质文物的保存。经分析检验发现,酸性腐蚀主要与造纸中涂敷明矾的工艺有关,为了防止纸张的酸性腐蚀,可在纸浆中加入碳酸钙等添加剂。回答下列问题:
(1)上述涉及的物质中,原子序数最大的元素是____ (填化学符号),其位于元素周期表中的_____ 区。
(2)H、C、O素的电负性由大到小的顺序为____ (用元素符号表示)。
(3)熔融AlCl3有挥发性的二聚体,二聚体Al2C16结构式为____ ,其中Al的配位数为____ 。
(4)CaF2一种晶胞结构如图所示。

①CaF2属于____ (填“离子”或“共价”)化合物。
②F-位于Ca2+原子形成的____ (填“八面体空隙”或“四面体空隙”)。
③图中A处原子分数坐标为(0,0,0),若晶胞边长的单位为1,则B处原子分数坐标为____ 。
(5)由碳元素形成的某种晶体的晶胞结构如图所示,设阿伏加德罗常数的值为NA,晶体的密度为ρg·cm-3,则该晶胞的棱长为____ (用含NA、ρ的代数式表示)pm。

(1)上述涉及的物质中,原子序数最大的元素是
(2)H、C、O素的电负性由大到小的顺序为
(3)熔融AlCl3有挥发性的二聚体,二聚体Al2C16结构式为
(4)CaF2一种晶胞结构如图所示。

①CaF2属于
②F-位于Ca2+原子形成的
③图中A处原子分数坐标为(0,0,0),若晶胞边长的单位为1,则B处原子分数坐标为
(5)由碳元素形成的某种晶体的晶胞结构如图所示,设阿伏加德罗常数的值为NA,晶体的密度为ρg·cm-3,则该晶胞的棱长为

您最近一年使用:0次



