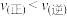下列说法错误的是
| A.向密闭容器中充入一定量的NO2气体,压缩容器(不改变其他条件),气体的颜色先变深后变浅,变深的原因可用勒夏特列原理解释 |
| B.向0.1 mol·L-1的氨水中通氨气,则NH3·H2O的电离程度减小 |
C.已知[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O,加水稀释,平衡逆移 [CuCl4]2-(黄色)+4H2O,加水稀释,平衡逆移 |
D.分别向甲容器(绝热恒容)中充入l mol PCl5,乙容器(恒温恒容)充入PCl3和Cl2各l mol,发生反应PCl5(g) PCl3(g)+Cl2(g) ∆H>0,平衡时K(甲) < K(乙) PCl3(g)+Cl2(g) ∆H>0,平衡时K(甲) < K(乙) |
21-22高三上·湖南株洲·开学考试 查看更多[5]
湖南省株洲市第二中学2022届高三上学期入学考试化学试题福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)章末培优2 专题2 化学反应速率与化学平衡-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)安徽省六安市第一中学2022届高三上学期第三次月考化学试题
更新时间:2021-09-03 09:33:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
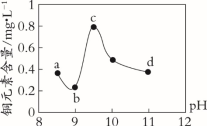
查阅资料,平衡I:Cu(OH)2 + 4NH3 [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;
平衡II:Cu(OH)2 + 2OH- [Cu(OH-)4]2-
[Cu(OH-)4]2-
下列说法不正确 的是

查阅资料,平衡I:Cu(OH)2 + 4NH3
 [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;平衡II:Cu(OH)2 + 2OH-
 [Cu(OH-)4]2-
[Cu(OH-)4]2-| 项目 | 废水水质 | 排放标准 |
| pH | 1.0 | 6~9 |
| Cu2+/ mg·L-1 | 72 | ≤0.5 |
| NH4+/ mg·L-1 | 2632 | ≤15 |
下列说法
| A.废水中Cu2+处理的最佳pH约为9 |
| B.b~c段:随pH升高,Cu(OH)2的量增加,平衡I正向移动,铜元素含量上升 |
| C.c~d段:随pH升高,c(OH-)增加,平衡I逆向移动,铜元素含量下降 |
| D.d点以后,随c(OH-)增加,铜元素含量可能上升 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】500℃时向恒容密闭容器中充入1 mol NO2(g)发生如下反应:2NO2(g)⇌N2O4(g),反应达到平衡后,向容器内再充入1 mol NO2,下列说法正确的是
| A.气体颜色最终比原平衡时还要浅 | B.平衡常数K增大 |
| C.平衡向正反应方向移动 | D.NO2的转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,在带活塞的密闭容器中,反应H2(g) +I2(g) 2HI(g)(△H〈0)达到平衡后,下列说法不正确的是
2HI(g)(△H〈0)达到平衡后,下列说法不正确的是
 2HI(g)(△H〈0)达到平衡后,下列说法不正确的是
2HI(g)(△H〈0)达到平衡后,下列说法不正确的是 | A.恒容时,升高温度,平衡向逆反应方向移动,正反应速率减小 |
| B.恒温时,减小容积平衡不移动,但气体颜色加深 |
| C.恒容时,通入H2,I2的质量分数减小 |
| D.恒压时,通入HI气体,刚开始时正反应速率会减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一化学平衡状态体系中,发生下列量的变化,其中一定会使平衡发生移动的是( )
| A.体系的压强 | B.反应物的浓度 |
| C.正、逆反应速率 | D.反应物的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】臭氧(O3)是一种很好的消毒剂,可溶于水且在水中易分解产生游离氧原子[O],[O]具有很强的杀菌消毒能力。常温常压下发生反应如下:反应①O3 O2+[O] ΔH>0平衡常数为K1;反应②O3+[O]
O2+[O] ΔH>0平衡常数为K1;反应②O3+[O] 2O2 ΔH<0 平衡常数为K2;总反应为2O3
2O2 ΔH<0 平衡常数为K2;总反应为2O3 3O2 ΔH<0 平衡常数为K;下列叙述正确的是
3O2 ΔH<0 平衡常数为K;下列叙述正确的是
 O2+[O] ΔH>0平衡常数为K1;反应②O3+[O]
O2+[O] ΔH>0平衡常数为K1;反应②O3+[O] 2O2 ΔH<0 平衡常数为K2;总反应为2O3
2O2 ΔH<0 平衡常数为K2;总反应为2O3 3O2 ΔH<0 平衡常数为K;下列叙述正确的是
3O2 ΔH<0 平衡常数为K;下列叙述正确的是| A.适当升高温度,可提高消毒效率 |
| B.K=K1+K2 |
| C.使用合适催化剂,可使O3完全转化为O2 |
| D.压强增大,K2减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】密闭容器中的反应aM(g) bN(g)+cP(g)达到平衡后,保持温度不变,将容器体积扩大到原来的两倍,达到新的平衡时,N的浓度变为原来的70%,以下判断正确的是
bN(g)+cP(g)达到平衡后,保持温度不变,将容器体积扩大到原来的两倍,达到新的平衡时,N的浓度变为原来的70%,以下判断正确的是
 bN(g)+cP(g)达到平衡后,保持温度不变,将容器体积扩大到原来的两倍,达到新的平衡时,N的浓度变为原来的70%,以下判断正确的是
bN(g)+cP(g)达到平衡后,保持温度不变,将容器体积扩大到原来的两倍,达到新的平衡时,N的浓度变为原来的70%,以下判断正确的是| A.M的转化率减小 | B.P的物质的量增多 |
| C.化学计量数:a>b+c | D.平衡向逆反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列变化不能用勒夏特列原理解释的是
| A.红棕色的NO2气体加压后颜色先变深再变浅 |
| B.打开汽水瓶,看到有大量的气泡逸出 |
| C.二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 |
| D.H2、I2、HI混合气体加压后颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在反应2SO2+O2  2SO3中,有a mol SO2和b mol O2参加反应,达到化学平衡状态时有c mol SO3生成,则SO2在平衡混合物中的体积分数为
2SO3中,有a mol SO2和b mol O2参加反应,达到化学平衡状态时有c mol SO3生成,则SO2在平衡混合物中的体积分数为
 2SO3中,有a mol SO2和b mol O2参加反应,达到化学平衡状态时有c mol SO3生成,则SO2在平衡混合物中的体积分数为
2SO3中,有a mol SO2和b mol O2参加反应,达到化学平衡状态时有c mol SO3生成,则SO2在平衡混合物中的体积分数为A.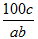 ×100% ×100% | B.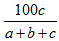 ×100% ×100% |
C.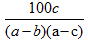 ×100% ×100% | D.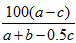 % % |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是
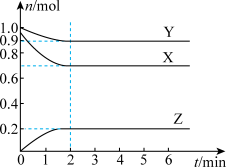

| A.平均相对分子质量不变时,该反应体系达平衡状态 |
B.该反应的化学方程式为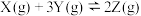 |
| C.反应达到平衡时,体系压强是反应开始时的0.9倍 |
| D.反应达到平衡时,体系中Y的物质的量分数为50% |
您最近一年使用:0次

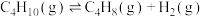
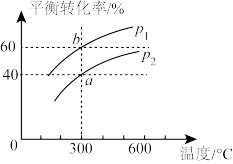
 ,反应
,反应 经一段时间后达到平衡。反应过程中测定的部分数据见下表:
经一段时间后达到平衡。反应过程中测定的部分数据见下表:

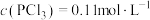 ,则反应的
,则反应的
 和0.20mol
和0.20mol ,达到平衡前
,达到平衡前