CO2储量大,是常见的温室效应气体,其综合利用意义深远。
CO2与H2制CH3OH可能发生如下反应:
(i)CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41.1kJ·mol-1
(ii)CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H2=-162kJ·mol-1
(iii)CO(g)+2H2(g)=CH3OH(g) △H3=-90.1kJ·mol-1
(iv)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H4
(1)反应(iv)自发进行的条件是:___ 。
(2)科学研究工作者研究了不同外界条件与CH3OH产率或不同产物选择性的关系,如图所示。
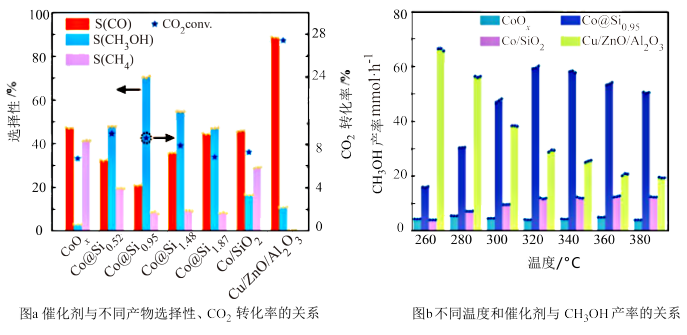
由上述可知,合适的催化剂及其适宜温度分别为___ 、___ 。
(3)以铜基催化剂催化CO2加氢制甲醇可能的反应历程存在如下步骤(*表示催化剂的活性中心,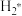 表示H2在催化剂表面的吸附态):
表示H2在催化剂表面的吸附态):
①H2(g)+*→H2*②H2*+*→2H*③CO2(g)+*→CO2*④CO2*+H*→HCO2*⑤HCO2*+H*→H2CO*+O*⑥____⑦H3CO*+H*→CH3OH*+*⑧CH3OH*→CH3OH(g)+*⑨O*+H*→OH*+*⑩OH*+H*→H2O*+*
请写出步骤⑥的化学方程式为___ 。
反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)在恒温恒压条件下进行,能证明反应达到平衡状态标志的是:
CH3OH(g)+H2O(g)在恒温恒压条件下进行,能证明反应达到平衡状态标志的是: ___ 。
A.混合气体的密度不变
B.甲醇的体积分数不变
C.相同时间内二氧化碳的消耗速率等于甲醇的生成速率
D.反应体系的温度不再变化
(4)恒温恒压下发生CO2(g)+3H2(g) CH3OH(g)+H2O(g)反应,欲增大甲醇的产量,一定可行的措施有
CH3OH(g)+H2O(g)反应,欲增大甲醇的产量,一定可行的措施有___ 。
(5)200℃时,将0.200molCO2和0.400molH2充入压强恒定为P的密闭容器中,发生CO2(g)+3H2(g) CH3OH(g)+H2O(g)反应。在催化剂作用下,CO2的最高转化率为50%,则此温度下该反应的平衡常数Kp=
CH3OH(g)+H2O(g)反应。在催化剂作用下,CO2的最高转化率为50%,则此温度下该反应的平衡常数Kp=___ 。平衡时,保持压强P恒定不变,再向体系里充入0.200molCO2和0.100mol水蒸气,反应向___ 方向进行。(选填“正反应,逆反应,保持平衡”)
CO2与H2制CH3OH可能发生如下反应:
(i)CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41.1kJ·mol-1
(ii)CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H2=-162kJ·mol-1
(iii)CO(g)+2H2(g)=CH3OH(g) △H3=-90.1kJ·mol-1
(iv)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H4
(1)反应(iv)自发进行的条件是:
| A.低温自发 | B.高温自发 |
| C.任何条件都能自发 | D.任何条件都不能自发 |

由上述可知,合适的催化剂及其适宜温度分别为
(3)以铜基催化剂催化CO2加氢制甲醇可能的反应历程存在如下步骤(*表示催化剂的活性中心,
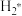 表示H2在催化剂表面的吸附态):
表示H2在催化剂表面的吸附态):①H2(g)+*→H2*②H2*+*→2H*③CO2(g)+*→CO2*④CO2*+H*→HCO2*⑤HCO2*+H*→H2CO*+O*⑥____⑦H3CO*+H*→CH3OH*+*⑧CH3OH*→CH3OH(g)+*⑨O*+H*→OH*+*⑩OH*+H*→H2O*+*
请写出步骤⑥的化学方程式为
反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)在恒温恒压条件下进行,能证明反应达到平衡状态标志的是:
CH3OH(g)+H2O(g)在恒温恒压条件下进行,能证明反应达到平衡状态标志的是: A.混合气体的密度不变
B.甲醇的体积分数不变
C.相同时间内二氧化碳的消耗速率等于甲醇的生成速率
D.反应体系的温度不再变化
(4)恒温恒压下发生CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)反应,欲增大甲醇的产量,一定可行的措施有
CH3OH(g)+H2O(g)反应,欲增大甲醇的产量,一定可行的措施有| A.向体系中通入CO2 |
| B.移走甲醇 |
| C.移走H2O(g) |
| D.与初始投料等物质的量的通入CO2、H2 |
 CH3OH(g)+H2O(g)反应。在催化剂作用下,CO2的最高转化率为50%,则此温度下该反应的平衡常数Kp=
CH3OH(g)+H2O(g)反应。在催化剂作用下,CO2的最高转化率为50%,则此温度下该反应的平衡常数Kp=
更新时间:2021-09-05 18:13:33
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
【推荐1】“2030年前实现碳达峰、2060年前实现碳中和”是中国对世界的庄严承诺,体现大国的责任和担当。
(1)CO2作为未来的重要碳源,其选择性加氢合成CH3OH一直是研究热点,在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应Ⅰ: ΔH1=-49kJ·mol-1
ΔH1=-49kJ·mol-1
反应Ⅱ: ΔH2=+41.2kJ·mol-1
ΔH2=+41.2kJ·mol-1
①反应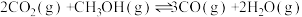 的ΔH=
的ΔH=_____ 。
②将1molCO2和3molH2混合气体以一定流速通过装有催化剂的反应器,CH3OH的选择性、H2的转化率与温度的关系如图1所示。( )
)
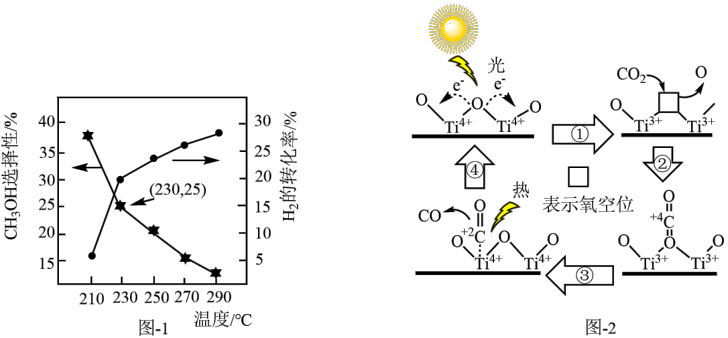
a.230℃时,测得CO2的转化率为40%,此时反应Ⅱ中消耗H2的物质的量为_____ 。
b.随着温度的升高,H2的转化率增大,其主要原因是_____ 。
(2)以TiO2为催化剂,光热化学循环分解CO2为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图2所示。根据元素电负性的变化规律,该过程可以描述为_____ 。
(3)一种脱除和利用水煤气中的CO2的方法如图3所示:
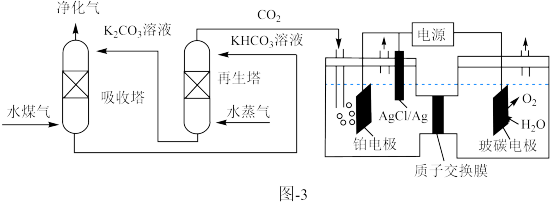
①某温度下,吸收塔中K2CO3溶液吸收一定量的CO2后,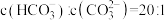 ,则该溶液的pH=
,则该溶液的pH=_____ 。(该温度下H2CO3的Ka1=4.6×10-7,Ka2=5.0×10-11)
②利用电化学原理,将CO2电催化还原为CH4,阴极上除发生AgCl转化为Ag的反应外,另一个电极反应式为_____ 。
(1)CO2作为未来的重要碳源,其选择性加氢合成CH3OH一直是研究热点,在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应Ⅰ:
 ΔH1=-49kJ·mol-1
ΔH1=-49kJ·mol-1反应Ⅱ:
 ΔH2=+41.2kJ·mol-1
ΔH2=+41.2kJ·mol-1①反应
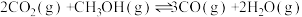 的ΔH=
的ΔH=②将1molCO2和3molH2混合气体以一定流速通过装有催化剂的反应器,CH3OH的选择性、H2的转化率与温度的关系如图1所示。(
 )
)
a.230℃时,测得CO2的转化率为40%,此时反应Ⅱ中消耗H2的物质的量为
b.随着温度的升高,H2的转化率增大,其主要原因是
(2)以TiO2为催化剂,光热化学循环分解CO2为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图2所示。根据元素电负性的变化规律,该过程可以描述为
(3)一种脱除和利用水煤气中的CO2的方法如图3所示:

①某温度下,吸收塔中K2CO3溶液吸收一定量的CO2后,
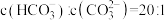 ,则该溶液的pH=
,则该溶液的pH=②利用电化学原理,将CO2电催化还原为CH4,阴极上除发生AgCl转化为Ag的反应外,另一个电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】氮氧化物的处理对建设生态文明具有重要意义,如何消除氮氧化物的污染成为当前研究的主要课题之一、回答下列问题:
(1)已知:①碳的燃烧热为 ;②
;②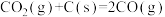
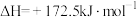 。结合图1,写出一氧化氮分解生成两种无污染气体的热化学方程式
。结合图1,写出一氧化氮分解生成两种无污染气体的热化学方程式___________ 。
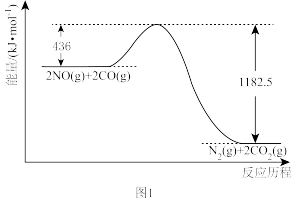
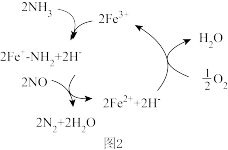
(2) 还原法。研究发现反应过程如图2,此反应过程中的催化剂为
还原法。研究发现反应过程如图2,此反应过程中的催化剂为___________ ,写出脱氮过程的总反应的化学方程式___________ 。
(3) 还原法。已知催化剂Rh表面
还原法。已知催化剂Rh表面 催化还原NO的反应机理如表,其他条件一定时,决定
催化还原NO的反应机理如表,其他条件一定时,决定 催化还原NO的反应速率的基元反应为
催化还原NO的反应速率的基元反应为___________ (填序号)。
(4) 还原法。利用甲烷可实现氮氧化物的消除,反应原理为
还原法。利用甲烷可实现氮氧化物的消除,反应原理为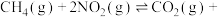
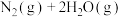
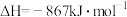 。一定温度下,在2.0L刚性密闭容器中通入1mol
。一定温度下,在2.0L刚性密闭容器中通入1mol  和2mol
和2mol  ,测得反应时间(t)与容器内气体总压强(p)的变化如表所示。
,测得反应时间(t)与容器内气体总压强(p)的变化如表所示。
达到平衡时, 的转化率为
的转化率为___________ 。若起始时加入2mol  和2mol
和2mol  ,则该温度下的压强平衡常数
,则该温度下的压强平衡常数
___________ (以分压表示,分压=总压×物质的量分数)。
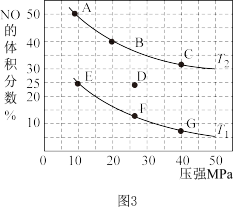
(5)CO还原法。汽车尾气(CO、NO)可转化为无毒、无害物质。在密闭容器中充入10mol CO和8mol NO发生反应( ),如图3为平衡时NO的体积分数与温度、压强的关系。若在D点对反应容器降温的同时缩小体积,使体系压强增大,重新达到的平衡状态可能是图3中A~G点中的
),如图3为平衡时NO的体积分数与温度、压强的关系。若在D点对反应容器降温的同时缩小体积,使体系压强增大,重新达到的平衡状态可能是图3中A~G点中的___________ 点。

(6)电解氧化吸收法。将废气中的 转变为硝态氮。电解
转变为硝态氮。电解 NaCl溶液时,溶液中相关成分的质量浓度与电流强度的变化关系如图4。电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO的主要反应的离子方程式为
NaCl溶液时,溶液中相关成分的质量浓度与电流强度的变化关系如图4。电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO的主要反应的离子方程式为___________ 。
(1)已知:①碳的燃烧热为
 ;②
;②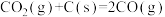
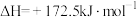 。结合图1,写出一氧化氮分解生成两种无污染气体的热化学方程式
。结合图1,写出一氧化氮分解生成两种无污染气体的热化学方程式

(2)
 还原法。研究发现反应过程如图2,此反应过程中的催化剂为
还原法。研究发现反应过程如图2,此反应过程中的催化剂为(3)
 还原法。已知催化剂Rh表面
还原法。已知催化剂Rh表面 催化还原NO的反应机理如表,其他条件一定时,决定
催化还原NO的反应机理如表,其他条件一定时,决定 催化还原NO的反应速率的基元反应为
催化还原NO的反应速率的基元反应为| 序号 | 基元反应 | 活化能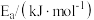 |
| ① | 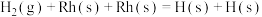 | 12.6 |
| ② | 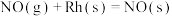 | 0.0 |
| ③ | 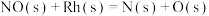 | 97.5 |
| ④ |  | 83.7 |
| ⑤ | 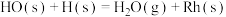 | 33.5 |
| ⑥ |  | 45.0 |
| ⑦ | 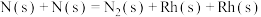 | 120.9 |
| ⑧ | 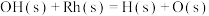 | 37.7 |
| ⑨ | 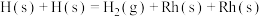 | 77.8 |
| ⑩ | 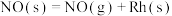 | 108.9 |
(4)
 还原法。利用甲烷可实现氮氧化物的消除,反应原理为
还原法。利用甲烷可实现氮氧化物的消除,反应原理为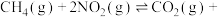
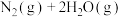
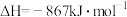 。一定温度下,在2.0L刚性密闭容器中通入1mol
。一定温度下,在2.0L刚性密闭容器中通入1mol  和2mol
和2mol  ,测得反应时间(t)与容器内气体总压强(p)的变化如表所示。
,测得反应时间(t)与容器内气体总压强(p)的变化如表所示。| 反应时间t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强p/(100kPa) | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
达到平衡时,
 的转化率为
的转化率为 和2mol
和2mol  ,则该温度下的压强平衡常数
,则该温度下的压强平衡常数
(5)CO还原法。汽车尾气(CO、NO)可转化为无毒、无害物质。在密闭容器中充入10mol CO和8mol NO发生反应(
 ),如图3为平衡时NO的体积分数与温度、压强的关系。若在D点对反应容器降温的同时缩小体积,使体系压强增大,重新达到的平衡状态可能是图3中A~G点中的
),如图3为平衡时NO的体积分数与温度、压强的关系。若在D点对反应容器降温的同时缩小体积,使体系压强增大,重新达到的平衡状态可能是图3中A~G点中的

(6)电解氧化吸收法。将废气中的
 转变为硝态氮。电解
转变为硝态氮。电解 NaCl溶液时,溶液中相关成分的质量浓度与电流强度的变化关系如图4。电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO的主要反应的离子方程式为
NaCl溶液时,溶液中相关成分的质量浓度与电流强度的变化关系如图4。电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO的主要反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】(一)镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为
①Ni(s)+4CO(g) Ni(CO)4(g) ΔH<0
Ni(CO)4(g) ΔH<0
②Ni(CO)4(g) Ni(s)+4CO(g) ΔH>0
Ni(s)+4CO(g) ΔH>0
完成下列填空:
(1)在温度不变的情况下,要提高反应①中Ni(CO)4的产率,可采取的措施有____ 、____ 。
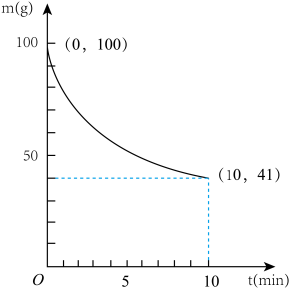
(2)已知在一定条件下2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如图所示。Ni(CO)4在0~10min的平均反应速率为_____ 。
(3)若反应②达到平衡后,保持其他条件不变,降低温度,重新达到平衡时___ 。
a.平衡常数K增大 b.CO的浓度减小
c.Ni的质量减小 d.υ逆[Ni(CO)4]增大
(二)已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) ΔH=-57kJ·mol-1,一定温度下,将1molN2O4充入一恒压密闭容器中。
N2O4(g) ΔH=-57kJ·mol-1,一定温度下,将1molN2O4充入一恒压密闭容器中。
(1)下列示意图正确且能说明反应达到平衡状态的是___ 。
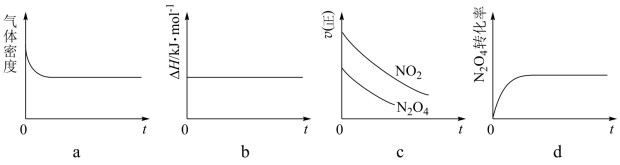
(2)若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数____ (填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率υ(N2O4)=___ mol·L-1·s-1。
(3)达到平衡后,若向该恒压容器中再充入0.5molHe,则平衡将__ (填“向左移动”“向右移动”或“不移动”)。
(4)该反应在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是___ (填字母序号)。
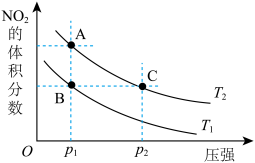
a.A、C两点气体的颜色:A深,C浅
b.A、C两点NO2的转化率:A<C
c.B、C两点的气体的平均相对分子质量:B<C
d.由状态B到状态A,可以用加热的方法
(三)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1丁烯(C4H8)的热化学方程式如下:
已知:
①C4H10(g) C4H8(g)+H2(g) ΔH1
C4H8(g)+H2(g) ΔH1
②C4H10(g)+ O2(g)=C4H8(g)+H2O(g) ΔH2=-119kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119kJ·mol-1
③H2(g)+ O2(g)=H2O(g) ΔH3=-242kJ·mol-1
O2(g)=H2O(g) ΔH3=-242kJ·mol-1
反应①的ΔH1为____ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x___ 0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是___ (填标号)。
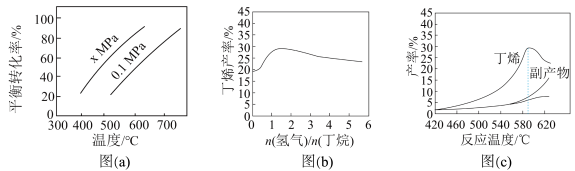
A.升高温度 B.降低温度
C.增大压强 D.降低压强
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是__ 。
①Ni(s)+4CO(g)
 Ni(CO)4(g) ΔH<0
Ni(CO)4(g) ΔH<0②Ni(CO)4(g)
 Ni(s)+4CO(g) ΔH>0
Ni(s)+4CO(g) ΔH>0完成下列填空:
(1)在温度不变的情况下,要提高反应①中Ni(CO)4的产率,可采取的措施有
(2)已知在一定条件下2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如图所示。Ni(CO)4在0~10min的平均反应速率为

(3)若反应②达到平衡后,保持其他条件不变,降低温度,重新达到平衡时
a.平衡常数K增大 b.CO的浓度减小
c.Ni的质量减小 d.υ逆[Ni(CO)4]增大
(二)已知NO2和N2O4可以相互转化:2NO2(g)
 N2O4(g) ΔH=-57kJ·mol-1,一定温度下,将1molN2O4充入一恒压密闭容器中。
N2O4(g) ΔH=-57kJ·mol-1,一定温度下,将1molN2O4充入一恒压密闭容器中。(1)下列示意图正确且能说明反应达到平衡状态的是

(2)若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数
(3)达到平衡后,若向该恒压容器中再充入0.5molHe,则平衡将
(4)该反应在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

a.A、C两点气体的颜色:A深,C浅
b.A、C两点NO2的转化率:A<C
c.B、C两点的气体的平均相对分子质量:B<C
d.由状态B到状态A,可以用加热的方法
(三)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1丁烯(C4H8)的热化学方程式如下:
已知:
①C4H10(g)
 C4H8(g)+H2(g) ΔH1
C4H8(g)+H2(g) ΔH1②C4H10(g)+
 O2(g)=C4H8(g)+H2O(g) ΔH2=-119kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119kJ·mol-1③H2(g)+
 O2(g)=H2O(g) ΔH3=-242kJ·mol-1
O2(g)=H2O(g) ΔH3=-242kJ·mol-1反应①的ΔH1为

A.升高温度 B.降低温度
C.增大压强 D.降低压强
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】SnO2是锡的重要氧化物,现以锡锑渣(主要含塑料及SnO2、Sb4O6、PbO2)为原料,提纯SnO2的工艺流程图如下:
②Na2SnO3可溶于水,难溶于乙醇。
请回答下列问题:
(1)“焙烧”的主要目的是_______ 。
(2)“沉铅”时同时生成S沉淀的化学方程式_______ 。
(3)“还原”时Na3SbO4发生的离子方程式为_______ 。
(4)在不同溶剂中Na2SnO3的溶解度随温度变化如图。_______ 。
②由Na2SnO3溶液可获得Na2SnO3晶体,具体操作方法为_______ 、用_______ 洗涤、干燥。
(5)下列冶炼方法与本工艺流程中加入焦炭冶炼锡的方法相似的是_______。
(6)将10kg锡锑渣进行碱浸,“还原”时消耗0. 13kg锡粒,假设其余各步损失不计,干燥后称量锡酸钠质量为4. 0kg,滴定测得锡酸钠中锡的质量分数为53. 5%。锡锑渣中锡元素的质量分数为_______ 。

②Na2SnO3可溶于水,难溶于乙醇。
请回答下列问题:
(1)“焙烧”的主要目的是
(2)“沉铅”时同时生成S沉淀的化学方程式
(3)“还原”时Na3SbO4发生的离子方程式为
(4)在不同溶剂中Na2SnO3的溶解度随温度变化如图。
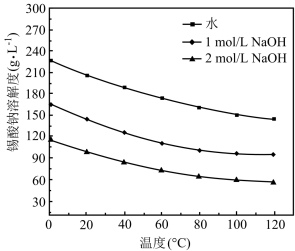
②由Na2SnO3溶液可获得Na2SnO3晶体,具体操作方法为
(5)下列冶炼方法与本工艺流程中加入焦炭冶炼锡的方法相似的是_______。
| A.工业制粗硅 | B.电解熔融氯化钠制钠 |
| C.氧化汞分解制汞 | D.工业炼铁 |
(6)将10kg锡锑渣进行碱浸,“还原”时消耗0. 13kg锡粒,假设其余各步损失不计,干燥后称量锡酸钠质量为4. 0kg,滴定测得锡酸钠中锡的质量分数为53. 5%。锡锑渣中锡元素的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】根据相关知识回答下列问题
(1)①已知H2与O2反应生成lmolH2O(g)时放出241.8kJ的热量,请完成该反应的热化学方程式:2H2(g)+O2(g)-2H2O(g)△H=_____________ kJ/mol;
②已知:C(石墨,s)=C(金刚石,s)△H>0 则稳定性:石墨_________ 金刚石(填“>”、“<“或“=”)。
(2)①25℃时,0.10mol/L的NaHCO3溶液呈碱性,原因是_________ 水解引起的(填“Na+”或“HCO3-”);该溶液中c(Na+)+c(HCO3-)_________ 0.2mol/L(填“>”、“<“或 “=”)
②常温下,0.0100mol/L盐酸的pH=________________ ;
③用0.0100mol/L盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为__________ (填“蓝色“或“无色”),且半分钟内保持不变。
(3)在某密闭容器中进行可逆反应:FeO(s)+CO(g) Fe(s)+CO2(g)△H>0, 平衡常数表达式为K=
Fe(s)+CO2(g)△H>0, 平衡常数表达式为K=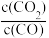
①反应达到平衡后,向容器中通入CO,化学平衡向__________ 方向移动(填“正反应”或“逆反应”);
②若升高温度,平衡常数K____________ (填“增大”、“减少”“不变”);
③查阅资料得知1100℃时K=0.263。某时刻测得容器中c(CO2)=0.025mol/L,c(CO)=0.10mol/L,此时刻反应_____________ 平衡状态(填“达到”或“未达到”);其理由为:__________ (写出必要的计算过程)。
(1)①已知H2与O2反应生成lmolH2O(g)时放出241.8kJ的热量,请完成该反应的热化学方程式:2H2(g)+O2(g)-2H2O(g)△H=
②已知:C(石墨,s)=C(金刚石,s)△H>0 则稳定性:石墨
(2)①25℃时,0.10mol/L的NaHCO3溶液呈碱性,原因是
②常温下,0.0100mol/L盐酸的pH=
③用0.0100mol/L盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为
(3)在某密闭容器中进行可逆反应:FeO(s)+CO(g)
 Fe(s)+CO2(g)△H>0, 平衡常数表达式为K=
Fe(s)+CO2(g)△H>0, 平衡常数表达式为K=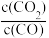
①反应达到平衡后,向容器中通入CO,化学平衡向
②若升高温度,平衡常数K
③查阅资料得知1100℃时K=0.263。某时刻测得容器中c(CO2)=0.025mol/L,c(CO)=0.10mol/L,此时刻反应
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的生成热(ΔH)。图甲为ⅥA族元素(包括氧、硫、硒、碲)氢化物a、b、c、d的生成热数据示意图。试完成下列问题。
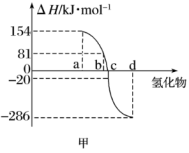
(1)请你归纳非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系:___ 。
(2)在25℃、101kPa下,已知SiH4气体在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190.0kJ,写出SiH4燃烧热的热化学方程式是___ 。
Ⅱ.可逆反应FeO(s)+CO(g) Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表:
Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表:
(3)写出该反应平衡常数的表达式___ 。
(4)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量___ ;充入氦气,混合气体的密度___ (填“增大”“减小”或“不变”)。
(5)CH4—CO2催化重整反应为CH4—CO2催化重整反应为CH4(g)+CO2(g) 2CO(g)+2H2(g)。某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
2CO(g)+2H2(g)。某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为____ mol2·L—2。
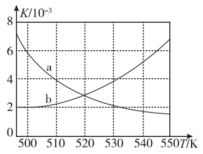
(6)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇。发生的主要反应之一为CO(g)+2H2(g) CH3OH(g) ΔH<0,如图,能正确反映平衡常数K随温度变化关系的曲线为
CH3OH(g) ΔH<0,如图,能正确反映平衡常数K随温度变化关系的曲线为____ (填曲线标记字母),其判断理由是___ 。

(1)请你归纳非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系:
(2)在25℃、101kPa下,已知SiH4气体在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190.0kJ,写出SiH4燃烧热的热化学方程式是
Ⅱ.可逆反应FeO(s)+CO(g)
 Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表:
Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表:| T/K | 938 | 1100 |
| K | 0.68 | 0.40 |
(4)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量
(5)CH4—CO2催化重整反应为CH4—CO2催化重整反应为CH4(g)+CO2(g)
 2CO(g)+2H2(g)。某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
2CO(g)+2H2(g)。某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为(6)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇。发生的主要反应之一为CO(g)+2H2(g)
 CH3OH(g) ΔH<0,如图,能正确反映平衡常数K随温度变化关系的曲线为
CH3OH(g) ΔH<0,如图,能正确反映平衡常数K随温度变化关系的曲线为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】环己烯是工业常用的化工原料。工业上通过热铂基催化剂重整将环己烷脱氢制备环己烯,其热化学方程式为
 。
。
(1)几种共价键的键能数据如下:
则a=_______  。
。
(2)在恒温恒容密闭容器中充入环己烷气体,仅发生上述反应。下列叙述正确的是_______ (填字母)。
a.混合气体的密度不随时间变化时说明该反应达到平衡状态
b.平衡后再充入环己烷气体,平衡向右移动
c.加入高效催化剂,单位时间内环己烯的产率可能会增大
d.增大固体催化剂的质量,一定能提高正、逆反应速率
(3)环己烷的平衡转化率和环己烯的选择性(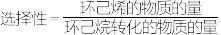 )随温度的变化如图所示:
)随温度的变化如图所示:
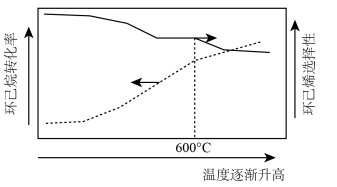
①随着温度升高,环己烷平衡转化率增大的原因是_______ 。
②当温度高于600℃时,可能的副产物有_______ (任写出其中一种结构简式)。
(4)在873K、100kPa条件下,向反应器中充入氩气和环己烷的混合气体,仅发生反应: 。
。
①环己烷的平衡转化率随 的增大而
的增大而_______ (填“升高”或“降低”或“不变”),其原因是_______ 。
②当 时,达到平衡所需时间为20min,环己烷的平衡转化率为
时,达到平衡所需时间为20min,环己烷的平衡转化率为 ,则平衡时环己烷的分压为
,则平衡时环己烷的分压为_______ kPa(保留2位小数),该环己烷脱氢反应的压强平衡常数
_______ kPa(保留2位小数)。[注:用分压计算的平衡常数为压强平衡常数( ),分压=总压×物质的量分数]
),分压=总压×物质的量分数]

 。
。(1)几种共价键的键能数据如下:
| 共价键 |  |  |  |  |
键能/ | 436 | 413 | 348 | a |
 。
。(2)在恒温恒容密闭容器中充入环己烷气体,仅发生上述反应。下列叙述正确的是
a.混合气体的密度不随时间变化时说明该反应达到平衡状态
b.平衡后再充入环己烷气体,平衡向右移动
c.加入高效催化剂,单位时间内环己烯的产率可能会增大
d.增大固体催化剂的质量,一定能提高正、逆反应速率
(3)环己烷的平衡转化率和环己烯的选择性(
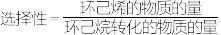 )随温度的变化如图所示:
)随温度的变化如图所示:
①随着温度升高,环己烷平衡转化率增大的原因是
②当温度高于600℃时,可能的副产物有
(4)在873K、100kPa条件下,向反应器中充入氩气和环己烷的混合气体,仅发生反应:
 。
。①环己烷的平衡转化率随
 的增大而
的增大而②当
 时,达到平衡所需时间为20min,环己烷的平衡转化率为
时,达到平衡所需时间为20min,环己烷的平衡转化率为 ,则平衡时环己烷的分压为
,则平衡时环己烷的分压为
 ),分压=总压×物质的量分数]
),分压=总压×物质的量分数]
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】丙烯是石化工业的基础原料,也是重要的有机化工原料。近年来,丙烷脱氢制丙烯工艺备受关注。丙烷脱氢过程的主反应为
反应①: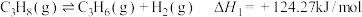
副反应为
反应②: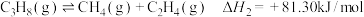
反应③: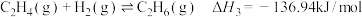
反应④:
(1)对于反应④,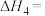
___________ 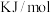
(2)该体系平衡时,下列说法正确的是___________
(3)丙烷脱氢过程的主、副反应平衡常数 与温度T(K)的关系曲线如下图
与温度T(K)的关系曲线如下图
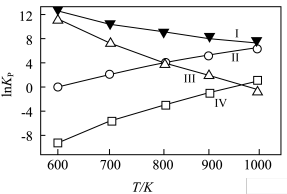
(i)从热力学的角度分析,在高温条件下,C-C键断裂的裂解反应比C-H键断裂的脱氢反应容易,由此可知,代表反应①的平衡常数 与温度T(K)的关系曲线的是
与温度T(K)的关系曲线的是___________ (填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
(ii)若仅考虑反应①,在温度为T,起始压强为P时,在刚性容器中加入一定量的丙烷,经过一段时间后,测得反应①丙烷平衡转化率为60%,则反应①的
___________ 。
(iii)下列哪些措施能提高丙烯的产率___________
A.优良的催化剂 B.低压 C.适当的升高温度 D.高压 E.通入氢气
(4)在常压下,不同温度下、不同水烃比(1mol丙烷中加入水蒸气的物质的量)的反应①丙烷脱氢平衡转化率曲线如下图
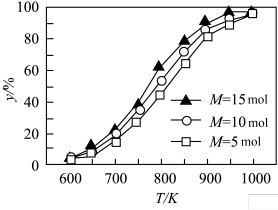
由图可知,温度为800K,最佳水烃比=___________ ,原因是___________
反应①:
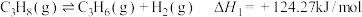
副反应为
反应②:
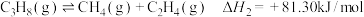
反应③:
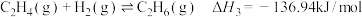
反应④:

(1)对于反应④,
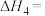
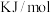
(2)该体系平衡时,下列说法正确的是___________
| A.增大压强,反应④平衡不移动 |
| B.单位时间内消耗丙烯的物质的量等于消耗丙烷的物质的量 |
| C.增大压强,气体平均摩尔质量增大 |
| D.选择适当催化剂既能提高丙烷平衡转化率和丙烯选择性 |
 与温度T(K)的关系曲线如下图
与温度T(K)的关系曲线如下图
(i)从热力学的角度分析,在高温条件下,C-C键断裂的裂解反应比C-H键断裂的脱氢反应容易,由此可知,代表反应①的平衡常数
 与温度T(K)的关系曲线的是
与温度T(K)的关系曲线的是(ii)若仅考虑反应①,在温度为T,起始压强为P时,在刚性容器中加入一定量的丙烷,经过一段时间后,测得反应①丙烷平衡转化率为60%,则反应①的

(iii)下列哪些措施能提高丙烯的产率
A.优良的催化剂 B.低压 C.适当的升高温度 D.高压 E.通入氢气
(4)在常压下,不同温度下、不同水烃比(1mol丙烷中加入水蒸气的物质的量)的反应①丙烷脱氢平衡转化率曲线如下图

由图可知,温度为800K,最佳水烃比=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】利用CO2可合成烷烃、醇等系列重要化工原料。回答下列有关问题:
I.制备甲烷:CO2(g)+4H2(g)=CH4(g)+2H2O (g) △H
已知:CH4、H2的燃烧热分别为 △H1 =—893kJ·mol-1、△H2=—285.8 kJ· mol-1,1mol液态H2O变成水蒸气需吸收44kJ的热量。
(1)△H=___________ kJ· mol-1。
II.制备甲醇:
主反应: CO2(g) + 3H2 CH3OH(g) +H2O (g) △H1=—58 kJ·mol-1
CH3OH(g) +H2O (g) △H1=—58 kJ·mol-1
副反应: CO2(g) + H2(g) CO(g) + H2O (g) △H2= +41 kJ·mol-1
CO(g) + H2O (g) △H2= +41 kJ·mol-1
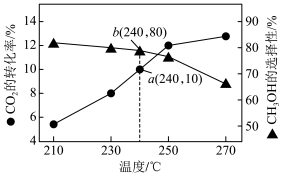
某一刚性容器中充入1molCO2和3molH2,在催化剂存在的条件下进行反应,测得温度与平衡转化率、产物选择性的关系如下图所示。
已知: CH3OH选择性=
(2)240°C该反应达到平衡时,产生的CH3OH的物质的量为___________ mol,240°C时副反应的化学平衡常数为___________ 。
(3)有研究表明,在原料气中掺入适量的CO有利于提高CH3OH选择性,说明其可能的原因是___________ , 有利于提高CH3OH选择性反应条件还可以是_____ (填标号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
I.制备甲烷:CO2(g)+4H2(g)=CH4(g)+2H2O (g) △H
已知:CH4、H2的燃烧热分别为 △H1 =—893kJ·mol-1、△H2=—285.8 kJ· mol-1,1mol液态H2O变成水蒸气需吸收44kJ的热量。
(1)△H=
II.制备甲醇:
主反应: CO2(g) + 3H2
 CH3OH(g) +H2O (g) △H1=—58 kJ·mol-1
CH3OH(g) +H2O (g) △H1=—58 kJ·mol-1副反应: CO2(g) + H2(g)
 CO(g) + H2O (g) △H2= +41 kJ·mol-1
CO(g) + H2O (g) △H2= +41 kJ·mol-1某一刚性容器中充入1molCO2和3molH2,在催化剂存在的条件下进行反应,测得温度与平衡转化率、产物选择性的关系如下图所示。

已知: CH3OH选择性=

(2)240°C该反应达到平衡时,产生的CH3OH的物质的量为
(3)有研究表明,在原料气中掺入适量的CO有利于提高CH3OH选择性,说明其可能的原因是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
您最近一年使用:0次



