氮、磷对水体的污染情况越来越受到人们的重视。回答下列问题:
(1)常温下,在 约为9时,用澄清石灰水可将水体中的
约为9时,用澄清石灰水可将水体中的 转化为
转化为 沉淀除去,该反应的离子方程式为
沉淀除去,该反应的离子方程式为_______ 。
(2)除去地下水中的硝态氮通常用还原剂将其还原为 。
。
①Prusse等提出的用 作催化剂,常温下,在
作催化剂,常温下,在 为4.0~6.0时,可直接用
为4.0~6.0时,可直接用 将
将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。研究发现用 和
和 的混合气体代替
的混合气体代替 ,
, 的去除效果比只用
的去除效果比只用 时更好,其原因是
时更好,其原因是_______ 。
②在 约为5时,用纳米
约为5时,用纳米 粉可将
粉可将 还原为
还原为 ,
, 粉被氧化为
粉被氧化为 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为_______ 。
(3)实验测得相同条件下,用次氯酸钠脱除水体中的氨态氮的过程中(
 ),
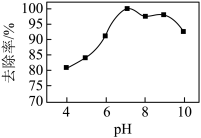
), 与氨态氮的去除率关系如图所示,在
与氨态氮的去除率关系如图所示,在 大于9时,
大于9时, 越大,去除率越小,其原因是
越大,去除率越小,其原因是_______ 。
(1)常温下,在
 约为9时,用澄清石灰水可将水体中的
约为9时,用澄清石灰水可将水体中的 转化为
转化为 沉淀除去,该反应的离子方程式为
沉淀除去,该反应的离子方程式为(2)除去地下水中的硝态氮通常用还原剂将其还原为
 。
。①Prusse等提出的用
 作催化剂,常温下,在
作催化剂,常温下,在 为4.0~6.0时,可直接用
为4.0~6.0时,可直接用 将
将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为 和
和 的混合气体代替
的混合气体代替 ,
, 的去除效果比只用
的去除效果比只用 时更好,其原因是
时更好,其原因是②在
 约为5时,用纳米
约为5时,用纳米 粉可将
粉可将 还原为
还原为 ,
, 粉被氧化为
粉被氧化为 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为(3)实验测得相同条件下,用次氯酸钠脱除水体中的氨态氮的过程中(

 ),
), 与氨态氮的去除率关系如图所示,在
与氨态氮的去除率关系如图所示,在 大于9时,
大于9时, 越大,去除率越小,其原因是
越大,去除率越小,其原因是
19-20高三上·山东临沂·阶段练习 查看更多[10]
(已下线)第3讲 氧化还原反应黑龙江省牡丹江市第二高级中学2022-2023学年高三上学期第三次月考化学试题江西省丰城市第九中学2022-2023学年高三上学期摸底考(日新班)化学试题吉林省长春吉大附中实验学校2021-2022学年高三上学期第三次摸底考试化学试题(已下线)第14周 周测卷-备战2022年高考化学周测与晚练(新高考专用)广东省普通高中2022届高三9月阶段性质量检测化学试题(已下线)考点11 弱电解质的电离及溶液pH-2020年高考化学命题预测与模拟试题分类精编山东省新高考备考监测2020届高三10月联考化学试题2019年湖北省黄冈市高三11月新高考备考监测联考化学试题山东省临沂市第一中学2020届高三10月月考化学试题
更新时间:2021-09-14 17:49:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe2(SO4)3,在反应后的溶液中滴加KSCN溶液不显红色。
(1)该反应中,被氧化的元素是____________ ,氧化剂是____________ 。
(2)写出该反应的化学方程式并标明电子转移的方向和数目:_____________________ 。
(3) 由此可知,氧化性强弱的关系是:Fe2(SO4)3____________ 。SnCl4, 还原性强弱的关系是:SnCl2__ FeSO4(填>,﹤或 = )
(1)该反应中,被氧化的元素是
(2)写出该反应的化学方程式并标明电子转移的方向和数目:
(3) 由此可知,氧化性强弱的关系是:Fe2(SO4)3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】焦亚硫酸钠(Na2S2O5) 是常用的脱氧剂,其制备方法是向Na2CO3溶液中通入SO2,生成NaHSO3和CO2,一定条件下NaHSO3 转化为Na2S2O5。完成下列填空:
(1) 碳原子的原子结构示意图是_____________ ;CO2的化学键类型_______________________ 。
(2) 从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。______________________ 。
(3)SO2 与Na2CO3 溶液反应生成NaHSO3 和CO2 ,其化学方程式为_____________________ ,证明NaHSO3 溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________________ 。
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+ H2O→Na2SO4+ H2SO4,该反应中,氧化产物是_____ ;若反应中转移了0.04 mol 的电子,有____ g Na2S2O5参加反应。
(5)连二亚硫酸钠Na2S2O4俗称保险粉,广泛用于纺织工业的还原性染色、清洗、印花、脱色以及织物的漂白等。Na2S2O4属于强还原剂,暴露于空气中易被氧气氧化。Na2S2O4遇KMnO4 酸性溶液发生反应:
5Na2S2O4+6KMnO4+4H2SO4=5Na2SO4+3K2SO4+6MnSO4+4H2O。为了测定保险粉纯度。称取5.0g Na2S2O4样品溶于冷水中,配成100mL溶液,取出10mL 该溶液于锥形瓶中,用0.1000mol/L的KMnO4 溶液滴定。重复上述操作2 次,平均消耗KMnO4 溶液21.00mL。则该样品中Na2S2O4的质量分数为________ (杂质不参与反应)。(保留至0.1%)
(1) 碳原子的原子结构示意图是
(2) 从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。
(3)SO2 与Na2CO3 溶液反应生成NaHSO3 和CO2 ,其化学方程式为
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+ H2O→Na2SO4+ H2SO4,该反应中,氧化产物是
(5)连二亚硫酸钠Na2S2O4俗称保险粉,广泛用于纺织工业的还原性染色、清洗、印花、脱色以及织物的漂白等。Na2S2O4属于强还原剂,暴露于空气中易被氧气氧化。Na2S2O4遇KMnO4 酸性溶液发生反应:
5Na2S2O4+6KMnO4+4H2SO4=5Na2SO4+3K2SO4+6MnSO4+4H2O。为了测定保险粉纯度。称取5.0g Na2S2O4样品溶于冷水中,配成100mL溶液,取出10mL 该溶液于锥形瓶中,用0.1000mol/L的KMnO4 溶液滴定。重复上述操作2 次,平均消耗KMnO4 溶液21.00mL。则该样品中Na2S2O4的质量分数为
您最近一年使用:0次
【推荐1】工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。该法的工艺流程为
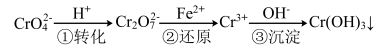
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显____________ 色.
(2)能说明第①步反应达平衡状态的是_____________ 。
a Cr2O72-和CrO42-的浓度相同 b 2v(Cr2O72-)=v(CrO42-)
c 溶液的颜色不变 d.溶液的pH值不变
(3)第②步中,还原0.01mol Cr2O72-离子,需要________ mol的FeSO4·7H2O。
(4)许多过渡(金属)元素的氢氧化物在水中有两种电离方式,Cr(OH)3在溶液中存在以下平衡:H+ + CrO2-(亮绿色)+H2O Cr(OH)3(s)
Cr(OH)3(s) Cr3+(紫色)+ 3OH-
Cr3+(紫色)+ 3OH-
下列有关说法中正确的是_______
a 加酸则平衡向右移动,则生成Cr3+盐,加碱则平衡向左移动,生成亚铬酸盐(CrO2-)
b 在一定条件下存在:Cr(OH)3+OH-=CrO2-+2H2O;Cr(OH)3+3H+=Cr3++3H2O
c Cr3+盐中加入NaOH溶液,先产生沉淀,后沉淀消失,溶液变成无色
d Cr(OH)3(固)在水中的存在叁个平衡

其中第①步存在平衡:2CrO42-(黄色)+2H+
 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O(1)若平衡体系的pH=2,则溶液显
(2)能说明第①步反应达平衡状态的是
a Cr2O72-和CrO42-的浓度相同 b 2v(Cr2O72-)=v(CrO42-)
c 溶液的颜色不变 d.溶液的pH值不变
(3)第②步中,还原0.01mol Cr2O72-离子,需要
(4)许多过渡(金属)元素的氢氧化物在水中有两种电离方式,Cr(OH)3在溶液中存在以下平衡:H+ + CrO2-(亮绿色)+H2O
 Cr(OH)3(s)
Cr(OH)3(s) Cr3+(紫色)+ 3OH-
Cr3+(紫色)+ 3OH-下列有关说法中正确的是
a 加酸则平衡向右移动,则生成Cr3+盐,加碱则平衡向左移动,生成亚铬酸盐(CrO2-)
b 在一定条件下存在:Cr(OH)3+OH-=CrO2-+2H2O;Cr(OH)3+3H+=Cr3++3H2O
c Cr3+盐中加入NaOH溶液,先产生沉淀,后沉淀消失,溶液变成无色
d Cr(OH)3(固)在水中的存在叁个平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在一个固定体积的密闭容器内,保持一定的温度发生以下反应:H2+Br2⇌2HBr.已知加入1mol H2和2mol Br2 时,达到平衡状态生成a mol HBr.在相同条件下,且保持平衡时的各物质的百分含量相同,则填写下列空白:
| 编号 | 起始状态(mol) | 平衡时HBr 物质的量(mol) | ||
| H2 | Br2 | HBr | ||
| 已知 | 1 | 2 | 0 | a |
| ① | 2 | 4 | 0 | |
| ② | 1 | 0.5a | ||
| ③ | m | n(n≥2m) | ||
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】CO2甲烷化反应为:CO2+4H2⇌CH4+2H2O,易发生副反应生成CO,CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41kJ/mol。不同条件下,按照n(CO2):n(H2)=1:4投料同时发生CO2甲烷化反应和副反应,CO2的平衡转化率如图所示。
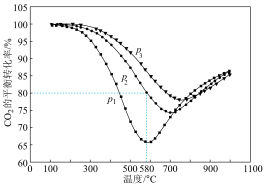
(1)CO2甲烷化反应的ΔH_______ 0(填“>”“<"或“=”)。
(2)压强p1、p2、p3由大到小的顺序是_______ 。压强为p2时,随着温度升高,CO2平衡转化率先减小后增大的原因是_______ 。
(3)580℃,压强为p2条件下,CH4的选择性为80%[CH4选择性=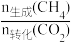 ×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=
×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=_______ 。

(1)CO2甲烷化反应的ΔH
(2)压强p1、p2、p3由大到小的顺序是
(3)580℃,压强为p2条件下,CH4的选择性为80%[CH4选择性=
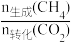 ×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=
×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=
您最近一年使用:0次
【推荐1】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如图所示。

(1)pH=3时溶液中铜元素的主要存在形式是___________ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液pH范围在___________ 。
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,___________ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___________ 。
(4)已知一些难溶物的溶度积常数如表。
为除去某工业废水中含有的Cu2+、Pb2+、Hg2+杂质,最适宜向此工业废水中加入过量的___________ (填选项)。
A.NaOH B.FeS C.Na2S
(5)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20。在25℃时,向浓度均为0.1mol•L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成___________ (填化学式)沉淀。
(6)已知25℃时,Ksp[Fe(OH)3]=2.6×10-39,该温度下反应Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数K=___________ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液pH范围在
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
(4)已知一些难溶物的溶度积常数如表。
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-35 | 3.4×10-28 | 6.4×10-33 | 1.6×10-24 |
A.NaOH B.FeS C.Na2S
(5)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20。在25℃时,向浓度均为0.1mol•L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
(6)已知25℃时,Ksp[Fe(OH)3]=2.6×10-39,该温度下反应Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铵盐是实验室常用试剂。回答下列问题:
(1)NH4Cl溶液中 水解的离子方程式为
水解的离子方程式为_____ ;加入镁粉可产生大量气体,该气体的成分是______ (写化学式)。
(2)物质的量浓度相同的下列四种铵盐的溶液中,c( )从大到小的顺序为
)从大到小的顺序为______ (用标号表示)。
A.(NH4)2CO3 B.CH3COONH4 C.NH4HSO4 D.NH4Cl
(3)少量Mg(OH)2能溶于CH3COONH4浓溶液(呈中性)的原因是______ (用文字和方程式说明)。
(4)甲醛法测定铵盐中氮的质量分数的实验步骤如下:步骤I.称取a g (NH4)2SO4样品,用水溶解后定容于250 mL容量瓶中;步骤II.取出25.00 mL溶液于锥形瓶中,加入足量中性甲醛溶液[4 +6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
+6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
①滴定到终点时,溶液颜色的变化是__________ 。
②该(NH4)2SO4样品中氮的质量分数为______ (用含a、c、V的代数式表示)。
③推测下列铵盐中不能用该法测定其中氮的质量分数的是______ (填标号)。
A.NH4Cl B.NH4HCO3 C.NH4NO3 D.CH3COONH4
(1)NH4Cl溶液中
 水解的离子方程式为
水解的离子方程式为(2)物质的量浓度相同的下列四种铵盐的溶液中,c(
 )从大到小的顺序为
)从大到小的顺序为A.(NH4)2CO3 B.CH3COONH4 C.NH4HSO4 D.NH4Cl
(3)少量Mg(OH)2能溶于CH3COONH4浓溶液(呈中性)的原因是
(4)甲醛法测定铵盐中氮的质量分数的实验步骤如下:步骤I.称取a g (NH4)2SO4样品,用水溶解后定容于250 mL容量瓶中;步骤II.取出25.00 mL溶液于锥形瓶中,加入足量中性甲醛溶液[4
 +6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
+6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。①滴定到终点时,溶液颜色的变化是
②该(NH4)2SO4样品中氮的质量分数为
③推测下列铵盐中不能用该法测定其中氮的质量分数的是
A.NH4Cl B.NH4HCO3 C.NH4NO3 D.CH3COONH4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列问题。
(1)已知NaA水溶液呈碱性。
①NaA水溶液呈碱性的原因___________ (用离子方程式解释)。
②在NaA水溶液中各离子浓度的大小关系是___________ 。
(2)实验室在配制AlCl3的溶液时,为了抑制AlCl3的水解可加入少量的___________ (填写物质的名称)。把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。(填化学式)
(3)毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用重石制备BaCl2·2H2O的流程如图:

已知:
Ksp(BaC2O4)=1.6×10−7,Ksp(CaC2O4)=2.3×10−9。
加入NH3·H2O调pH=8可除去_____ (填离子符号),滤渣Ⅱ中含______ (填化学式)。加入H2C2O4时应避免过量,原因是_____ 。
(1)已知NaA水溶液呈碱性。
①NaA水溶液呈碱性的原因
②在NaA水溶液中各离子浓度的大小关系是
(2)实验室在配制AlCl3的溶液时,为了抑制AlCl3的水解可加入少量的
(3)毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用重石制备BaCl2·2H2O的流程如图:

已知:
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
加入NH3·H2O调pH=8可除去
您最近一年使用:0次



