对于可逆反应2SO2(g)+O2(g)  2SO3(g) ΔH<0,升高温度产生的影响是
2SO3(g) ΔH<0,升高温度产生的影响是
 2SO3(g) ΔH<0,升高温度产生的影响是
2SO3(g) ΔH<0,升高温度产生的影响是| A.正反应速率增大,逆反应速率减小 |
| B.正反应速率减小,逆反应速率增大 |
| C.正、逆反应速率同等程度的增大 |
| D.正、逆反应速率不同程度的增大 |
更新时间:2021-10-09 21:49:05
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是( )
| 编号 | 金属(粉末状) | 酸的浓度 | 酸的体积 | 反应温度 |
| A | 0.1 mol Mg | 6 mol/L硝酸 | 10 mL | 60℃ |
| B | 0.1 mol Mg | 6 mol/L盐酸 | 10 mL | 60℃ |
| C | 0.1 mol Fe | 3 mol/L硫酸 | 10 mL | 60℃ |
| D | 0.1 mol Mg | 3 mol/L硫酸 | 10 mL | 30℃ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】反应C(s)+H2O(g) CO(g)+ H2(g)在一可变容积的密闭容器中进行, 在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是
CO(g)+ H2(g)在一可变容积的密闭容器中进行, 在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是
 CO(g)+ H2(g)在一可变容积的密闭容器中进行, 在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是
CO(g)+ H2(g)在一可变容积的密闭容器中进行, 在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是| A.增加CO的物质的量 | B.保持压强不变,充入N2使容器体积变大 |
| C.保持体积不变,充入N2使体系压强增大 | D.将容器的体积缩小一半 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】化学与生活、社会、科技和环境密切相关。下列说法正确的是
| A.地下管道用导线连接锌块可以减缓管道的腐蚀 |
| B.电解过程中,化学能转化为电能“储存”起来 |
| C.催化剂可降低水分解反应的焓变,有利于开发氢能源 |
| D.电器着火可用泡沫灭火器灭火 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在一可变容积的密闭容器中进行反应:C(s) + H2O(g)= CO(g) + H2(g),下列条件的改变能使反应速率减慢的是
| A.增加C的量 | B.将容器的体积缩小一半 |
| C.保持体积不变,充入N2,使体系的压强增大 | D.保持压强不变,充入N2,使容器的体积变大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】碳是生命的核心元素,碳及其化合物在工农业生产中有着广泛的应用。工业上用CO2生产CH3OH燃料,其热化学方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),下列有关说法正确的是
CH3OH(g)+H2O(g),下列有关说法正确的是
 CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),下列有关说法正确的是
CH3OH(g)+H2O(g),下列有关说法正确的是A.增大 的值,可提高H2的转化率 的值,可提高H2的转化率 |
| B.升高温度能提高CO2的反应速率和转化率 |
C.达平衡时缩小容器体积, (正)增大, (正)增大, (逆)减小 (逆)减小 |
| D.1molCO2和3molH2充分反应时放出的热量为49.0kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关说法正确的是
| A.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
B.  ,升高温度,反应速率v(H2)和氢气的平衡转化率均增大 ,升高温度,反应速率v(H2)和氢气的平衡转化率均增大 |
| C.升高温度,单位体积分子总数增大,活化分子百分数不变,化学反应速率增大 |
D.常温下,反应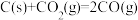 不能自发进行,则该反应的 不能自发进行,则该反应的 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列事实,不能用勒夏特列原理解释的是
| A.硫酸工业中,增大O2的浓度有利于提高SO2的转化率 |
B.对2HI(g) H2(g)+I2(g)平衡体系增加压强使颜色变深 H2(g)+I2(g)平衡体系增加压强使颜色变深 |
| C.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| D.滴有酚酞的氨水溶液,适当加热溶液(氨气不挥发)后颜色变深(注:NH3·H2O的电离是吸热反应) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关物质性质与用途对应关系不正确 的是( )
| A.NaHCO3受热易分解,可用于制胃酸中和剂 |
| B.CaO能与SO2反应,可作为工业废气处理时的脱硫剂 |
| C.硅的导电性介于导体和绝缘体之间,可用于制造计算机硅芯片的材料 |
| D.饱和氯水既有酸性又有漂白性,加入适量NaHCO3固体,其漂白性增强 |
您最近一年使用:0次

 。若保持其他条件不变,升高温度,H2平衡浓度变小,下列说法正确的是
。若保持其他条件不变,升高温度,H2平衡浓度变小,下列说法正确的是
 (CH3COOH)2
(CH3COOH)2

