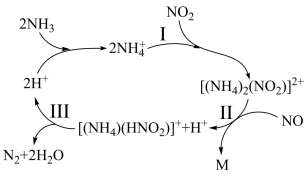
硝酸是一种具有强氧化性、腐蚀性的强酸。硝酸工业与合成氨工业紧密相关,氨氧化法是工业生产中制取硝酸的主要途径,其主要流程是将氨和空气的混合气通入灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮(NO)。生成的一氧化氮利用反应后残余的氧气继续氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸。4NH3+5O2 4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知4NH3(g)+5O2(g)
4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知4NH3(g)+5O2(g) 4NO(g)+6H2O(g)为可逆反应,下列有关说法不正确的是
4NO(g)+6H2O(g)为可逆反应,下列有关说法不正确的是
 4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知4NH3(g)+5O2(g)
4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知4NH3(g)+5O2(g) 4NO(g)+6H2O(g)为可逆反应,下列有关说法不正确的是
4NO(g)+6H2O(g)为可逆反应,下列有关说法不正确的是| A.反应△S>0 |
| B.反应中生成22.4LNO时,转移2.5mol电子 |
| C.氨气在足量的氧气中,催化氧化的产物是NO |
| D.减压、增加氧气能提高氨气的平衡转化率 |
更新时间:2021-10-19 19:43:11
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】2022年的诺贝尔化学奖得主美国科学家K.Barry Sharpless,在不对称催化领域起了奠基性的作用,其中Sharpless环氧化反应是现代有机合成中最重要的基本反应之一,下列变化中,需要加入氧化剂才能实现的氧化反应是
A.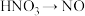 | B.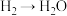 | C.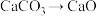 | D. |
您最近一年使用:0次
【推荐2】N2O既是医学上的一种麻醉剂,又是一种常见的温室气体。制取N2O的方法有很多,例如:
①NH4NO3=N2O↑+2H2O
②K2SO3+2NO=K2SO4+N2O
③2NH3+2O2=N2O+3H2O
④2NaNO3+(NH4)2SO4=2N2O↑+Na2SO4+4H2O
下列说法中正确的是
①NH4NO3=N2O↑+2H2O
②K2SO3+2NO=K2SO4+N2O
③2NH3+2O2=N2O+3H2O
④2NaNO3+(NH4)2SO4=2N2O↑+Na2SO4+4H2O
下列说法中正确的是
| A.反应①中NH4NO3既是氧化剂又是还原剂,H2O是氧化产物 |
| B.反应②中K2SO3是还原剂,N2O是氧化产物 |
| C.反应③中每生成1个N2O,转移8个电子 |
| D.反应④中NaNO3是还原剂,N2O既是氧化产物又是还原产物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】Mg、Al两种金属分别跟相同体积、相同浓度的稀H2SO4反应,同温同压下生成氢气的体积相同,则Mg、Al两种金属之间的量的关系一定正确的是
| A.两个反应转移的电子数目相等 |
| B.加入镁、铝的质量比为4:3 |
| C.金属溶解的物质的量相等 |
| D.加入的两种金属的质量不等 |
您最近一年使用:0次
【推荐2】水热法制备Fe3O4纳米颗粒的总反应:3Fe2++2S2O +O2+x M=Fe3O4+S4O
+O2+x M=Fe3O4+S4O +2H2O,下列有关说法正确的是
+2H2O,下列有关说法正确的是
 +O2+x M=Fe3O4+S4O
+O2+x M=Fe3O4+S4O +2H2O,下列有关说法正确的是
+2H2O,下列有关说法正确的是| A.M为OH-离子,x = 4 |
| B.只有Fe2+是还原剂 |
C.O2、S2O 都是氧化剂 都是氧化剂 |
| D.每生成1molFe3O4,反应中转移3mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知反应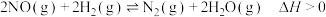 ,其正反应速率方程为
,其正反应速率方程为 (
( 为速率常数,只与温度、催化剂有关),下列说法错误的是
为速率常数,只与温度、催化剂有关),下列说法错误的是
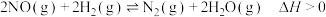 ,其正反应速率方程为
,其正反应速率方程为 (
( 为速率常数,只与温度、催化剂有关),下列说法错误的是
为速率常数,只与温度、催化剂有关),下列说法错误的是| A.NO的浓度对反应速率的影响大于氢气的浓度对反应速率的影响 |
| B.其他条件不变,压缩容器体积,体系内活化分子百分数增大 |
| C.达到平衡时升温,该反应向正反应方向进行 |
D.某时刻降低温度, 减小,体系内活化分子百分数减小 减小,体系内活化分子百分数减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NO2与N2O4能相互转化,热化学方程式为N2O4(g)⇌2NO2(g)ΔH=57kJ·mol-1,下列有关说法正确的是
| A.升高体系温度正反应速率增大,逆反应速率也增大 |
| B.若容器体积不变,气体密度不变时说明该反应建立化学平衡 |
C.其它条件不变,向平衡后的容器中再加入少量N2O4, 的值变大 的值变大 |
| D.增大体系的压强能提高N2O4的反应速率和转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】如下图表示反应2SO2(g)+O2(g) 2SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
2SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是

 2SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
2SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
| A.t1时增加了SO2和O2的浓度,平衡向正反应方向移动 |
| B.t1时降低了温度,平衡向正反应方向移动 |
| C.t1时减小了压强,平衡向逆反应方向移动 |
| D.t1时减小了SO2的浓度,又增加了SO3的浓度,导致平衡向逆反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列与化学反应能量变化相关的叙述中错误的是
| A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的∆H相同 |
| B.物质发生化学变化一定伴随能量的变化 |
| C.放热反应的反应速率总是大于吸热反应的反应速率 |
| D.水凝结成冰的过程中,ΔH<0、ΔS<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:△G=△H-T△S,当△G<0,反应能自发进行,△G>0反应不能自发进行。下列说法中正确的是
| A.非自发反应在任何条件下都不能发生 |
| B.熵增加且放热的反应一定是自发反应 |
| C.自发反应一定是熵增加的反应,非自发反应一定是熵减小或不变的反应 |
| D.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】相同的温度和压强下,有关下列两个反应的说法不正确 的是
注:①其中△n表示反应方程式中气体系数差;
②△H-T△S<0的反应方向自发
| 反应 | △H/kJ•mol-1 | △n | △S/J•K•mol-1 |
| MgCO3(s)=MgO(s)+CO2(g) | 117.6 | 1 | a |
| CaCO3(s)=CaO(s)+CO2(g) | 177.9 | 1 | b |
②△H-T△S<0的反应方向自发
| A.因为△n相同,所以a与b大小相近 |
| B.热分解温度:MgCO3(s)>CaCO3(s) |
| C.a-b=S[MgO(s)]+S[CaCO3(s)]-S[MgCO3(s)]-S[CaO(s)] |
| D.两个反应在不同温度下的△H和△S都大于零 |
您最近一年使用:0次

 ,其中反应前后B元素化合价不变。下列说法错误的是
,其中反应前后B元素化合价不变。下列说法错误的是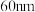 ,因此纳米铁是胶体
,因此纳米铁是胶体 ,氢气既是氧化产物又是还原产物
,氢气既是氧化产物又是还原产物
 参加反应,则反应中转移电子的物质的量为
参加反应,则反应中转移电子的物质的量为