常温下,下列有关叙述正确的是(双选)
| A.pH=8的NaY溶液中,c(Na+)-c(Y-)=9.9×10-7mol·L-1 |
B.Na2CO3溶液中,2c(Na+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
C.pH相等的①NH4NO3 ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH )大小顺序①=②>③ )大小顺序①=②>③ |
| D.10 mL pH=12的NaOH溶液中加入pH=2的HA溶液至pH=7,则所得溶液体积一定为20 mL(忽略溶液混合时体积变化) |
2018·重庆·模拟预测 查看更多[7]
(已下线)2019年高考江苏卷化学试题变式题(不定项选择题)(已下线)专题26 盐类的水解(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第23讲 盐类水解(练) — 2022年高考化学一轮复习讲练测(新教材新高考)2020届高三化学二轮冲刺新题专练——混合溶液中微粒浓度大小比较2020届高三化学二轮冲刺新题专练——混合型溶液中微粒浓度大小的比较(提升练)【全国百强校】黑龙江省鹤岗市第一中学2019届高三上学期第三次月考化学试题【全国百强校】重庆市西南大学附属中学校2018届高三第六次月考(3月)理科综合化学试题
更新时间:2021-10-20 14:38:05
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关电解质溶液的说法正确的是
| A.25℃时 pH=2 的 HF 溶液中,由水电离产生的 OH-浓度为 10-12 mol·L-1 |
| B.0.1 mol·L-1 Na2CO3 溶液中:c(Na+)=c(HCO3 -)+c(H2CO3)+2c(CO32- ) |
| C.向 1 L 1 mol·L-1 的 NaOH 热溶液中通入一定量 Br2,恰好完全反应生成溴化钠、次溴酸钠和溴酸钠(溴 酸为强酸、次溴酸为弱酸)的混合溶液:c(Na+)+c(H+)=6c(BrO3-)+2c(BrO-)+c(HBrO)+c(OH-) |
| D.25℃时 pH=3 的盐酸与 pH=11 的氨水等体积混合,所得溶液的 pH<7 |
您最近半年使用:0次
多选题
|
适中
(0.65)
【推荐2】痛风性关节病的发病机理和尿酸钠有关。室温下,尿酸钠(NaUr)能溶于水,取其清液滴加盐酸,溶液中尿酸的浓度c(HUr)与pH的关系如图所示。已知Ka(HUr)=2.0×10-6。下列说法正确的是
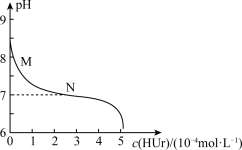

| A.上述滴加盐酸时反应的离子方程式:Ur-+H+=HUr |
B.M→N的变化过程中,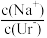 逐渐减小 逐渐减小 |
| C.N点时,c(Cl-)=c(HUr) |
| D.当c(Cl-)=c(HUr)时,c(H+)<c(OH-) |
您最近半年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作、现象 | 结论 |
| A | 向Na[Al(OH)4]溶液中滴加NaHCO3溶液,有白色胶状沉淀生成 | [Al(OH)4]-结合氢离子能力比CO 强 强 |
| B | 向等体积、等浓度的稀硫酸中分别加入少许等物质的量的ZnS和CuS固体,ZnS溶解而CuS不溶解 | Ksp(CuS)>Ksp(ZnS) |
| C | 常温下,用pH计测0.1mol/LNaX溶液和0.lmol/LNaF溶液的pH,前者小于后者 | 酸性:HX<HF |
| D | 10mL0.1mol/LFeCl3溶液和20mL0.1mol·L-1KI溶液混合,充分反应后,一份滴加淀粉溶液,一份滴加KSCN溶液,前者变为蓝色,后者变为红色 | 溶液中存在平衡: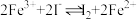 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
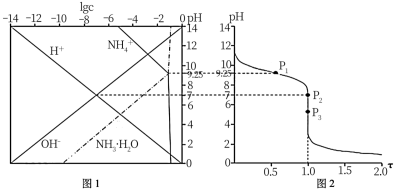
【推荐1】25℃时,用HCl气体调节0.1 mol·L-1氨水的pH,系统中微粒浓度的对数值(lgc)与pH的关系如图1所示,反应物的物质的量之比[ι= ]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
 ]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
]与pH的关系如图2所示。若忽略通过气体后溶液体积的变化,下列有关说法正确的是
| A.P1所示溶液:c(Cl-)=0.05 mol·L-1 |
| B.P2所示溶液:c(NH3·H2O)<c(OH-)+c(Cl-) |
C.P3所示溶液:c( )+c(NH3·H2O)=c(Cl-)+c(H+) )+c(NH3·H2O)=c(Cl-)+c(H+) |
| D.25℃时,NH3·H2O的电离平衡常数为10-4.75 |
您最近半年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】已知等体积等浓度的CH3COOH和CH3COONa溶液等体积混合后呈酸性。则0.4mol/L的CH3COONa与0.2mol/L的盐酸等体积混合后,下列关系正确的是( )
| A.c(CH3COO-) +c(CH3COOH) =0.4mol/L | B.c(Na+)>c(CH3COO-)>c(Cl-)>c(H+) |
| C.c(Na+)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) | D.c(CH3COO-)>c(CH3COOH) |
您最近半年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( )
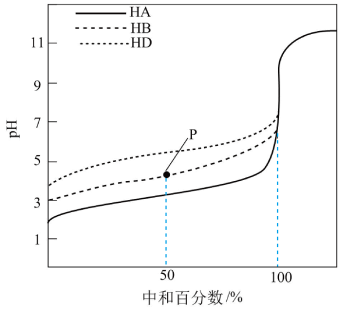

| A.三种酸的电离常数关系:KHA<KHB<KHD |
| B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) |
| C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) |
| D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+) |
您最近半年使用:0次
多选题
|
适中
(0.65)
【推荐1】室温下,下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
| A.20 mL 0.1 mol·L-1 CH3COONa溶液中加入0.1 mol·L-1盐酸至溶液pH=7:c(CH3COOH)=c(Cl-) |
| B.向澄清石灰水中通入Cl2至Ca(OH)2恰好完全反应:c(Ca2+)+c(H+)===c(OH-)+c(Cl-)+c(ClO-) |
| C.0.2 mol·L-1 CH3COOH溶液与0.1 mol·L-1 NaOH溶液等体积混合(pH<7):c(H+)+c(CH3COOH)>c(OH-)+c(CH3COO-) |
| D.0.1 mol·L-1 CH3COOH溶液与0.1 mol·L-1 Na2CO3溶液等体积混合(无气体逸出):c(CO32-)<c(CH3COOH)+c(H2CO3) |
您最近半年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】室温下,下列说法中不正确的是
| A.已知酸性:CH3COOH>H2CO3>HClO,则pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):③>②>① |
B.0.01mol/L NH4HCO3溶液中离子浓度:c(NH )>c(HCO )>c(HCO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| C.向NaHS溶液中加入等物质的量的KOH固体后:c(Na+)=c(H2S)+c(HS-)+2c(S2-) (忽略溶液温度的变化) |
| D.向含白色ZnS的悬浊液中滴入几滴CuSO4溶液,产生黑色沉淀可证明Ksp(ZnS)>Ksp(CuS) |
您最近半年使用:0次


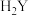 溶液中逐渐加入
溶液中逐渐加入 固体(忽略加入时引起的溶液体积变化),所得溶液中含Y元素的三种微粒的分布系数(浓度分数)
固体(忽略加入时引起的溶液体积变化),所得溶液中含Y元素的三种微粒的分布系数(浓度分数) 随溶液pH变化的关系如图所示,下列说法正确的是
随溶液pH变化的关系如图所示,下列说法正确的是 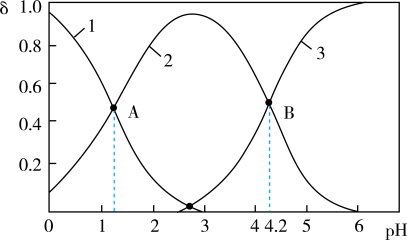
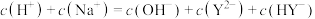
 时,溶液中的
时,溶液中的
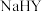 和
和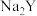 溶液等体积混合,所得溶液的
溶液等体积混合,所得溶液的
 的
的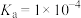 。若把少量
。若把少量 溶液中,发生的离子反应可表示为:
溶液中,发生的离子反应可表示为:


